서 론
재료 및 방법
공시재료 및 재배방법
유전자형 분석
발아 특성 평가(통제 발아 실험)
종피색 검정
통계분석
결과 및 고찰
유전자형 검정 결과
수발아 저항성 검정 결과
MFT-3A 유전자형과 발아 형질 간 연관성
Myb10 유전자와 수발아 형질 간 관계
Phenol 기반 종피색 score와 수발아 관련 발아 형질 간의 관계
적 요
서 론
밀(Triticum aestivum L.)은 쌀, 옥수수와 함께 세계 3대 식량작물로 분류되며, 전 세계 인구의 약 40% 이 주된 열량원으로 이용하는 작물이다. 밀은 인류 전체 에너지 섭취량의 약 20%와 단백질 섭취량의 약 25%를 차지하며, 다양한 가공식품의 원료로 활용되는 주요 곡류로서 단백질, 비타민, 식이섬유, 생리활성 물질, 무기질 등을 함유하고 있다(Ahn, 2002; Yang et al., 2021). 2024년도 기준, 우리나라의 1인당 연간 밀 소비량은 약 38.3 kg에 달하는 주요 식량작물이다. 그러나 밀은 기상과 재배환경의 영향을 크게 받는 작물로, 연차 및 재배지역에 따라 수량과 품질의 변이가 크게 나타난다. 특히 강우패턴, 생육기 온도, 출수기 및 성숙기의 기상조건은 단백질 함량과 전분 조성 등 품질에 직접적인 영향을 미쳐, 안정적인 원료곡 생산을 어렵게 하는 주요 요인으로 지적되고 있다(Kim et al., 2012; An et al., 2017; Lee et al., 2020; Park et al., 2023). 이로 인해 동일 품종이라 하더라도 재배연도 및 지역에 따라 품질 특성의 연차 변동성이 크게 나타나며, 제분 및 가공 적성의 안정적인 확보에 한계가 있는 것으로 보고되고 있다. 국내 밀 자급률은 2023년 기준 2.0%로 낮은 수준에 머물러 있으나(MAFRA, 2024), 이는 가격 경쟁력뿐 아니라 재배 및 품질 불안정 등이 복합적으로 작용한 결과로 볼 수 있다. 특히 국내 밀 재배는 논·밭 전환과 이모작 확대에 따라 재배시기와 환경조건이 다양화 되었고, 이로 인해 인한 장마, 집중강우, 고온 및 저온 스트레스 등 불리한 기상조건에 노출되는 빈도가 증가하고 있다. 이러한 기상환경은 수확기 전후 종실의 생리적 안정성을 저해하여 수발아(Pre-Harvest Sprouting, PHS) 발생 위험을 크게 높이는 주요 요인으로 작용한다.
수발아는 등숙 후기의 저온, 장시간 강우 및 다습한 환경, 수확 지연 등으로 이삭에서 종자가 비정상적으로 발아하는 현상으로, α-amylase 활성 증가에 따른 품위 저하, 제분·제빵 적성 저하, 저장성 악화 등을 초래한다(Shin et al., 2013; Jiang & Xiao, 2005). 특히 국내 이모작 재배 조건에서는 밀 등숙기 장마의 영향으로 이삭에 달린 종실의 수분 흡수가 촉진되며, 이후 반복되는 수분 흡수와 건조 과정으로 종실의 생리적 활력이 저하된다. 이로 인해 수확 후 종실의 발아력이 감소하고, 결과적으로 상품성 저하와 수량 손실 위험이 증가하는 경향이 관찰되었다(Park et al., 2024). 또한 밀의 주요 품질 형질에서 환경 효과는 유전 효과에 비해 약 5–6배 수준으로 크게 나타났으며, 이러한 결과는 내재해성 품종의 개발과 재배·수확 후 관리기술 개발이 병행되어야 함을 시사한다(Grausgruber et al., 2000; Zhu & Khan, 2001; Liu et al., 2019; Kang et al., 2024).
밀 수발아 저항성은 종피색, 이삭각도(ear angle), 까락 유무(awnless) 등의 형태학적 특성, ABA 신호 반응, 등의 생리학적 특성, 종자 휴면(Seed dormancy) 유전자 등 유전적 특성 등 다수의 요인에 의해 복합적으로 조절되는 형질이다(Chang et al., 2023; Kumar et al., 2023). 대표적인 종자 휴면 관련 유전자인 TaMFT는 종자 휴면과 발아 조절에 관여하는 MOTHER OF FT AND TFL1 (MFT) 계열에 속하는 유전자로, 수발아 저항성과 밀접한 관련이 있는 것으로 알려져 있다(Nakamura et al., 2011).
대표적으로 4A 염색체의 Phs-A1 좌위에서는 TaMKK3-A가 인과 유전자로 규명되었고, 3A염색체의 TaMFT-3A (TaPHS1) 역시 수발아 및 휴면에 영향을 미치는 것으로 보고되었다. 이와 함께 발아 억제 관련 TaVP1 (VP1/ABI3)과 종피색 관련 유전자인 Tamyb10간 간접적 연관성도 다수 보고되었다(Shorinola et al., 2017; Lin et al., 2018; Dallinger et al., 2024; Zhang et al., 2025; Nakamura et al., 2001; Liu et al., 2024; Lang et al., 2024; Zhu et al., 2023). 이러한 유전적 복잡성은 단일 좌위 도입만으로는 환경 변이에 안정적인 수발아 저항성을 확보하기 어려우며, 표적 좌위의 정밀 도입과 배경 회복을 병행하는 분자마커 선발(marker assisted selection)과 배경 선발(background selection)을 함께 적용하는 것이 효과적임을 시사한다(Lin et al., 2018; Chang et al., 2023; Kumar et al., 2023; Albrecht et al., 2024).
본 연구에서는 국내외 육성 자원을 대상으로 수발아 저항성 평가에 활용되어 온 발아 관련 형질을 통제된 발아 시험 조건에서 분석하고 그 결과를 바탕으로 기존 문헌에서 보고된 분자마커의 적용 가능성을 검토하였다. 이를 통해 수발아 저항성과 연관된 유전적·생리적 특성을 가진 자원을 탐색함으로써, 향후 이삭 기반 수발아 검정과 병행되는 수발아 저항성 육종 연구를 위한 기초 자료를 마련하고자 하였다. 본 결과는 발아 관련 형질과 연관된 분자마커 정보를 활용하여 재배환경 변동에 따른 품질 불안정성을 해석하는 데 보조적인 정보를 제공할 수 있을 것으로 판단된다. 아울러 수발아 저항성과 관련된 유전자형 정보는 교배 모·부본 선정을 위한 참고 자료로 활용될 수 있으며, 추후 현장 조건을 반영한 수발아 검정과 함께 적용될 경우 품질 안정성이 요구되는 재배 환경에서의 육종 연구에 기여할 수 있을 것으로 기대된다.
재료 및 방법
공시재료 및 재배방법
본 시험에서는 국내외 밀 품종 및 계통 164점을 시험재료로 사용하였다. 각 품종을 2024년 11월 12일에 국립식량과학원 밭작물개발부(밀양, 대한민국) 교배친 계통 포장(답리작)에서 N-P2O5-K2O를 9.1-7.4-3.9 kg/10a로 시비하고 품종당 4.5 m2 면적에 30×15 cm로 점파하여 재배하였다.
유전자형 분석
수발아 저항성을 판별하기 위해, 이전 연구에서 수발아와의 연관성이 보고된 TaMFT-3A 유전자의 −222 SNP 좌위를 표적으로 하는(Nakamura et al., 2011; Rasheed et al., 2016) KASP (Kompetitive Allele-Specific PCR) 마커 TaMFT_1617R을 이용하여 유전자형 분석을 수행하였다(Table 1). 본 마커는 TaMFT 유전자의 SNP를 기반으로 설계되었으며, FAM(A) 신호는 수발아 감수성과, HEX(G) 신호는 수발아 저항성과 각각 연관되는 것으로 보고된 바 있다. 본 연구에서는 선행 연구 결과를 바탕으로 FAM(A) 형을 수발아 감수성(Chinese Spring-type, CS형), HEX(G) 형을 저항성(Zenkoujikomugi-type, Zen형)으로 구분하였다(Nakamura et al., 2011; Chono et al., 2015; Rasheed et al., 2016).
Table 1.
KASP markers used for the selection of pre-harvest sprouting resistance in wheat cultivars and the germplasm.
| Primer name | Chr. | Gene | FAM primer | HEX primer | Common primer | Reference |
| TaMFT_1617R | 3A | TaMFT-A1 | A | G |
TGATCCATGC ACGCATCAG CGATCG | Rasheed et al. (2016) |
| Resistant | Susceptible | |||||
|
CGTGCATGCAGCCTA CGCATACGTA |
CGTGCATGCAGCCTA CGCATACGTG |
또한, 종피색을 검정하기 위해 종피색을 결정하는 주요 유전자로 알려진 Myb10 유전자에 대한 STS (Sequence-Tagged Site) 마커 분석을 병행하였다(Table 2).
Table 2.
Functional and linked gel-based markers used for the selection of pre-harvest sprouting resistance in wheat crossing parents and the germplasm.
| Marker name | Chr. | Gene | Forward primer (5’-3’) | Reverse primer (5’-3’) | Reference |
| Myb10-STS | 1D | Tamyb10-D1 |
TGCTGTGGAGGGGCGCAAG ATCAACTGG |
CGGATTGTGGAGGGGCGCA AGATCAACTGA | Lang et al. (2021) |
생육재생기 이후 1-2엽의 샘플을 채취한 뒤 Cetyltrimethylammonium bromide (CTAB, Doyle & Dolye, 1987) 방법을 이용하여 genomic DNA를 추출하였다. TaMFT_1617R 마커의 PCR 반응은 95℃에서 15분 간 초기 변성 후, 터치다운 사이클 10회(95℃에서 20초; 65℃에서 시작하여 매 사이클 마다 1℃씩 감소하며 25초간 반응)를 수행하고, 이후 추가 사이클 30회(95℃ 10초, 57℃ 60초)의 조건으로 진행하였다. STS 마커 PCR 반응은 94℃에서 5분간 초기 변성 후, 94℃에서 20초, 65℃에서 30초, 72℃에서 1분으로 40사이클 수행한 뒤 최종 신장은 72℃에서 7분간 실시하였다. 증폭 산물은 1.5% agarose gel electrophoresis로 확인하였다.
발아 특성 평가(통제 발아 실험)
생리적 성숙기부터 7일이 경과한 뒤 수확하여 건조 후 손탈곡하였다. 탈곡한 종자는 휴면성을 유지하기 위하여 검정 전까지 -20℃ 냉동고에 보관하였다. 수발아율 검정을 위하여 품종별로 50립의 종자를 90 × 15mm 페트리접시에 여과지 두 장과 증류수 3 ml를 넣고 배치한 후, 3반복으로 실시하여 22℃에서 7일간 배양하였다. 발아한 종자는 매일 계수한 뒤 제거하였다.
발아특성지표로는 발아율(mean germination percentage, MGP), 평균발아일수(mean germination time, MGT), 평균발아속도(mean germination speed, MGS) 및 발아지수(germination index, GI)를 조사하였다. MGP는 총 공시 종자 수 대비 최종 발아 종자 수의 백분율로 산출하였다(ISTA, 2015). MGT는 매일 발아한 종자 수와 발아까지 경과한 시간의 곱의 합을 총 발아 종자 수로 나누어 계산하였다(Ellis & Roberts, 1981). MGS는 매일 발아한 종자 수를 해당 일수로 나눈 값의 합으로 산출하였다(Maguire, 1962). GI는 파종 후 1일부터 7일까지 매일 발아한 종자 수에 대해 초기 발아에 더 높은 가중치를 부여하는 방식으로 계산하였다(Singh et al., 2012; Gao et al., 2024). 이때, ng는 시험 종료 시 최종 발아한 종자 수, nt는 총 공시 종자 수를 의미하며, ni는 파종 후 i번째 조사 시점에서 발아한 종자 수, ti는 파종 후 경과 시간을 나타낸다.
종피색 검정
밀 종피색은 유전적 요인에 의해 결정되며, 적립계 밀은 수발아에 대한 저항성을 나타내는 것으로 보고되어 있다(McIntosh et al., 2013). 본 연구에서는 종피색 판별을 위해 Phenol test를 실시하였다. Phenol 용액(CAS 108-95-2)은 증류수에 1% (w/v)로 제조하여 갈색병에 보관하였으며, 제조 후 24시간 이내에 사용하였다. 각 품종 및 계통 당 건전 종자 30립을 1반복으로 사용하였다. 수확한 종자는 수분함량은 약 11-13% 수준으로 자연건조하여 검정에 이용하였다. 종자는 수돗물에 16시간 침지한 후 표면의 물기를 제거하였고 종구가 아래로 향하도록 90 mm 페트리접시에 배치하고 뚜껑을 덮은 다음, 종자 크기의 약 3/4이 잠기도록 1% Phenol 용액 약 10 mL를 첨가하였다. 처리된 페트리접시는 20 ± 0.5℃ 암조건 챔버에 두고 4시간 동안 착색 변화를 관찰하였다. 종피 착색 정도는 국립종자원 특성조사기준(KSVS)에 따라 1-9 등급(1: 무착색, 3: 미약한 황갈색, 5: 연갈색, 7: 갈색, 9: 진한 갈색) 척도를 적용하되, 홀수 등급(1, 3, 5, 7, 9)을 시각적 판별 기준으로 설정하여 평가하였다. 두 명의 독립된 관찰자가 판정한 값의 평균을 취함으로써 등급 간 경계에 있는 시료에 대한 판정 정밀도를 높였다. 또한, 모든 시료는 동일한 조건에서 평가하였으며 착색 정도의 상대적 비교를 위해 적립 및 백립 표준 품종을 함께 배치하여 기준점으로 활용하였다. 모든 시료는 동일한 조명 조건에서 촬영 한 RGB 이미지를 HSV (Hue, Saturation, Value) 색공간으로 변환한 후 이미지로부터 채도(S)와 명도(V) 값을 추출하였다. 본 분석은 종자에 대한 페놀 처리 시 나타나는 종피색의 적변 정도를 정량적으로 평가하기 위한 것으로, 무처리 대비 색상 변화의 크기를 수치화하여 적립계와 백립계를 구분하고 적립계 내에서도 적변 강도의 차이를 등급별로 비교하기 위해 수행하였다. HSV 색공간은 색상과 밝기 정보를 분리하여 표현함으로써 RGB 색공간에 비해 조명 조건의 영향을 상대적으로 줄일 수 있어 페놀 반응에 따른 종피색 변화 평가에 적합한 색공간이다. HSV 값의 계산 및 등급 간 색도 차이 검증은 외부 이미지 분석 도구를 이용하여 수행하였다. 본 시험 방법은 국립종자원에서 개정한 작물별 특성조사기준(밀)을 참고하여 수행하였다(KSVS, 2015; UPOV, 2017).
통계분석
수발아 저항성 검정 결과에 대한 통계분석은 R Studio (version 4.4.1; R Studio, PBC, Boston, MA, USA)를 이용하여 수행하였다. 처리 간 평균 비교를 위해 분산분석(ANOVA)을 실시하였으며, 정규성 및 등분산성 가정을 만족하지 않는 경우에는 비모수 검정인 Kruskal–Wallis 검정을 적용하였다. 유의한 차이가 확인된 경우, 사후 검정으로는 ANOVA에는 Tukey의 HSD 검정을, Kruskal–Wallis 검정에는 Dunn 검정을 각각 사용하였다.
결과 및 고찰
유전자형 검정 결과
국내외 밀 품종에서 수발아 저항성과 관련된 다양한 유전자가 보고되어 있으며, 이 중 MFT-3A는 종자 휴면성과 밀접한 관련이 있는 주요 유전자 중 하나로 알려져 있다. 수발아 저항성과 연관된 대립유전자를 판별할 수 있는 분자표지의 유효성을 검정하기 위하여, 형광 기반 KASP 분자마커인 TaMFT_1617R를 이용한 유전자형 분석을 수행하였다(Fig. 1).
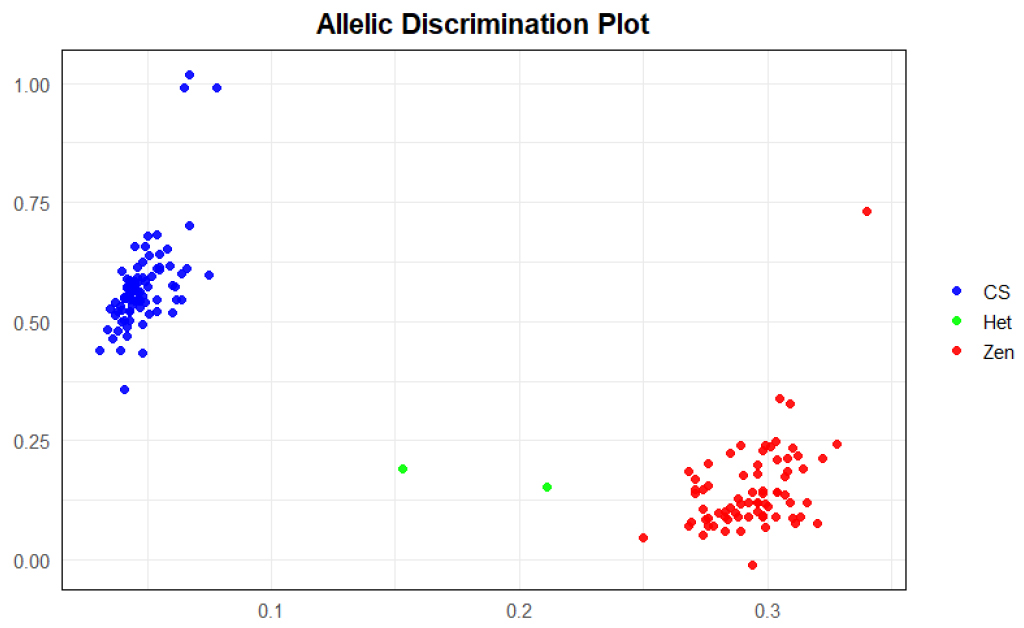
Fig. 1
Allelic discrimination plot obtained by KASP genotyping using the TaMFT_1617R marker in a panel of 164 wheat accessions comprising cultivars, breeding lines, and the germplasm. Red dots indicate Zen-type alleles (Zenkoujikomugi, n = 72) associated with resistance to pre-harvest sprouting (PHS), blue dots indicate CS-type alleles (Chinese Spring, n = 83) associated with susceptibility, and green dots indicate heterozygous genotypes (Heterozygous, n = 2). Seven samples were classified as no-calls. This analysis was conducted to determine the presence of MFT-3A alleles associated with PHS resistance.
본 마커는 Nakamura 등(2011)이 보고한 MFT-3A 프로모터 영역의 기능적 SNP를 검출하는 CAPS 마커 정보를 기반으로 개발되었으며, 3A 염색체 상의 MFT-3A 프로모터 SNP를 구분할 수 있다(Nakamura et al., 2011; Chono et al., 2015). 기존 연구에 따르면, 강한 종자 휴면성을 보이는 Zen형은 해당 프로모터 SNP가 G로 나타나며, 수발아에 취약한 CS형은 A로 확인된다(Nakamura et al., 2011). 이 SNP는 basic leucine zipper (bZIP) 계열 전사인자의 결합 부위로 알려진 A-box 모티프(TACGTA)를 절단(truncation)하여 MFT-3A 발현 조절에 영향을 미치는 것으로 보고되었다(Izawa et al., 1993; Nakamura et al., 2011).
TaMFT_1617R 마커를 적용한 결과, FAM 및 HEX 형광 신호가 각각 X축과 Y축으로 명확히 분리되어 Zen형(n = 72)과 CS형(n = 83) 유전자형이 뚜렷하게 구분되었다. 특히 기존 연구에서 수발아 감수성으로 보고된 Chinese Spring은 CS형으로 판별되었으며(Oda, 2015), 수발아 저항성으로 알려진 Alchanmil, Gosomil, Joah 등 5개 품종은 Zen형으로 분류되었다(Park et al., 2009; RDA, 2011; Shin et al., 2013; Kang et al., 2015). 이러한 결과는 본 마커가 선행연구에서 보고된 MFT-3A 유전자형–수발아 저항성 간의 연관성을 일관되게 재현함을 보여준다.
종피색과 연관된 Myb10 유전자는 종자 휴면 및 수발아 저항성과 밀접한 관련이 있는 것으로 제시되어 왔다(Wang et al., 2016; Lang et al., 2021). Lang 등(2021)은 수발아 저항성 QTL인 PHS-3D를 밀 3DL 염색체의 2.4 Mb PAV 영역으로 규명하고, 해당 저항성 효과가 Myb10-D에 의해 결정됨을 확인하였다. Myb10-D는 종피 색소 축적과 관련된 플라보노이드(카테킨 및 프로안토시아니딘) 생합성 경로를 조절하는 MYB 전사인자로 알려져 있으며, 저항성 하플로타입에서는 ABA 생합성 경로 활성화를 통해 종자 휴면이 강화되고 발아가 지연되는 것으로 제시되었다(Himi & Noda, 2005; Wang et al., 2016). 동일한 교배친 집단을 대상으로 STS-Myb10 마커 분석을 수행한 결과, 적립계 74계통과 백립계 90계통(계통 및 품종 포함)으로 구분되었다. 품종별로는 Alchanmil, Anbaekmil, Dajoongmil 등이 적립계로, Baekjoong, Baekkang, Dabunmil 등이 백립계로 분류되었다.
이러한 결과를 통하여 STS-Myb10 마커는 교배친 집단 내 종피색 유전자형을 안정적으로 구분하였으며, TaMFT_1617R 마커는 MFT-3A 유전자형 판별에 활용 가능함을 확인하였다. 이후 절에서는 두 유전자 마커 분석 결과를 종합하여, Myb10과 MFT-3A 유전자형 간의 분포 특성과 유전자형 및 수발아 검정 결과 간의 상관관계를 추가로 분석하였다.
수발아 저항성 검정 결과
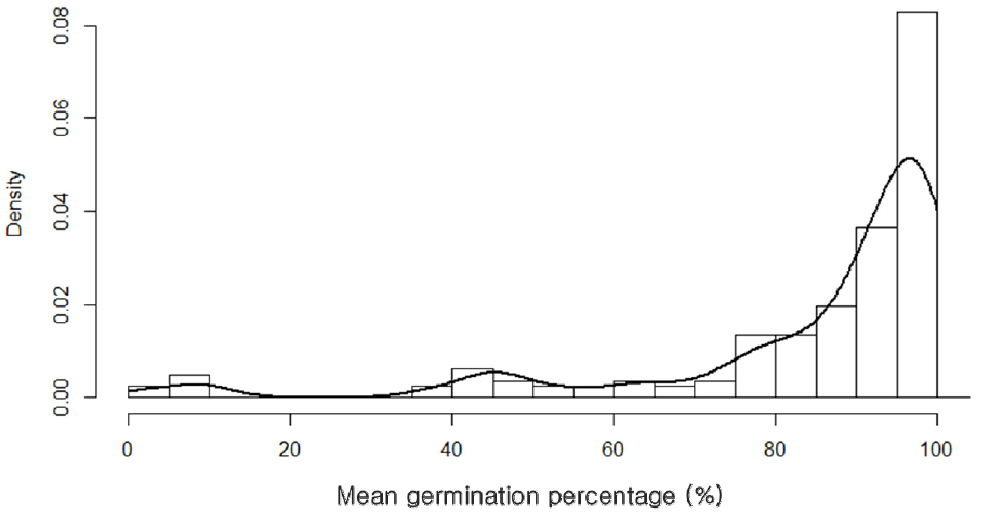
교배친 164점을 대상으로 수발아 검정을 실시한 결과, MGP는 6.6%에서 100%까지 연속적으로 분포하여 시험 재료 간 폭넓은 표현형 변이가 관찰되었다(Fig. 2). 이 중 Arijinheuk, BETHLEHEM, Suwon281 등 일부 품종 및 계통은 MGP가 낮아 발아가 강하게 억제되는 양상을 보인 반면, Olmil, Junggye4742 등은 MGP가 높아 수발아에 취약할 것으로 예상되었다. 이러한 발아 및 종자 휴면 특성이 다유전자적 요인과 환경 요인의 복합적 상호작용에 의해 조절된다는 기존 보고와 일치한다(Finch-Savage & Leubner-Metzger, 2006; Gao & Ayele, 2014; Penning et al., 2023). 한편, GI는 품종 간 발아 진행 속도와 균일성의 차이를 반영하는 지표로서 넓은 범위로 분포하였다. MGP가 매우 낮은 일부 계통에서는 제한된 수의 발아 개체에 의해 GI 값이 상대적으로 크게 나타나는 경우도 관찰되었으며, 이에 본 연구에서는 GI를 수발아 저항성의 직접 지표라기보다는 발아 특성 해석을 위한 보조 지표로 활용하였다.
MFT-3A 대립유전자형(저항성/감수성)과 Myb10 유전자형(적립/백립)을 고정요인으로 하고, 각 교배친을 독립 관측치로 하는 선형모형 기반 요인분석을 수행하였다(Table 3). 그 결과, MGP에서는 MFT-3A 유전자의 주효과가 유의하지 않았으며(p = 0.2814), Myb10 유전자의 주효과 또한 통계적으로 유의하지는 않았으나 유의수준에 근접한 경향을 보였다(p = 0.0636). MGT에서는 MFT-3A 유전자의 주효과가 유의하게 나타났으며(p = 0.0037), 대립유전자형에 따라 발아 개시 시점의 차이가 관찰되었다. 반면, Myb10의 주효과와 MFT-3A × Myb10 상호작용은 유의하지 않았다(p = 0.3409, 0.4566). MGS에서는 Myb10 유전자의 주효과가 유의하게 나타났으며(p = 0.0361), 백립계 품종에서 상대적으로 높은 발아속도가 관찰되었다. 모든 형질에서 MFT-3A × Myb10 상호작용은 통계적으로 유의하지 않았다(p > 0.05).
Table 3.
Results of linear model–based factorial analysis examining the effects of MFT-3A allele type and Myb10 genotype on germination-related traits in wheat. Analyses were conducted using each accession as an independent observation, with MFT-3A allele type (resistant vs. susceptible), Myb10 genotype (red vs. white grain), and their interaction included as fixed effects.
MFT-3A 유전자형과 발아 형질 간 연관성
TaMFT_1617R 마커로 분류된 유전자형에 따라 발아 관련 형질의 분포를 비교한 결과, 형질 별로 유전자형 간 차이의 정도가 상이하게 나타났다(Fig. 3). MGP의 경우, 두가지 유형 모두에서 약 90–100%의 높은 발아율 구간에 분포가 집중되었으며, 두 유전자형 집단 간 분포가 크게 중첩되어 유전자형에 따른 뚜렷한 차이는 관찰되지 않았다(Fig. 3A).
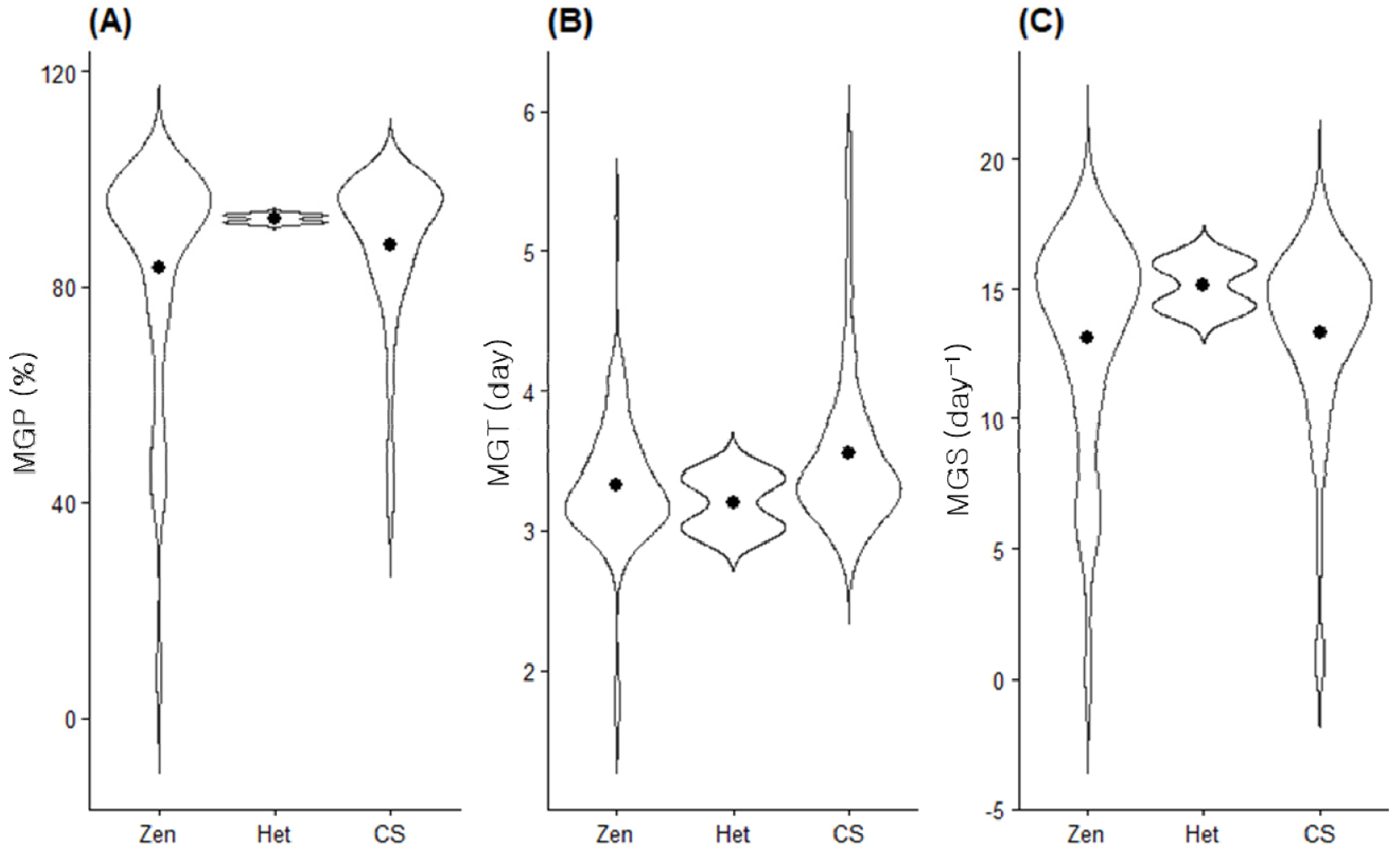
Fig. 3
Distribution of germination-related traits according to TaMFT-1617R genotype in wheat. Violin plots illustrating the distribution of (A) mean germination percentage (MGP), (B) mean germination time (MGT), and (C) mean germination speed (MGS) across Zen-type (Zen), heterozygous (Het), and CS-type (CS) allele groups. The width of each violin represents the kernel density of the data, and the black dots indicate mean values.
MGT는 두 유형 모두에서 유사한 범위로 분포하였으나, 분포의 중심 위치에는 차이가 나타났다. Zen형은 CS형에 비해 발아가 상대적으로 빠르게 개시된 계통들이 다수 포함되어, 중앙값이 낮은 방향으로 이동하는 경향을 보였다(Fig. 3B). 이는 통제된 탈곡 종자 발아 조건에서 Zen형 계통이 상대적으로 빠른 발아 개시를 나타냈음을 의미한다. 다만, 본 시험은 이삭에 부착된 상태에서의 수발아를 직접적으로 평가한 것이 아니라, 충분한 수분이 공급되는 실내 발아 조건에서 수행되었으므로, 이러한 결과를 실제 수발아 저항성과 동일하게 해석하기에는 한계가 있다. 또한, 동일 유전자형 내에서도 발아 개시 시점에 변이가 존재하여, 일부 계통에서는 발아 지연 현상도 함께 관찰되었다.
MGS의 경우, CS형과 Zen형 계통 모두에서 중간에서 높은 발아속도 구간에 분포가 집중되었으며, 두 유전자형 간 분포 양상은 전반적으로 유사하였다(Fig. 3C). 이는 발아가 시작된 이후의 진행 속도 측면에서는 TaMFT_1617R 유전자형에 따른 차이가 크지 않음을 의미한다.
분산분석 결과(Table 4), MGP와 MGS는 유전자형 간 통계적으로 유의한 차이를 보이지 않았다(p = 0.315, 0.733). 반면, MGT에서는 유전자형 간 유의한 차이가 확인되었으며(p = 0.027), Zen형 계통이 CS형 계통에 비해 평균적으로 더 짧은 발아일수를 나타냈다. 이러한 결과는 TaMFT_1617R 마커가 발아율이나 발아속도보다는 발아 개시 시점과 보다 밀접하게 연관될 가능성을 시사한다.
Table 4.
Germination-related traits according to TaMFT genotype in wheat.
| Genotype | n | MGP (%) | MGT (days) | MGS (day-1) |
| CS | 83 | 87.9 ± 14.4 | 3.55 ± 0.58a | 13.3 ± 3.6 |
| Het | 2 | 92.7 ± 0.94 | 3.20 ± 0.26ab | 15.2 ± 1.2 |
| Zen | 72 | 83.7 ± 21.6 | 3.32 ± 0.48b | 13.1 ± 4.2 |
| p-value | - | 0.315 | 0.027* | 0.733 |
그러나 본 연구에서 관찰된 MGT의 차이는 유전자형 집단 간 분포가 상당 부분 중첩되는 양상을 보였으며, 효과 크기 또한 제한적인 수준이었다. 따라서 본 연구 조건에서 TaMFT_1617R 마커를 이용하여 발아 형질만으로 CS형과 Zen형 계통을 명확히 구분하기에는 한계가 있는 것으로 판단된다. 향후 다습 또는 인공강우 조건에서의 이삭 발아율, α-amylase 활성, falling number (FN) 분석과 같은 추가적인 표현형 검정을 통해 유전자형 효과를 보다 정밀하게 검증할 필요가 있을 것으로 사료된다(Depauw et al., 2012; Gavazza et al., 2012; Mares & Mrva, 2014).
Myb10 유전자와 수발아 형질 간 관계
밀의 종피색은 유전적으로 조절되는 형질로, 일반적으로 적립계 밀 품종은 백립계 품종에 비해 수발아에 강한 것으로 보고되어 왔다. 종피색과 수발아 저항성에는 공통으로 관여하는 여러 QTL 및 유전자가 보고되어 있으며, 대표적으로 Tamyb10-A1과 Tamyb10-D1 등이 알려져 있다. 이러한 유전자들은 종자 휴면 및 발아 반응과 밀접하게 연관되어 있어, 종피색은 수발아 저항성 평가에서 보조 지표로 활용되어 왔다(Himi et al., 2011; Bassoi & Flintham, 2005; Lin et al., 2018; Wang et al., 2016; Chen et al., 2025). Myb10은 flavonoid 생합성을 조절하는 R2R3-MYB 전사인자로, 밀에서 적색 종피 형성을 결정하는 핵심 유전자로 알려져 있으며 종피색과 종자 휴면에 관여해 수발아 저항성과 간접적으로 연관되는 것으로 보고된 바 있다(Himi et al., 2002; Himi & Noda, 2005). 본 연구에서는 STS-Myb10 마커를 이용한 유전자형 분류와 Phenol 반응에 기반한 종피색 score(1–9)를 함께 적용하여, 종피색 관련 유전적·표현형적 요인과 발아 형질 간의 관계를 단계적으로 분석하였다(Chang et al., 2023).
이와 같은 배경을 바탕으로, Myb10의 독립적인 효과는 이미 요인분석 기반 통계모형을 통해 평가하였으며(Table 3), Table 5는 해당 통계적 결과를 보조적으로 해석하기 위해 Myb10 유전자형에 따른 적립과 백립 간 발아형질의 차이를 직관적으로 비교 및 제시한 것이다.
Myb10 유전자형에 따른 발아 형질 비교 결과(Table 5), MGP와 MGT에서는 백립계와 적립계 간 통계적으로 유의한 차이가 관찰되지 않았다. 이는 본 연구에서 설정한 조건하에서는 종피색과 연관된 유전적 배경이 발아율이나 평균적인 발아 시점을 단독으로 설명하기에는 제한적임을 시사한다. 적립계 밀의 수발아와 연관된 특성은 종피에 축적된 페놀성 화합물 등에 의해 수분 흡수가 지연되는 물리·화학적 특성과 관련된 것으로 보고되어 있으며, 이러한 기작은 이론적으로 발아 개시 시점의 지연으로 나타날 가능성이 있다. 그러나 본 연구에서는 탈곡 종자를 이용한 시험조건에서 충분한 수분이 직접 공급됨에 따라, 종피 투과성 차이에 따른 초기 수분흡수 지연효과가 완충되었을 가능성이 있으며, 이로 인해 Myb10 유전자형 간 발아 개시 시점의 차이가 명확하게 반영되지 않았을 수 있다.
아울러 본 연구에서 평가한 발아 관련 형질(GP, MGT, MGS)은 탈곡 종자를 이용한 통제된 실내 발아 시험을 통해 측정되었으며, 이삭 상태에서 발생하는 실제 수발아를 직접적으로 평가한 것은 아니다. 선행연구들에서 보고된 Myb10 유전자 및 종피색과 수발아 저항성 간의 강한 연관성은 주로 이삭 기반 발아 시험 또는 강우 조건을 모사한 환경에서 관찰된 결과로, 종피에 축적된 색소 및 페놀성 화합물이 수분 흡수를 지연시키는 물리·화학적 효과가 주요 기작으로 제시되어 왔다. 이에 비해, 본 연구와 같이 탈곡 종자에 충분한 수분이 직접 공급되는 발아 시험 조건에서는 이러한 종피 관련 효과가 상대적으로 완화될 수 있으며, 이로 인해 Myb10 유전자형과 발아율 또는 발아 개시 시점 간의 연관성이 기존 연구에 비해 약하게 관찰되었을 가능성이 있다.
반면, MGS에서는 Myb10 유전자형 간 유의한 차이가 확인되었으며(p = 0.040; Table 5), 이는 종피색과 연관된 유전적 요인이 발아의 전반적인 진행 속도, 특히 발아 초기 단계의 발아 양상과는 부분적으로 연관될 가능성을 시사한다. MGT가 전체 발아 개체의 발아 시점을 평균적으로 반영하는 지표인 반면, MGS는 발아 초기에 출현하는 발아 개체의 비율과 발아진행속도에 보다 민감하게 반응하는 지표이므로, 종피색과 관련된 유전적 요인의 영향이 MGT보다 MGS에서 상대적으로 더 뚜렷하게 관찰된 것은 발아 지표의 특성 차이에 기인한 결과로 해석될 수 있다.
Table 5.
Germination-related traits according to Myb10 genotype in wheat. MGP, MGT, and MGS were evaluated to assess the effect of seed coat color–associated Myb10 markers.
| STS-Myb10 | n | MGP (%) | MGT (days) | MGS (day-1) |
| Red | 74 | 82.9 ± 20.8 | 3.51 ± 0.64 | 12.44 ± 4.73b |
| White | 90 | 87.7 ± 16.3 | 3.39 ± 0.45 | 12.7 ± 4.73a |
| p-value | - | 0.099 | 0.162 | 0.040* |
Values are presented as means ± SE. Statistical significance was determined using one-way ANOVA (p < 0.05). This table presents a one-factor analysis based on Myb10 genotype, whereas statistical inference accounting for the effect of MFT-3A and its interactions were based on the factorial model shown in Table 3.
종합하면, Myb10 유전자형 및 Phenol 반응을 기반으로 한 종피색 분류는 발아 형질 중 특히 MGS와는 부분적으로 연관되는 경향을 보였으나, 본 연구 조건에서는 수발아 저항성의 핵심 지표로 간주되는 MGP나 MGT을 명확히 구분할 수준의 효과는 확인되지 않았다. 따라서 종피색 관련 지표는 수발아 저항성과 관련된 생리적 특성을 해석하는 보조 지표로 활용되기보다는, 다른 유전적 요인 또는 환경 조건을 반영한 표현형 검정과 병행하여 보조적으로 활용하는 것이 타당할 것으로 판단된다.
Phenol 기반 종피색 score와 수발아 관련 발아 형질 간의 관계
종피색은 Myb10 유전자형에 의해 크게 구분되지만(Himi et al., 2011; Wang et al., 2016), 동일 유전자형 내에서도 착색 강도에는 연속적인 표현형 변이가 존재한다(Bassoi & Flintham, 2005; Ruud et al., 2025). 이러한 표현형적 분산이 발아 형질과 어떻게 연관되는지를 평가하기 위해, Phenol 반응에 기반한 종피색 score를 기준으로 발아 관련 형질을 추가 분석하였다. 종피색 score(1–9)에 따라 자원을 그룹화한 후 MGP, MGT, MGS에 대해 ANOVA를 수행하였다. Phenol 반응에 따른 종피색 score 그룹별 평균 발아 형질은 Table 6에 제시하였다. MGP와 MGT는 score 그룹 간 평균값 차이가 크지 않았으며, MGS에서는 일부 score 그룹에서 상대적으로 낮은 값을 나타내는 경향이 관찰되었다.
Table 6.
Mean germination traits across seed coat color score classes. MGP, MGT, and MGS are presented for each score class. Although differences in mean MGP values were observed among score classes, no consistent increasing or decreasing trends were detected across scores.
Score 등급에 따른 발아 형질의 분산분석 결과(Table 7), MGP와 MGT에서는 score 그룹 간 통계적으로 유의한 차이가 확인되지 않았다. MGP의 경우 일부 score 그룹에서 발아율 분포의 차이가 관찰되었으나, 집단 간 중앙값 차이보다 집단 내 분산이 상대적으로 크게 나타났다(Fig. 4A). MGT 또한 score 그룹 전반에서 유사한 범위를 보여, 발아 개시 시점은 종피색 score에 의해 뚜렷하게 구분되지 않는 경향을 보였다(Fig. 4B). 반면, MGS에서는 score 그룹 간 통계적으로 유의한 차이가 확인되었으며(F = 2.659, p = 0.0348; Table 7), Figure 4C에서와 같이 일부 중간 score그룹에서는 상대적으로 높은 발아속도를 보인 반면, score 7 그룹에서는 발아속도가 감소하는 경향이 관찰되었다.
Table 7.
ANOVA results for germination-related traits across score groups.
| Trait | F | p-value |
| MGP (%) | 1.621 | 0.1716 |
| MGT (days) | 2.114 | 0.0815 |
| MGS (day-1) | 2.659 | 0.0348* |
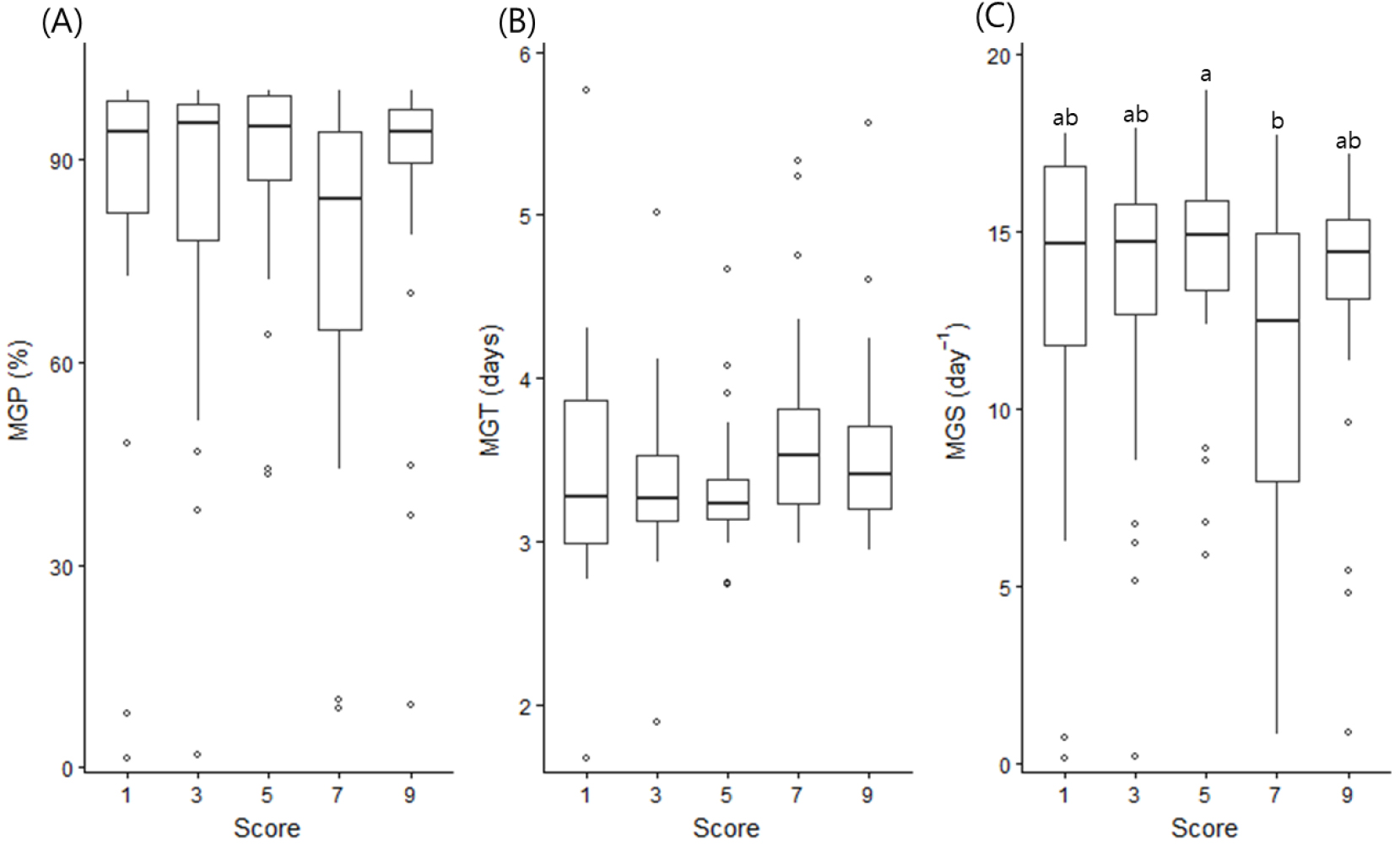
Fig. 4
Boxplots illustrating variations in germination-related traits across seed coat color score groups. (A) MGP, (B) MGT, and (C) MGS are shown for each score class. Boxes represent interquartile range, horizontal lines indicate medians, and open circles denote outliers. Different letters above the boxes indicate significant differences among score groups based on one-way ANOVA followed by Tukey’s HSD test (p < 0.05).
이러한 결과는 종피색을 반영하는 score가 발아 진행 속도와는 일정 부분 연관될 수 있으나, 발아율이나 발아 개시 시점을 단독으로 설명하기에는 한계가 있음을 시사한다. 이는 종피색이 수발아 저항성에 영향을 미치는 여러 요인 중 하나의 표현형적 지표로 작용할 가능성을 보여준다.
적 요
1.본 연구는 수발아 저항성과 관련된 TaMFT 유전자 기반 KASP 마커(TaMFT_1617R)를 국내외 밀 교배친에 적용하고, 발아 관련 형질과의 연관성을 분석하여 수발아 저항성 육종소재 선발을 위한 기초자료를 확보하고자 수행하였다.
2.국내외 밀 품종 및 자원 164점을 대상으로 유전자형을 분석한 결과, MGP와 MGS에서는 TaMFT 유전자형 간 유의한 차이가 관찰되지 않았으나, MGT에서는 유의한 차이가 확인되어 Zen형 품종이 CS형에 비해 평균적으로 짧은 발아일수를 나타냈다.
3.종피색(Myb10) 및 Phenol 반응 기반 분석에서는 MGS에서만 유의한 차이가 관찰되었으며, 종피색 단독으로는 수발아 저항성을 충분히 설명하기 어려웠다.
4.이상의 결과는 TaMFT_1617R 마커가 통제된 발아 시험 조건에서 발아 개시 시점과 일부 연관될 수 있음을 보여주며, 수발아 저항성과의 관계를 해석하기 위한 기초 정보로 활용될 수 있음을 시사한다. 다만, 실제 수발아 저항성 육종에의 적용을 위해서는 이삭 기반 수발아 검정을 포함한 추가적인 표현형 평가가 필요함을 보여준다.