서 론
재료 및 방법
콩 생육초기 바이러스병 조사를 위한 시료 채집
콩 감염 바이러스의 RT-PCR 진단
메타전사체 분석을 이용한 바이러스의 탐색
메타전사체 분석으로 검출된 새로운 바이러스의 검정
결 과
콩 생육초기 바이러스 감염주 채집 및 발병율
콩 생육초기 감염 바이러스의 RT-PCR 진단
메타전사체 분석을 통하여 탐색된 식물바이러스
콩 생육초기 감염 바이러스에 따른 병징
고 찰
적 요
서 론
콩(Glycine max)은 우리나라에서 재배면적이 55,008 ha로 연간생산량은 80,926 t이며, 연간생산액은 4,082억 원에 달하는 주요 식량작물이다(MAFRARK, 2021). 한반도를 포함한 동북아시아 일대는 콩의 야생형인 돌콩(Glycine soja)이 널리 분포하고 콩 품종의 유전적 다양성이 매우 높아 콩의 발원지로 알려져 있다(Lee & Park, 2006; Lee et al., 2008). 또한 콩에 발생하는 바이러스병도 오랜 기간의 상호작용 결과로 높은 다양성과 큰 유전적 변이를 나타낸다(Kim et al., 2003; Lim et al., 2003).
과거 우리나라 콩 바이러스병 연구는 지표식물을 이용한 생물검정, 전자현미경 검경, 혈청학적 진단 등을 주로 수행하였고, 그 결과 Soybean mosaic virus (SMV), Cucumber mosaic virus (CMV), Alfalfa mosaic virus (AMV)가 차례로 보고되었다(Cho & Chung, 1976; Lee et al., 1980, 1985). 이 중에서 SMV는 종자전염과 충매전염으로 인하여 엄청난 경제적 피해를 끼치는 바이러스병으로 확인되었다. 이에 따라 SMV에 대한 분류, 전염, 저항성 등 다양한 연구가 수행되었으며(Cho, 1981, 1995; Cho & Chung, 1976; Cho & Goodman, 1982; Cho et al., 1984), 그 결과 SMV 저항성 품종 육성과 보급 사업이 활발하게 이루어졌다. 이러한 노력으로 SMV에 의한 피해는 과거보다 현저히 감소한 것으로 판단되지만 콩 포장에서 바이러스병의 발생은 여전히 계속되고 있다. 최근 분자생물학적 방법을 사용한 다수의 콩 바이러스병 관련 연구들로 12종의 바이러스가 국내에서 보고되었다(Table 1). 최근 수행된 연구들에 따르면 우리나라 콩 재배지에는 SMV, SYMMV, SYCMV가 주요 병원체로 판단된다(Cho et al., 2013; Lee et al., 2012; Seo et al., 2014). 한편, 지금까지 수행된 바이러스병 조사는 콩 생육 중·후기에 주로 수행되었으며, 생육 초기의 바이러스병 발생 양상은 구체적으로 확인되지 않았다. 우리나라의 콩 소면적 자가채종 포장을 대상으로 수행한 조사에서 콩 바이러스 3종(SMV, SYMMV, SYCMV)의 발생양상은 조사 시기에 따라 현격히 달라진다는 것이 확인되었다(Cho et al., 2013). 본 연구에서는 콩 바이러스병 관리대책을 수립하기 위한 기초자료 확보를 위하여 RT-PCR 진단 및 메타전사체 분석으로 통하여 생육초기 발생하는 바이러스병의 종류와 감염실태를 조사하였다.
Table 1.
List of viruses found in soybean in Korea.
| Virus | Acronym |
Mode of transmissiona | Particle morphology | Reference |
| Alfalfa mosaic virus | AMV | Aphids, seed |
Non-enveloped, bacilliform with a diameter of 18 nm | Lee et al., 1985 |
| Bean common mosaic virus | BCMV | Aphids, seed |
Non-enveloped, flexuous, and filamentous rod-shaped with 750 nm long | Lee et al., 2015 |
| Clover yellow vein virus | ClYVV | Aphids |
Non-enveloped, flexuous, and filamentous rod-shaped with a length of 760 nm | Shin et al., 2014 |
| Cowpea mosaic virus | CPMV | Beetles, thrips |
Non-enveloped, icosahedral capsid with a diameter of 30 nm | Cho & Lee, 2003 |
| Cucumber mosaic virus | CMV | Aphids, seed |
Non-enveloped, encapsidated in isometric particle with a diameter of 30 nm | Lee et al., 1980 |
| Peanut mottle virus | PeMoV | Aphids, seed |
Non-enveloped, flexuous, filamentous rod-shaped with an approximate length of 750 nm | Lim et al., 2014 |
| Peanut stunt virus | PSV | Aphids, seed |
Non-enveloped, encapsidated in isometric particle with a diameter of 30 nm | Nam et al., 2012b |
| Soybean dwarf virus | SbDV | Aphids |
Non-enveloped, spherical virion with a diameter of 25-30 nm | Kim et al., 2006 |
| Soybean mosaic virus | SMV | Aphids, seed |
Non-enveloped, flexuous, filamentous rod-shaped with a length of 750 nm | Cho & Chung, 1976 |
| Soybean yellow common mosaic virus | SYCMV | Unknown |
Non-enveloped, icosahedral capsid structure with a diameter of 30 nm | Nam et al., 2012a |
| Soybean yellow mottle mosaic virus | SYMMV | Beetles, seed |
Non-enveloped, spherical, icosahedral capsid with a diameter of 28-34 nm | Nam et al., 2009 |
| Tomato spotted wilt virus | TSWV | Thrips, seed |
Enveloped, spherical with a diameter of 80-120 nm | Yoon et al., 2017 |
재료 및 방법
콩 생육초기 바이러스병 조사를 위한 시료 채집
콩 생육초기에 발생하는 바이러스를 조사하기 위하여 다양한 품종과 육종계통이 재배되고 있는 국립식량과학원 남부작물부 대구시험지(대구 달성군) 콩 육종포장을 채집대상으로 선정하였다. 2020년 6월 초·중순에 4차례의 조사를 통하여, 콩 파종 후 약 3-4주 된 식물체로부터 전형적인 바이러스 병징을 나타내는 잎 시료와 다양한 이상증상을 나타내는 시료를 다양하게 채집하였다. 채집된 시료의 병징은 모자이크(mosaic), 황화(yellowing), 퇴록반점(chlorotic spot), 위축(stunt) 등의 이상증상과 무병징(symptomless)을 포함하고 있다. 채집한 시료는 소량으로 나누어 –80°C 초저온냉동고에 보관하면서 바이러스 진단 및 동정에 사용하였다.
콩 감염 바이러스의 RT-PCR 진단
RT-PCR 진단을 위한 전체 RNA 분리는 easy-spinTM Total RNA Extraction Kit (iNtRON, Seongnam, Korea)를 이용하여 제공사의 매뉴얼에 따라 수행하였다. 콩 잎 시료 약 50 mg을 사용하여 전체 RNA를 분리하였으며, 최종적으로 50 µl의 elution buffer로 추출하여 RT-PCR 진단에 사용하였다. RT-PCR 진단은 지금까지 우리나라 콩에 발생보고된 11종 바이러스(AMV, BCMV, ClYVV, CMV, PeMoV, PSV, SbDV, SMV, SYCMV, SYMMV, TSWV)를 대상으로 수행하였다. 11종 바이러스에 대한 개별 시료 83점의 효율적이고 경제적인 진단을 위하여 4가지 조합의 다중진단법을 이용하였다(Table 2). 각각의 다중진단법 조합의 대상 바이러스는 다음과 같다 : 세트 1; AMV, SYCMV, SYMMV, 세트 2; PSV, SbDV, SMV; 세트 3; PeMoV, TSWV, ClYVV; 세트 4; CMV, BCMV. RT-PCR 조건은 특허(Lee et al., 2011) 및 논문(Park et al., 2018; Lee et al., 2004)에 기재된 방법으로 수행하였으며, RT-PCR 반응액은 SuPrimeScript RT-PCR Premix (GeNet Bio, Nonsan, Korea)을 이용하였다.
Table 2.
Primer sets for multiplex RT-PCR of 11 soybean virus species.a
aEach set of primers represent a diagnostic method using multiplex RT-PCR of soybean viruses developed in separate studies; sets 1 and 2: Lee et al., 2011; set 3: Park et al., 2018; set 4: Lee et al., 2004.
bAMV: Alfalfa mosaic virus, SYCMV: Soybean yellow common mosaic virus, SYMMV: Soybean yellow mottle mosaic virus, PSV: Peanut stunt virus, SbDV: Soybean dwarf virus, SMV: Soybean mosaic virus, PeMoV: Peanut mottle virus, TSWV: Tomato spotted wilt virus, ClYVV: Clover yellow vein virus, CMV: Cucumber mosaic virus, and BCMV: Bean common mosaic virus.
메타전사체 분석을 이용한 바이러스의 탐색
국내 보고된 11종 바이러스 이외의 미보고 및 신종 바이러스를 추가적으로 탐색하고, 또한 콩 생육초기 바이러스 병징과 유사한 증상을 나타내는 RT-PCR 음성반응 시료에 대한 검증을 위하여 차세대염기서열분석법(next generation sequencing, NGS)을 이용한 메타전사체 분석을 수행하였다. 채집한 콩 시료 83점을 하나의 검체로 집단화(pooling)하여, Maxwell® 16 LEV Plant RNA Kit (Promega, Madison, USA)를 이용하여 전체 RNA를 추출하였다. 추출된 전체 RNA를 TruSeq Stranded Total RNA LT Sample Prep Kit (Illumina, San Diego, USA)로 단일 라이브러리(single library)를 제작하였다. 라이브러리의 시퀀싱은 HiSeq 4000 system (Illumina, San Diego, USA)를 이용하여 101 bp paired end 방식으로 수행하였다(Macrogen, Seoul, Korea). 이를 통하여 약 40 Gbp의 미가공 데이터(raw data)를 생산하였으며, 획득한 원시데이터를 Trinity software version trinityrnaseq_r20140717를 이용하여 de novo 조립(assemble)하여 컨티그(contig)를 생산하였다. 어노테이션(annotation)은 조립된 컨티그를 공공 생물정보 데이터베이스인 Gene ontology (GO), UniProt, NCBI non-redundant protein (NR), Pfam, EggNOG, NCBI nucleotide (NT), Kyoto Encyclopedia of Genes and Genomes (KEGG)를 기반으로 NCBI BLASTn 및 BLASTx (DIAMOND software version 0.9.21) 분석을 통하여 수행되었다. 바이러스와 관련된 것으로 분석된 컨티그는 NCBI BLASTn·BLASTx search를 통하여 재검증하여 식물바이러스와 관련된 컨티그를 확보하였다.
메타전사체 분석으로 검출된 새로운 바이러스의 검정
RT-PCR 분석대상 11종 바이러스 이외의 메타전사체 분석으로 검출된 바이러스는 획득 컨티그 및 기보고 NCBI GenBank 염기서열을 바탕으로 프라이머를 설계하고, RT-PCR 진단 및 반응산물의 염기서열 결정으로 감염 여부를 확인하였다. 메타전사체 분석으로 획득한 Soybean geminivirus A (SGVA, 가칭) 관련 컨티그를 검정하기 위하여 프라이머 SGVA-F744 (5’-GCT ACT TTG TTA AGG GAT CAG TC-3’)와 SGVA-R1668 (5’-GAA TCG GAA TTT GAA ACA GTG G-3’)를 설계하였다. 프라이머는 SGVA 관련 컨티그의 염기서열을 바탕으로 설계하였으며, 반응 산물의 예상 크기는 925 bp이다. RT-PCR 반응 산물의 염기서열은 마크로젠사(Seoul, Korea)에 의뢰하여 결정하였다. 또한 SGVA의 감염 여부를 확인하기 위하여 채집시료를 대상으로 RT-PCR 진단을 수행하였다.
결 과
콩 생육초기 바이러스 감염주 채집 및 발병율
콩 생육초기 바이러스병 발생 양상을 조사하기 위하여 국립식량과학원 콩 육종포장(대구시험지)에서 파종 후 약 3-4주 된 생육초기에 바이러스병 시료를 채집하였다. 콩 품종 및 계통의 파종 시기 차이로 인하여 네 차례의 조사를 실시하였고, 그 결과 83점의 바이러스 병징을 보이는 시료를 채집하였다(Table 3). 이 시기에 주로 관찰되는 바이러스 병징은 모자이크, 황화, 퇴록반점, 위축 등 이었으며, 바이러스 병징을 나타내는 콩은 전체의 1% 미만이었다. 2020년도 국립식량과학원 육종포장에는 약 60종의 품종과 약 50 조합의 F2 및 F3 계통이 재배되었으며(국립식량과학원, 자료 미공), 본 조사에서는 10 품종 및 25 라인(line)에서 바이러스 병징을 나타내는 시료를 채집할 수 있었다(Table 3). 이 시기 바이러스 발병율은 콩 품종과 라인에 따라 매우 큰 차이를 보였다. 대부분의 콩 품종에서는 뚜렷한 바이러스 병징이 관찰되지 않거나, 극히 일부의 개체만 발병하였다. 그러나 청자5호(Cheongja5ho)와 미풍(Mipung)은 각각 약 30%와 10%의 높은 발병율을 나타내었다. F2 및 F3 계통의 라인에서도 대부분은 생육초기 뚜렷한 바이러스 병징을 관찰하기 힘들었다. 하지만 일부의 라인에서는 바이러스 병징을 보이는 감염주를 확인할 수 있었고, 특히 OB13086과 OB13083에서는 약 50%의 높은 발병율이 관찰되었다.
Table 3.
Investigation of the incidence of viral diseases in the early growth stage using the cultivars, lines, symptoms, and detected viruses of soybean.a,b
aIn June 2020, soybeans were collected 3–4 weeks after seeding in the breeding field of Department of Southern Area Crop Science, National Institute of Crop Science.
bInfecting virus was confirmed via RT-PCR and metatranscriptome analysis; RT-PCR targeted the following 11 species of viruses; Alfalfa mosaic virus (AMV), Bean common mosaic virus (BCMV), Clover yellow vein virus (ClYVV), Cucumber mosaic virus (CMV), Peanut mottle virus (PeMoV), Peanut stunt virus (PSV), Soybean dwarf virus (SbDV), Soybean mosaic virus (SMV), Soybean yellow common mosaic virus (SYCMV), Soybean yellow mottle mosaic virus (SYMMV), and Tomato spotted wilt virus (TSWV).
콩 생육초기 감염 바이러스의 RT-PCR 진단
채집한 시료 83점을 국내 콩에서 보고된 바이러스 11종(AMV, BCMV, ClYVV, CMV, PeMoV, PSV, SbDV, SMV, SYCMV, SYMMV, TSWV)에 대하여 다중 RT-PCR 진단을 실시하였다(Table 2). 그 결과, 진단대상 11종 바이러스 중에서 4종(SYMMV, SMV, SYCMV, PSV)이 검출되었고, 7종(AMV, BCMV, ClYVV, CMV, PeMoV, SbDV, TSWV)의 바이러스는 검출되지 않았다(Table 3). 전체 채집시료 83점 중에서 53점(63.9%)의 시료에서 바이러스가 검출되었으며, 30점(36.1%)의 시료에서는 바이러스가 검출되지 않았다(Table 3). 감염된 시료 53점에서는 SYMMV와 SMV가 복합감염된 1점의 시료를 제외하면, 모두 단독감염되어 있었다. 세부적으로 검출된 바이러스 4종의 검출율을 보면, SYMMV와 SMV는 각각 29점(54.7%)과 23점(43.4%)의 시료에서, SYCMV와 PSV는 각각 1점(1.9%)의 시료에서 검출되었다. 따라서, 콩 생육초기에 발생하는 주요 바이러스는 SYMMV와 SMV로 확인되었다.
콩 육종포장에서 생육초기 검출된 바이러스는 품종포와 계통포에 따라 뚜렷한 차이를 나타내었다(Table 3). 품종포에서는 SYMMV 1종의 바이러스만 검출되었다. SYMMV는 채집된 10개 품종 중에서 4개(청자5호, 미풍, 녹원, 선유2호) 품종에서 검출되었으며, 6개(장단백목, 부석, 태양콩, 두루울, 풍산나물콩, 태광콩) 품종에서는 검출되지 않았다. 특히 청자5호 품종은 채집시기에 약 30%의 발병율을 나타내었으며, 채집한 시료 17점 모두에서 SYMMV가 검출되었다. 그리고 미풍 품종은 약 10% 정도의 발병율을 나타내었으며, 6점의 채집시료 중 5점의 시료에서 SYMMV가 검출되었다. 녹원과 선유2호 품종은 각각 2점씩 채집되었고, 각각 1점의 시료에서 SYMMV가 검출되었다.
F2 및 F3 계통포에서는 4종(SMV, SYMMV, SYCMV, PSV)의 바이러스가 검출되었다(Table 3). 계통포에서 바이러스가 검출된 29점의 시료 중에서는 SMV가 23점(79.3%), SYMMV 5점(17.2%), SYCMV 1점(3.4%), PSV 1점(3.4%)이었다. 품종포에서는 SYMMV만 검출되었으나, 계통포에서는 SMV가 가장 많이 검출되었다. 이러한 결과로 볼 때, 콩 생육초기 바이러스병은 품종포에 비하여 계통포에서 훨씬 다양성이 높은 것으로 조사되었다. 특히 SMV는 채집시 약 50%의 높은 발병율을 보인 OB13083와 OB13086에서 채집한 시료 각각 6점에서 모두 검출되었다. 또한 SMV는 11개의 계통포 라인에서 검출되었다. 계통포에서 SYMMV는 인접하지 않은 5개의 라인에서 무작위하게 검출되어, 품종포에서의 발생양상과는 구별되었다.
콩 생육초기 바이러스병 증상을 보인 채집시료 83점을 11종 바이러스에 대하여 multiplex RT-PCR 진단한 결과, 30점(36.1%)의 시료에서는 바이러스가 검출되지 않았다. 11종 바이러스에 대한 multiplex RT-PCR 진단에서 음성으로 나타난 시료는 품종포에서 33.3% (12/36점), 계통포에서 38.2% (18/47점)로 특별한 차이를 나타내지 않았다. 따라서 이러한 시료는 생리장해 또는 진단대상 바이러스 이외의 병원체의 감염이 원인일 수 있을 것으로 판단되어, NGS를 이용한 메타전사체 분석을 실시하였다.
메타전사체 분석을 통하여 탐색된 식물바이러스
RT-PCR 진단대상 바이러스 이외의 추가적인 바이러스의 탐색과 RT-PCR 음성반응 시료를 검증하기 위하여 메타전사체 분석을 수행하였다. 이를 위하여 콩 생육초기 시료 83점을 전체화(pooling) 한 다음 NGS 분석을 수행하여 약 40 Gbp의 데이터를 생산하였다. 생산된 데이터를 Trinity software를 이용하여 119,866개의 컨티그로 de novo 조립하였다. 조립된 컨티그는 생물정보 데이터베이스를 기반으로 어노테이션 과정을 수행하였다. 어노테이션 결과, 6,124개 컨티그가 바이러스와 관련된 것으로 분석되었다. 분석된 6,124개의 컨티그를 NCBI BLASTn·BLASTx search를 이용하여 재검증하였으며, 최종적으로 12개의 컨티그가 식물바이러스 5종(SYMMV, SMV, SYCMV, PSV, SGVA)과 관련된 것으로 확인되었다(Fig. 1). RT-PCR 진단을 통하여 검출된 4종 바이러스(SYMMV, SMV, SYCMV, PSV)는 메타전사체 분석에서도 모두 검출되었다. 또한, RT-PCR 진단에서 검출되지 않은 7종 바이러스(AMV, BCMV, ClYVV, CMV, PeMoV, SbDV, TSWV)는 메타전사체 분석에서도 관련된 컨티그가 검출되지 않았다. 따라서 본 연구에서 83점의 시료에 대한 RT-PCR 진단과 메타전사체 분석의 결과로 판단할 때, 콩 생육초기 발생하는 바이러스를 효과적으로 검출하였다고 판단된다.
한편, 메타전사체 분석을 통하여 RT-PCR 진단대상에 포함되지 않은 신종 바이러스, SGVA의 컨티그가 검출되었다. SGVA의 존재를 확인하기 위하여 메타전사체 분석으로 검출된 컨티그 서열을 기반으로 프라이머를 설계하고 RT-PCR 진단을 수행하였다. 그 결과, 1점의 시료에서 SGVA가 검출되었다. RT-PCR 반응 산물의 염기서열을 분석하여 925 bp의 염기서열을 확인하였다. 925 bp의 염기서열을 NCBI BLASTn 분석한 결과, 콩에서 검출된 SGVA(GenBank MH428829)와 99.78%의 상동성을 나타내었다.
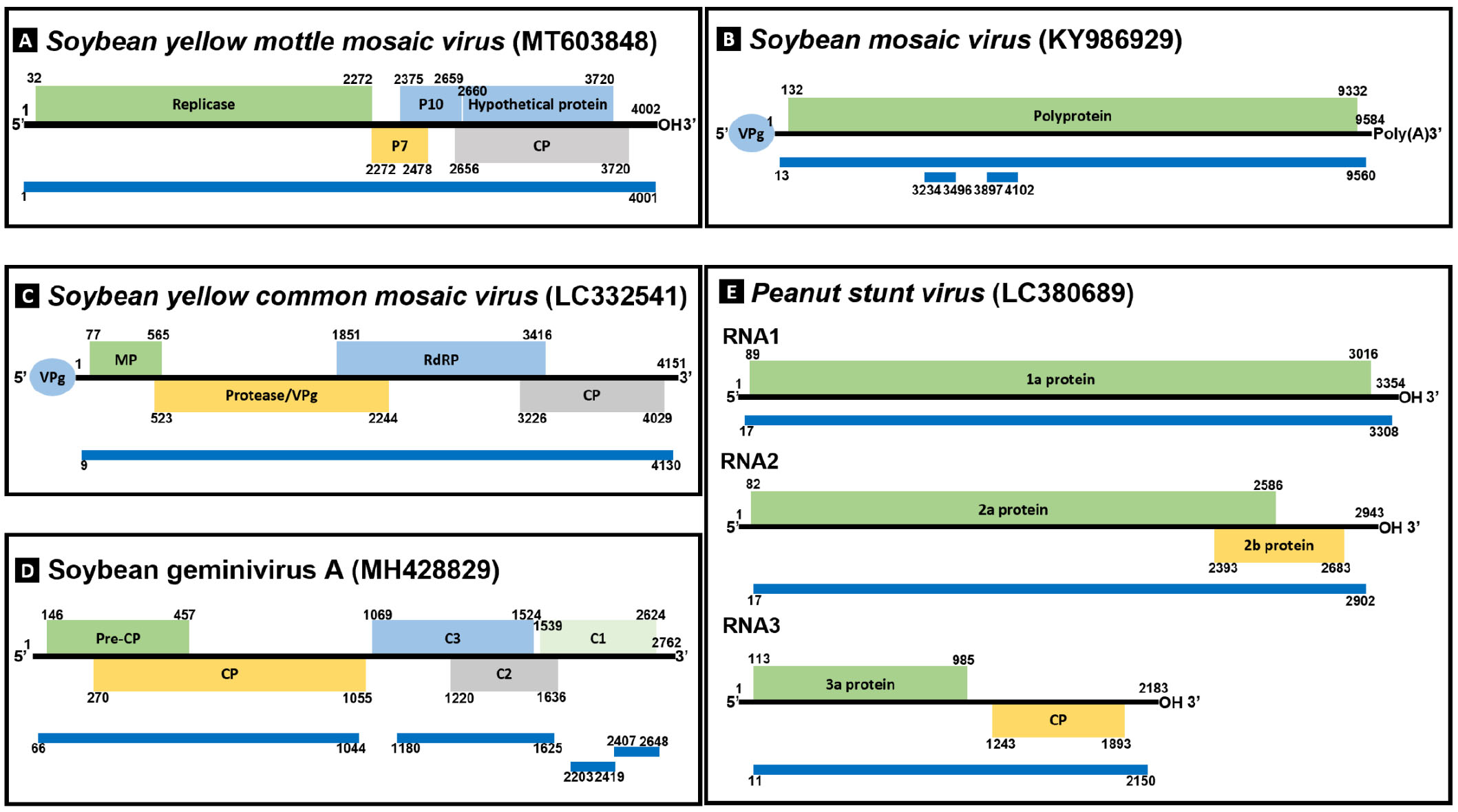
Fig. 1.
Genomic structure of the plant viruses and location of plant virus-associated contigs detected through metatranscriptome analysis. The blue bars indicate detected contigs and are located in relative positions to the reference genome. The reference genome used the sequence with the highest similarity in BLASTn analysis. A: Soybean yellow mottle mosaic virus (GenBank : MT603848), B: Soybean mosaic virus (KY986929), C: Soybean yellow common mosaic virus (LC332541), D: Soybean geminivirus A (MH428829), E: Peanut stunt virus (LC380689).
최종적으로 RT-PCR 진단과 메타전사체 분석을 통하여 콩 생육초기 포장에서 채집된 83점의 시료로부터 5종의 바이러스(SYMMV, SMV, SYCMV, PSV, SGVA)를 검출하였다. 채집 시료 83점 중에서 54점(65.1%)이 바이러스에 감염된 것으로 확인되었다(Fig. 2). 세부적으로 SYMMV (53.7%, 29/54점)와 SMV (42.6%, 23/54점)가 높은 비율로 검출되었으며, SYCMV, PSV, SGVA는 각각 1점(1.9%)의 시료에서 검출되었다.
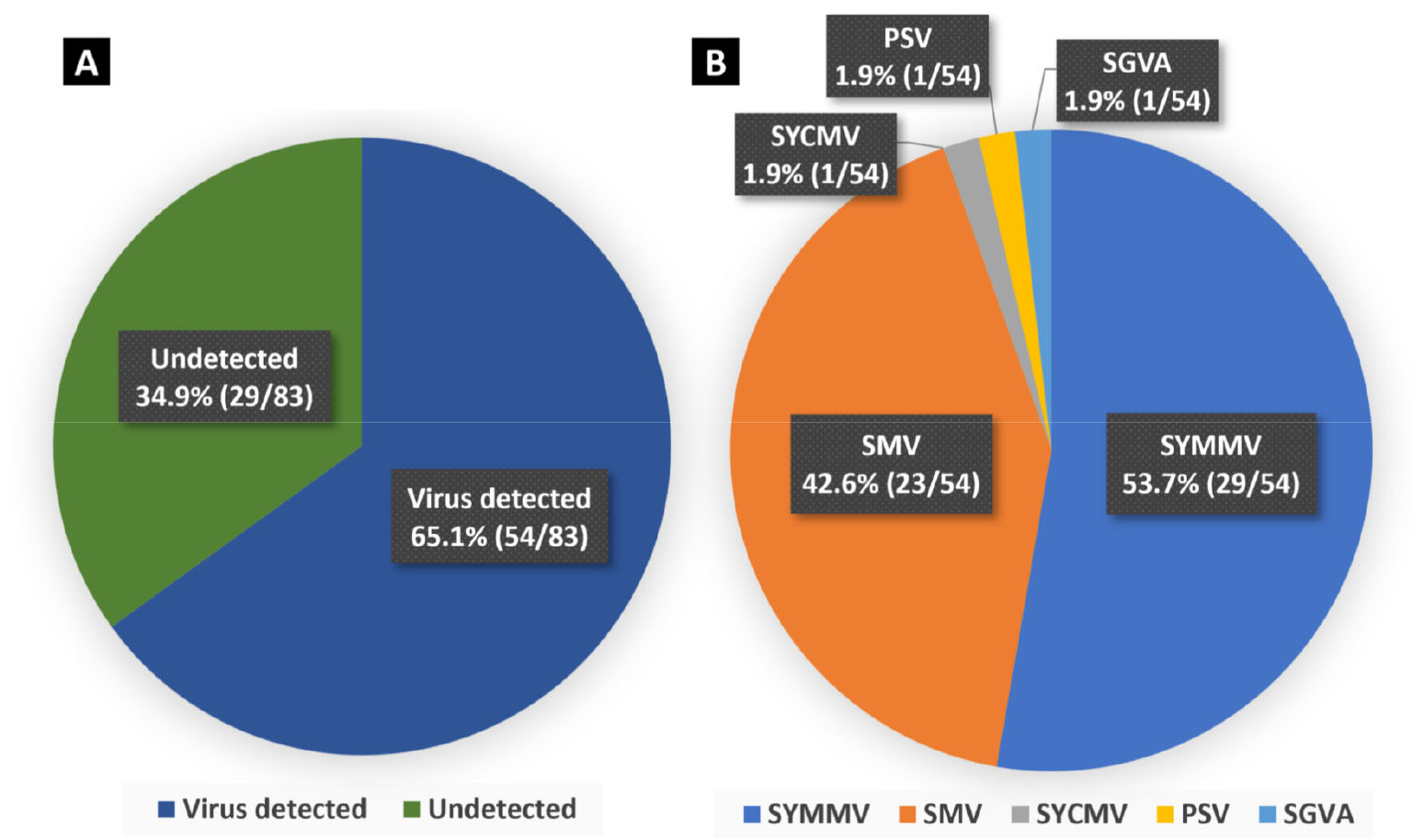
Fig. 2.
The proportion of viruses detected in soybean in the early growth stage. Virus detection was confirmed via RT-PCR and metatranscriptome analysis. (A) the sample ratio of detected and undetected viruses; and (B) individual virus proportion in the infected samples. Coinfection of Soybean yellow mottle mosaic virus and Soybean mosaic virus was confirmed in one sample.
콩 생육초기 감염 바이러스에 따른 병징
생육초기 채집된 콩 시료를 RT-PCR 및 메타전사체 분석으로 바이러스를 진단한 결과 감염 바이러스에 따라 병징의 차이를 나타내었다. 콩 생육초기 주로 관찰되는 바이러스 병징은 모자이크 증상이었으며, 그 이외에 황화, 퇴록반점, 위축, 얼룩(mottle) 등도 함께 관찰되었다. SYMMV 감염 콩은 대부분 잎에 뚜렷한 모자이크 병징을 나타내었으며(Fig. 3. A-C), 콩 생육초기 포장에서 육안으로 쉽게 감염주를 구별할 수 있었다. 반면 SMV는 다양한 병징을 나타내는 시료에서 검출되었다(Fig. 3. D-K). SMV는 계통포의 라인에 따라 유사하거나 구별되는 병징을 나타내었다(Table 3). OB13083와 OB13086 라인에서 검출된 SMV의 병징은 약간의 차이를 보였다. OB13083 라인은 모자이크와 함께 퇴록반점이 관찰되었으며(Fig. 3. D), OB13086 라인은 모자이크와 얼룩 증상이 관찰되었다(Fig. 3. E). 반면, OB13087-1 라인은 뚜렷한 모자이크와 함께 식물체 전체가 위축되고 생육이 불량하였다(Fig. 3. F).
아울러, SYCMV가 감염된 콩(Fig. 3. M)은 골든 모자이크(golden mosaic) 및 얼룩(mottle)이 관찰되었으며, PSV가 감염된 콩(Fig. 3. N)은 생육이 불량하고, 모자이크, 엽맥녹대(vein banding), 괴사반점(necrotic spot)이 관찰되었다. SGVA가 검출된 콩(Fig. 3. O)에서는 황화와 퇴록반점이 관찰되었다.

Fig. 3.
Symptoms in virus-infected soybeans in the early growth stage. Soybeans were collected approximately 3–4 weeks after seeding. Infection with the following five virus species was confirmed via RT-PCR: Soybean yellow mottle mosaic virus (SYMMV), Soybean mosaic virus (SMV), Soybean yellow common mosaic virus (SYCMV), Peanut stunt virus (PSV), and soybean geminivirus A (SGVA). Soybeans infected with SYMMV (A–C) showed distinct mosaic symptoms, whereas those infected with SMV (D–K) showed various symptoms such as mosaic, mottle, stunt, and chlorotic spots. Samples coinfected with SYMMV and SMV (L) were similar to those infected with SYMMV. Soybeans infected with SYCMV (M) exhibited chlorosis and golden mosaic symptoms. PSV (N) infection caused severe symptoms in soybeans, such as mosaic, vein banding, and necrotic spots, whereas soybeans infected with SGVA (O) showed chlorotic spots.
한편, 콩 생육초기 발생하는 모든 바이러스병의 채집을 위하여 다양한 이상증상을 채집하였다. RT-PCR 진단과 메타전사체 분석으로 29점(34.9%)의 시료는 바이러스가 감염되지 않은 것으로 확인되었다. 이 시료들은 퇴록반점, 황화, 잎 기형, 엽맥녹대 및 괴사 등의 이상 증상이 관찰되지만(Fig. 4), 전형적인 바이러스 병징과는 구별되었다. 이러한 이상 증상은 다양한 요인에 의한 생리장해로 판단된다.

Fig. 4.
Various abnormal symptoms observed in the early growth stages of soybean. No virus was detected in the samples via RT-PCR and metatranscriptome analysis; therefore, abnormal symptoms were presumably caused by physiological disorders and insects. (A and B) chlorotic spots; (C) yellowing, distortion, and malformation; (D–F) yellowing; (G–I) distortion and malformation; (J and K) vein banding and vein necrosis; and (L) chlorosis and yellow spots.
고 찰
본 연구는 콩 생육초기 포장에서 발생하는 모든 바이러스병을 확인하기 위하여 다양한 이상증상을 나타내는 콩 시료를 대상으로 수행되었다. 이에 따라 채집된 콩 시료 83점은 전형적인 바이러스 병징을 나타내는 시료만 아니라 다양한 이상증상을 나타내는 생리장해도 함께 채집하였다. 감염된 바이러스는 12종 바이러스에 대한 RT-PCR 진단과 전체 시료에 대한 메타전사체 분석을 통하여 분석하였으며, 그 결과 콩 시료 54점(65.1%)에서 바이러스가 검출되었다. 바이러스병 이외의 요인으로 판단되는 콩 시료는 29점(34.9%)이며, 바이러스가 검출된 시료와는 병징으로 구별이 가능하였다. 따라서 채집된 콩 시료는 생육초기에 발생하는 바이러스병을 조사하기에 충분한 양의 시료가 분석되었다고 판단된다. 세부적으로 바이러스는 RT-PCR 진단과 메타전사체 분석을 통하여 각각 4종(SYMMV, SMV, SYCMV, PSV)과 5종(SYMMV, SMV, SYCMV, PSV, SGVA)이 검출되었다. 메타전사체 분석에서는 RT-PCR 진단을 통하여 검출된 4종이 모두 확인되었으며, 추가로 신종으로 동정된 SGVA를 검출하였다. 한편, RT-PCR 진단에서 SYCMV, PSV, SGVA는 1점의 시료에서 검출되었음에도 전체 시료에 대한 메타전사체 분석에서도 효과적으로 검출되었다. 이러한 사항들을 종합하면, 본 연구에서 사용한 바이러스 시료 채집 방법과 두 가지 병원체 진단 방법은 콩 생육초기에 발생하는 모든 바이러스병을 효과적으로 탐색하고 검출한 것으로 판단된다.
과거 우리나라의 콩 바이러스병 연구는 종자전염과 충매전염으로 큰 경제적 피해를 일으키는 SMV를 중심으로 수행되었다(Cho, 1981, 1995; Cho & Chung, 1976; Cho & Goodman, 1982; Cho et al., 1984). SMV의 피해를 감소시키기 위하여 국가기관에서 저항성 품종 육종과 보급사업을 지속적으로 추진하였으며, 콩 재식용 종자생산과 관련하여 포장검사 및 종자검사의 검사기준에 포함하여 관리되고 되었다(「종자산업법 시행규칙」 제17조 제1항; 종자관리요강, 제12조). 이에 따라 SMV의 발생은 현저히 감소되었으나, 콩 포장에서 바이러스병의 발생은 여전히 계속되고 있다. 최근 몇 차례 조사에서 우리나라 콩 포장에는 SMV와 더불어 SYMMV, SYCMV가 널리 분포하고 있으며(Lee et al., 2012; Nam et al., 2009; Seo et al., 2014), 소면적 자가채종 농가에는 이른 시기부터 SMV와 SYMMV가 발생하는 것으로 알려졌다(Cho et al., 2013). 본 연구에서도 SYMMV와 SMV는 검출율을 각각 53.7%, 42.6%로 나타내어 콩 생육초기에 발생하는 주요 바이러스로 확인되었으며, SYMMV가 SMV보다 검출율이 높게 나타났다. 따라서, 콩 바이러스병 관리대책에는 SMV뿐만 아니라 SYMMV를 방제하기 위한 국가 차원의 체계적 정책 추진이 필요할 것으로 판단된다.
콩에서 SMV는 종자전염성 바이러스로 알려져 있으며, 본 연구에서도 생육초기부터 많은 발생을 보이는 것으로 판단할 때 국립식량과학원 육종포장도 종자전염이 주요한 발생 경로로 판단된다. OB13083 및 OB13086 라인은 바이러스병의 육안조사에서 발병율이 50% 이상으로 나타났으며, 이 라인들에서 채집한 각각 6점의 시료는 모두 SMV 감염으로 확인되었다(Table 3). 이 두 라인에서 확인된 SMV 분리주는 효과적으로 종자전염이 일어나는 것으로 추정된다.
본 연구에서 생육초기 가장 높은 검출율을 나타낸 SYMMV는 콩에서 종자전염이 지금까지 알려지지 않았다. 그러나 콩의 야생종인 돌콩과 콩과 작물인 녹두, 강낭콩에서 종자전염이 보고되어 있는 것으로 볼 때(Lee & Kim, 2013; Sandra et al., 2020), SYMMV 분리주 특성에 따라 콩에서 종자전염이 가능할 것으로 판단된다. 본 조사에서 콩 생육초기부터 SYMMV가 가장 높은 검출율을 나타낸다는 점을 고려할 때, 이들 분리주에 대한 종자전염 여부에 관한 추가적인 연구가 필요할 것으로 판단된다. 한편, SYMMV의 발생은 매개충을 통한 중간기주로부터의 감염이 주요한 경로일 가능성이 있다. Lee & Kim (2013)의 연구에 따르면, SYMMV는 콩 포장 주변에 널리 분포하는 콩과 식물(돌콩, 새팥, 토끼풀, 비수리 등)에서 검출되었으며, 돌콩에서는 효과적으로 종자전염되는 것으로 보고되었다. 돌콩은 우리나라 전역에서 널리 자생하고 있으며, 이른 생육기로 인하여 SYMMV가 콩 보다 이른 시기에 발생한다. 이러한 특성으로 볼 때, 콩 생육초기 SYMMV의 많은 발생은 돌콩과 같은 중간기주로부터의 충매전염이 영향을 미쳤을 것으로 판단된다.
콩 생육초기 SYMMV의 다발생 원인으로는 종자전염 및 충매전염과 함께 토양전염도 고려될 수 있다. 기존 연구에 따르면 SYMMV의 토양전염율은 감염성 즙액과 식물체 잔재물을 처리한 토양에서 26.7-100.0%로 나타났다(Lee, 2009). 이 연구에서 토양전염은 멸균 처리된 토양을 사용하여 토양 미생물이나 선충과 같은 매개체의 영향은 배제할 수 있다. 따라서 토양전염은 토양 내 축적된 바이러스 입자와 콩 사이의 상호작용 결과로 판단된다. 이 연구 결과를 볼 때, SYMMV는 조건에 따라 효과적으로 토양전염될 수 있는 것으로 판단되며, 콩을 연작할 경우 토양 내 SYMMV의 입자가 축적된다면 실제 포장에서도 SYMMV의 다발생에 영향을 미칠 것으로 판단된다. 본 연구가 수행된 국립식량과학원 육종포장은 오랫동안 콩이 연작되었으며, 품종포에서 청자5호와 미풍이 각각 30% 및 10%의 발병율을 나타낸 것으로 볼 때, SYMMV의 토양전염도 원인으로 지목될 수 있을 것이다.
본 연구에서 검출된 SGVA는 Geminiviridae에 속하는 DNA 바이러스로, 생물학적 특성은 구명되지 않은 신종이다. Geminiviridae는 기주범위가 매우 넓으며, 일반적으로 가루이류, 진딧물류, 매미충류에 의하여 전염된다(Fiallo-Olivé et al., 2021). 아직 SGVA에 대한 구체적인 특성은 구명되지 않았으나, Geminiviridae의 고위험 병원체인 Tomato yellow leaf curl virus (TYLCV)를 보면, 2008년에 우리나라 토마토에서 처음 발생한 후 토마토 등 다양한 작물과 잡초에서 심각한 피해를 일으키고 있으며(Kim et al., 2012), 최근에는 콩에서 종자전염도 보고되었다(Kil et al., 2017; Lee et al., 2010). 본 연구에서 SGVA가 콩 생육초기 시료에서 검출된 점으로 볼 때, 종자전염의 가능성도 있을 것으로 판단된다. 또한, Geminiviridae의 주요 매개충인 가루이류와 진딧물류는 콩 재배지에서 흔히 발견되는 해충이며, SGVA의 주요 매개충이 될 수 있을 것으로 판단된다. 따라서, SGVA가 콩 생육초기 이후 얼마나 어떻게 확산되는지 그리고 콩에 어떤 영향을 미치고 있는지에 관한 연구가 신속히 수행되어야 할 것이다.
적 요
본 연구는 콩 바이러스병 관리대책 수립을 위하여 생육초기에 발생하는 바이러스병의 감염실태를 조사하였다. 국립식량과학원 육종포장에서 파종 후 약 3-4주 된 콩 이상증상 시료 83점을 채집하였다. 채집한 시료의 감염 바이러스 진단은 12종 바이러스의 RT-PCR 진단과 전체 시료에 대한 메타전사체 분석을 통하여 수행하였다.
1. 포장에서 바이러스병 발병율은 전체적으로 1% 미만으로 조사되었으며 일부 품종 및 라인에서는 최대 50%까지 나타내었다.
2. RT-PCR 진단과 메타전사체 분석 결과 SYMMV, SMV, SYCMV, PSV, SGVA가 검출되었다.
3. 검출된 바이러스 중에서 SYMMV와 SMV는 각각 검출율이 53.7%, 42.6%로 나타내어 콩 생육초기에 발생하는 주요 바이러스로 확인되었다.
4. SYMMV에 감염된 콩은 전형적인 모자이크 증상을 나타내었으며, SMV에 감염된 콩은 모자이크, 얼룩, 위축, 퇴록반점과 같이 다양한 증상을 나타내었다.
5. 바이러스 전염 특성을 고려할 때 SMV는 주로 종자전염을 통하여 발생한 것으로 판단되며, SYMMV는 종자전염과 함께 충매전염 및 토양전염의 가능성이 복합적으로 고려되어야 할 것으로 판단된다.
6. SGVA는 본 연구를 통하여 콩 생육초기 포장에서 검출되었으며, 생육초기 이후 발생실태 및 콩에 미치는 영향에 관한 연구가 신속히 수행되어야 할 것이다.




