옥수수(Zea mays L.)는 세계 3대 주요 작물의 하나로 우리 나라뿐만 아니라 전 세계에서 식용, 사료용, 공업용, 의약품 용 등 다양한 용도로 사용되고 있다. 최근에는 저탄소 및 친 환경 시대를 위한 바이오 에너지로 옥수수 전분을 이용하여 에탄올 생산에 활용되고 있다(Vohra et al., 2014). Ganal et al. (2011)은 SNP genotyping array를 위하여 800,000만 개 이상의 SNP marker를 이용하였으며, 이러한 data를 기반으로 maize germplasm genotyping과 high density linkage mapping 을 분석하였다. 이들은 array의 high quality를 고려해 봤을 때, large genotyping array는 옥수수 육종 연구에 응용 및 가치가 있을 것으로 예상하고 있다. 최근 nested association mapping (NAM) population을 이용한 분자 육종 연구가 활 발하게 진행되고 있다. NAM population은 총 25개의 교잡 종 집단으로 B73 계통을 공유하고 있으며, 특히 B73은 이 미 유전자 배열의 해독이 끝났고 옥수수 육종에서 농업적으 로 가치 있는 자식 계통이다. McMullen et al. (2009)은 이 러한 NAM 집단을 활용하여 single nucleotide polymorphism (SNP) marker와 새로운 genotype 집단을 mapping하여 NAM population을 발굴하였으며, 이를 이용한 NAM 유전자 지도 를 만들었다. 또한 Yu et al. (2008)의 연구에서는 SNP data, common-parent-specific (CPS) marker, quantitative trait loci (QTL) mapping을 이용하여 컴퓨터 시뮬레이션을 시도하였다.
최근에는 지구온난화로 인한 기후 변화로 봄철 가뭄이 빈 번하게 관측되고 있다. 봄철 가뭄은 봄에 파종하는 작물들 의 생육에 심각한 피해를 주고, 수량을 상당히 감소키는 요 인으로 작용한다(Lee et al., 2013). 최근 우리나라의 봄철 기후(4월~6월)도 대륙성 고기압의 영향을 받아 강한 일사와 고온현상이 자주 발생되고 있다(기상청, 기상연보 2013). 이 와 같은 기후변화로 봄철에도 가뭄이 증가하고 있으며, 유 묘기의 작물들이 한발 피해를 받아 정상 생육이 어렵게 되 었다. 특히 옥수수는 다른 작물과 비교하여 잎이 넓고 키가 큰 작물로서 많은 물을 필요로 하며, 가뭄에는 강하지 않는 편이다. 가뭄이 심하면 생육이 저해되고, 유수형성기 이후 에 한발 피해를 받으면 암이삭이 나오는 시기가 수꽃이 나 오는 시기보다 많이 늦어져 수분이 어렵고 불임이삭이 발생 한다. 또한 등숙기간에 한발 피해를 받으면 옥수수 수량이 현저히 감소하여 상품가치가 떨어지게 된다. 따라서 옥수수 생육에 알맞은 토양수분은 최대용수량 60~80% 정도가 적 절하며, 이러한 환경을 유지하기 위해서는 월 평균 90~120 mm의 비가 내려야 한다. Eom et al. (2013)은 우리나라의 최근 30년간 45개 지역에서 기후변화에 따른 옥수수 전 생 육기간의 물 요구량을 산정하였다. 그 결과 하루 평균 물 요 구량은 3.27 mm day-1이었으며, 생육단계별로 초기에는 평균 2.02 mm day-1, 신장기에는 3.41 mm day-1, 생육중기에는 4.41 mm day-1, 생육후기에는 3.48 mm day-1, 생육말기에 는 3.01 mm day-1이었다.
가뭄으로 인한 한발 스트레스는 옥수수의 기관발달을 저 해하며, 잎과 수염 생장이 크게 감소한다. 잎 발달 장애는 잎 면적의 감소로 이어지고, 기공이 닫혀 잎의 온도가 높아 지면서 광합성 효율이 떨어지게 된다(Aslam, 2011). Herrero & Johnson (1981)은 수꽃의 개화유도를 위해 온도 별로 2 7°C, 32°C, 38°C(고온) 등의 스트레스를 처리하여 꽃가루 발아율을 평가하였다. 대부분의 옥수수 품종은 32°C이상에 서 꽃가루 발아율이 거의 zero수준으로 감소하였고, 38°C에 서는 모든 품종들에서 낮은 발아율을 보이거나 발아를 하지 않았다. 이것은 고온의 스트레스로 인해 옥수수 수꽃의 발 달을 저해시키는 요인으로 적용되었음을 보여준다. 옥수수 한발 내성에 대한 관심은 주로 옥수수 수염발달, anthesissilking interval (ASI) 및 종실 성숙에 대하여 한발 스트레스 가 미치는 영향을 집중하여 연구되었다(Bolaños & Edmeades, 1996). ASI는 한발이 옥수수의 종실이 맺히는 과정의 연관 성을 확인할 수 있는 지표로서, 전통적으로 옥수수 한발 관 련 연구에 널리 사용되어왔다. ASI의 중요성은 수꽃과 암 꽃의 개화기의 차이를 보는 것으로, 특히 한발 환경에서는 수꽃과 암꽃의 개화기의 차이가 벌어지는 것으로 알려져 있 다(Robins & Domingo, 1953; NeSmith & Ritchie, 1992). 하지만 ASI 등의 기존 지표는 개화기 옥수수에 대한 한발 측정 지표이며, 많은 시간과 노동력이 필요하다는 단점이 있다. 현재까지 옥수수 유묘기에 한발이 미치는 영향에 대한 연구로는 유전자원에 따른 한발 내성 평가(Maiti et al., 1996; Liu et al., 2003; Meeks et al., 2013), 한발이 antioxidant system에 미치는 영향(Li et al., 1998; Bai et al., 2006), 한발 스트레스를 줄이기 위하여 생장조절제의 처리 효과 (Zamaninejad et al., 2013; Seo et al., 2014), 한발에 의한 옥수수 유묘기의 뿌리 발달(Bilgin et al., 2008; Trachsel et al., 2010), 그리고 유묘기 한발 피해와 수량성과의 상관관 계(Grzesiak et al., 2012) 등이 있다. 최근에는 isozyme electrophoresis system을 이용하여 peroxidase isozyme과 polyphenol oxidase isozyme을 옥수수 한발 내성 marker로 사용하여 전 기영동상에서 band pattern의 차이를 비교하였다(El-Mouhamady & El-Seidy, 2014). 현재 국내에서는 옥수수 한발평가에 대 한 기준이 ASI에 국한되어 있으며, 유묘기의 한발 내성 평 가는 거의 이루어지지 않고 있다.
본 연구는 유묘기 한발 내성에 대한 지표를 설정하기 위 하여 평가를 수행하였으며, 개화기 한발 평가 지표인 ASI와 비교하여 옥수수 한발 내성 기초자료를 제공하고자 한다.
재료 및 방법
옥수수 품종
한발 조건에서 옥수수 품종 별 유묘기 잎말림 현상을 측 정하기 위하여 총 19가지 품종을 사용하였다. 옥수수 품종 은 NAM parent line 중 한발 내성에 대한 보고가 되어있는 품종을 우선적으로 선발하였으며, 상대적 비교가 가능하도 록 국내 품종 및 동남아시아 품종을 선발하였다(Table 1).
발아 및 환경
품종 별 종자는 29°C의 Growth chamber에서 36시간 이 상 고습처리하여 발아하였다. 발아 후 60 x 40 x 20.5 cm 화분에 질석(vermiculite) 30 L를 넣고 포장용수량까지 물 을 공급한 후 9 x 11.5 cm의 재식밀도로 파종하였다. 정확 한 비교를 위하여 품종 별 실험구와 대조구을 처리하였다. 대조구는 토양수분함량 15~25%, 25°C에서 16시간 동안 광 조건, 20°C에서 8시간 동안 암조건으로 유지하였으며, 실험 구는 3엽기까지 대조구와 동일한 조건에서 성장 후 3엽기 이후에는 수분을 중단하였다.
토양수분함량
토양수분함량은 WT1000N (Mirae Senser Inc.)제품을 이 용하여 측정하였으며, 세 차례의 측정값을 평균으로 산정하 였다. 기존 연구 결과로 밝혀진 토양수분과 한발 스트레스 의 상관관계를 참고하여 0 ~ -0.5MPa 구간을 정상 토양수 분함량으로, -0.5MPa ~ -1.2MPa 구간을 약한 한발, -1.2MPa ~ -2.0MPa 구간을 심한 한발, -2.0MPa 이하를 극심한 한발 환경으로 산정하였다(Schmidhalter et al., 1998; Sharp et al., 1988; Yamaguchi & Sharp, 2010). 정확한 평가를 위하 여 질석의 토양수분함량과 토양수분포텐셜의 상관관계를 측정하여 토양수분함량 별 옥수수 유묘기 한발 내성을 평가 하였다(Sharp et al., 1990; Batlang, 2006) (Fig. 1).
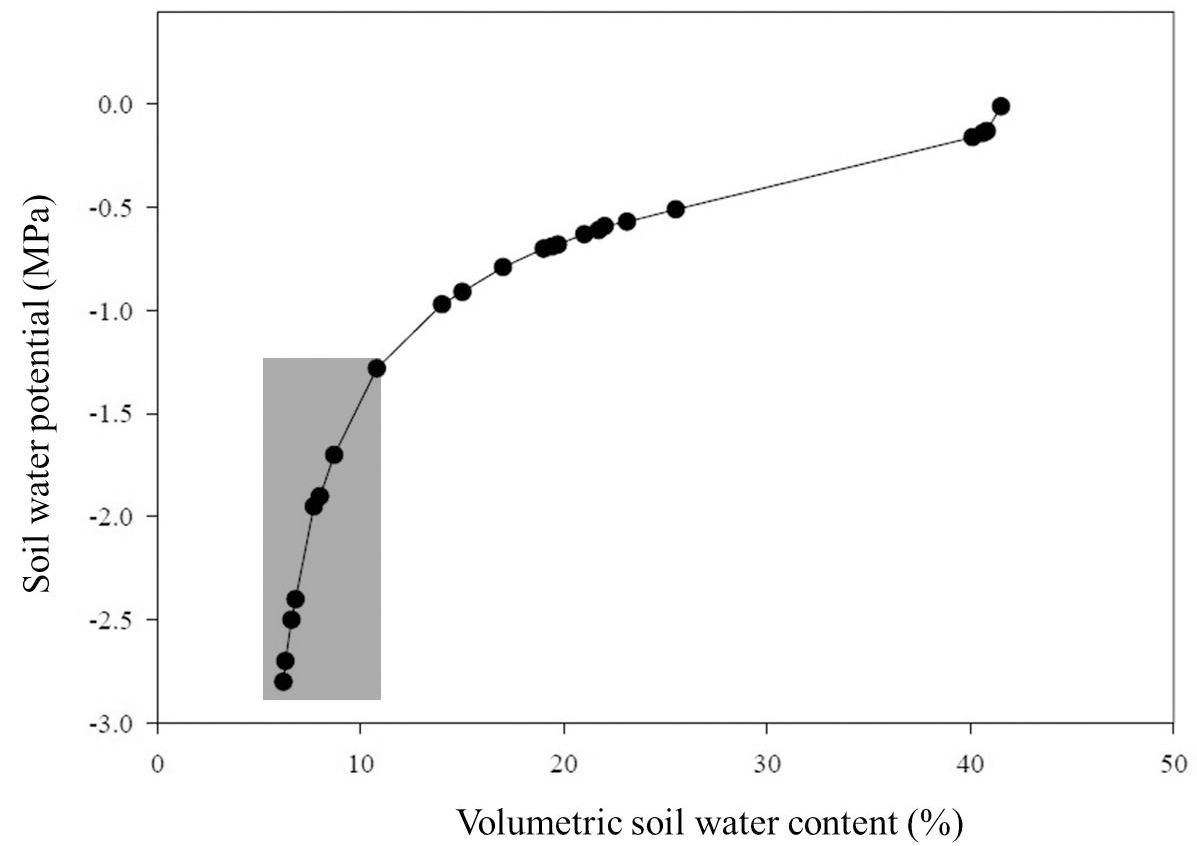
Fig. 1.
Soil volumetric water content on water potential of vermiculite predicted from a moisture release curve by Batlang, 2006.유묘기 한발처리
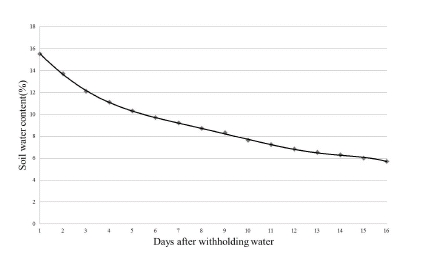
파종 후 3엽이 전개될 때까지 토양수분을 15~25%로 유 지하였으며, 3엽의 전개 후 실험구의 수분공급을 중단하였 다. 수분 공급 중단 후 질석의 토양수분함량은 Fig. 2와 같 다. 수분 공급 중단 후 약 6일 이후에는 약한 한발인 토양수 분함량 10%의 환경이 되었으며, 9일 이후에는 심한 한발인 7%의 토양수분함량을, 최종적으로는 토양수분함량이 5% 에 가까워져 극심한 한발 환경을 보였다.
잎말림 평가
잎말림 현상을 평가하기 위하여 CIMMYT의 잎말림 평 가 기준을 참고하였다(Bänziger et al., 2000). 잎말림은 각 잎별로 측정하였으며, 잎말림 평가 기준은 Fig. 3과 같다. 1 단계는 낮은 징조 혹은 정상상태를 의미하며, 2단계부터 잎 말림 현상을 의미한다. 3단계에서는 잎말림 현상이 심해져 V 형태로 바뀌며, 4단계에서는 잎말림 현상으로 인해 잎 양 쪽이 서로 닿게 된다. 5단계는 양파처럼 잎이 말리게 되고, 6단계에서는 잎이 죽는 것을 기준으로 하였다.
결과 및 고찰
잎말림 현상에 따른 한발 내성 검정
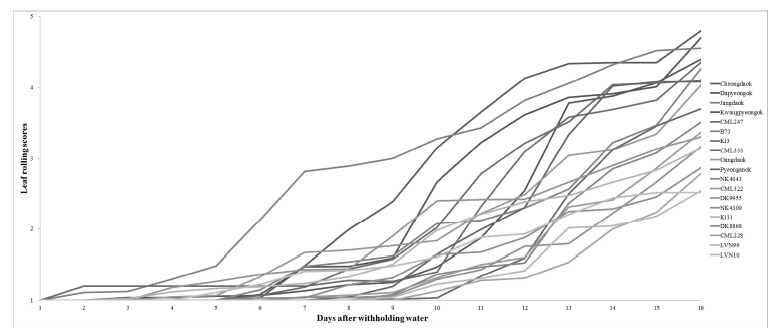
옥수수 종자를 파종하여 싹이 나오는데 걸리는 일수는 품 종간에 차이는 있으나 3엽기까지 성장하는데 대략 15일의 시간이 소요되었다. 유식물체에서 3엽이 활착된 후 수분 공 급을 중단 한 결과, 질석의 수분함유량이 줄어들었으며 이 와 비례하여 잎말림 현상이 관찰되었다. 수분 공급 중단 6 일 이후에는 평균적으로 10%의 토양수분함유량을 보였고, 이것은 약 -1.2 MPa로 약한 한발 스트레스에 해당한다(Fig. 2). 또한 수분 공급 중단 9일 이후에는 평균적으로 토양수 분함량 7% 미만의 심한 한발 스트레스를 보였다. 그리고 14일 이후에는 약 5%의 토양수분함량(-2.0MPa)인 극심한 한발 스트레스가 나타났다(Barker et al., 2005; Lopes et al., 2011). 총 19 품종에 대한 잎말림 현상을 전체적으로 확인하기 위하여 각 개체별 잎말림을 점수로 환산하였으며, Fig. 4와 같은 경향이 나타났다.
한발 스트레스를 처리한 후 약 6일 후에 잎말림을 조사한 결 과, 동남아시아의 상품화된 품종들(LVN10, LVN99, DK8868, DK9955, NK4300, NK4043)은 잎말림 현상이 거의 나타나 지 않았다. 반면에 이 구간에서 국내 품종인 장다옥은 약한 한발 스트레스에 해당되는 잎말림 현상이 관찰되었으며, 이 것을 제외한 대부분의 품종들은 잎말림 현상이 크게 나타나 지 않았다(Hsiao et al., 1984; O’Toole & Cruz, 1980; Praba et al., 2009; Siddique et al., 2000). 그러나 10일 이후에는 거의 모든 품종의 유묘기에서 잎말림 현상이 나타났으며, 이러한 현상은 타작물의 실험결과와 유사하여 -1.5 MPa 이 상의 심한 한발 환경에서는 옥수수 유묘기의 생육에 큰 영 향을 줄 것으로 예상된다(Jones, 2007).
전반적으로 Temperate 기후의 옥수수 보다는 Tropical 기 후의 옥수수가 한발 스트레스를 받았을 때 잎말림 현상이 낮게 나타나는 것을 볼 수 있다. 해외 연구진의 연구결과로 한발 내성이 약하다고 평가되어진 B73 품종의 경우 유묘기 의 한발 내성 또한 높지 않은 것으로 생각된다(Chen et al., 2012; Terbea & Ciocãzanu, 1999; Xu et al., 2014). 마찬가 지로 CIMMYT에서 육성한 Tropical inbred line 중 한발 내 성이 약하다고 평가되어온 Ki3와 CML247 품종 역시 유묘 기 한발 내성이 높지 않은 것으로 생각된다. 반면 CIMMYT 에서 개발된 품종 중 한발 내성이 강한 것으로 보고된 Ki11 품종은 유묘기 한발에서 잎말림이 거의 나타나지 않았다. 현재까지 대다수의 연구에서 옥수수 한발 내성은 ASI에 기 준을 두고 있어 유묘기 한발 내성과 직접적인 비교는 어려 우나, 대체적으로 유묘기의 한발 내성과 ASI를 이용한 한 발 내성의 유사성이 보인다.
한발 스트레스 수준에 따른 잎별 잎말림 현상
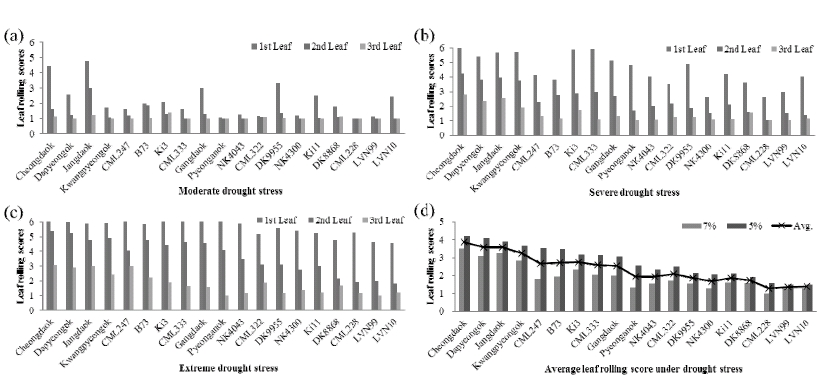
Fig. 4는 수분 공급을 중단한 이후 품종 간 모든 잎의 잎 말림 평균을 그림으로 나타낸 것으로, 직접적인 품종별 한 발 내성의 기준으로 적합하지 않다. 특히 토양수분함량 5% 에 해당하는 한발 내성의 경우 포장에서는 거의 나타나지 않는 극심한 한발 내성임을 고려할 때, 객관적 지표설정을 위해 잎말림 현상을 세분화하여 평가하였다. 따라서 잎별 잎말림 현상을 분석하기 위하여 세 단계로 나누어 잎말림을 측정하였다. 약한 한발 스트레스는 토양수분함량 10%를 기 점으로 하였으며, 심한 한발 스트레스를 토양수분함량 7%, 극심한 한발 스트레스는 토양수분함량 5%로 나누어 각 잎 별 잎말림 현상을 평가하였다(Barker et al., 2005; Lopes et al., 2011). 또한 전체적인 경향을 분석하기 위해 개체 별 잎 말림 현상을 점수화하였다(Fig. 5).
약한 한발 스트레스에서 국내 품종인 장다옥과 청다옥을 제외한 모든 품종에서 2,3엽의 잎말림 현상을 거의 찾아 볼 수 없었다(Fig. 5(a)). 하지만 몇몇 품종에서 약한 한발 스트 레스(10%)에서 첫 번째 잎의 잎말림이 3단계이상에서 관찰 되었다. 한국 품종 중 특히 청다옥과 장다옥은 10%의 약한 한발 스트레스에서도 첫 번째 잎의 잎말림 현상이 높게 나타 나는 것으로 관찰되었다. 그리고 동남아시아 품종인 DK9955 에서도 첫 번째 잎의 잎말림 현상이 국내 품종과 같이 비슷 하게 관찰되었다. NAM parent line 중 한발 내성이 크지 않 은 것으로 알려져 있는 B73과 Ki3는 약한 한발 수준(10%) 에서 2, 3엽의 잎말림 현상이 낮게 나타났다. 반면 장다옥 품종은 약한 한발에서 두 번째 잎이 3단계에 근접한 잎말림 현상을 보였다.
심한 한발 스트레스(7%, -1.5 MPa)에서는 대부분 품종들 의 첫 번째 잎에서 3단계 이상의 잎말림 현상이 나타났다 (Fig. 5(b)). 특히 한국 품종들은 첫 번째 잎에서 상대적으로 높 은 잎말림 현상이 관찰되었다. 동남아시아 품종인 DK9955, Ki3, CML333의 경우 첫 번째 잎에서 높은 잎말림 현상이 나타났으나, 2, 3옆의 잎말림 현상은 낮게 관찰되었다. 한국 품종인 다평옥, 청다옥, 장다옥, 광평옥의 경우 다른 품종들 에 비해 7%의 토양수분함량에서 2, 3엽의 심한 잎말림을 보였다. 대다수의 동남아시아 품종들은 7%의 토양수분함량 에서 2, 3엽기의 잎말림 현상이 2단계를 넘지 않았으나, 한 발 내성이 크지 않다고 보고된 CML333, B73, Ki3의 경우 두 번째 잎에서 잎말림 현상이 상대적으로 높게 나타났다 (Chen et al., 2012; Udomprasert et al., 2005; Voothuluru et al., 2013).
극심한 한발 스트레스인 토양수분함량 5%의 단계(-2.0 MPa)에서는 거의 모든 품종에서 첫 번째 잎의 잎말림 현상 이 5단계 이상 높게 나타났다(Fig. 5(c)). 그러나 동남아시아 품종인 DK8868, LVN10, LVN99의 경우 첫 번째 잎에서 5 단계 이상은 넘지 않았다. 반면 B73과 우리나라 품종인 다 평옥, 강다옥, 장다옥, 광평옥의 경우 두 번째 잎에서 심각 한 잎말림 현상이 나타났다. 첫 번째 잎의 경우 잎의 발달이 적고, 잎의 면적이 적어 추후 성장에 미치는 영향이 낮으나, 두 번째 잎의 잎말림이 심할 경우 생장이 크게 저해될 것으 로 생각된다(Rhoads and Bennett, 1990; Saglam et al., 2014). NAM parent line인 CML247과 우리나라 품종인 다평옥, 청다옥, 장다옥의 경우 세 번째 잎에서 3단계 이상의 잎말 림 현상이 나타났다. 대부분의 품종들은 토양수분함량 5% 의 한발 환경에서도 세 번째 잎에서 낮은 잎말림 현상이 나 타난 것과는 대조적인 결과다. 각각의 엽별 잎말림 현상으 로 유추해 볼 때, 스트레스의 강도가 심해질수록 첫 번째 잎 의 잎말림이 가속화 되는 것으로 보여지며, 한국품종의 경 우 2, 3옆의 잎말림이 토양수분함량 7%에서부터 시작하여 5%에서는 극심한 잎말림을 보였다. 반면 동남아시아 품종 들은 세 번째 잎의 잎말림이 2단계 이상을 보이지 않아 한 국품종에 비하여 토양수분함량 7%이하의 한발 수준에서도 잎말림 현상이 상대적으로 낮게 나타났다.
토양수분함량 10%의 한발 환경은 대다수 품종들에 큰 피 해를 주지 못하는 것을 볼 수 있다. 또한 토양수분함량 7% 의 심한 한발 환경에서 대다수 품종이 첫 번째 잎이 괴사하 는 것을 볼 수 있었다. 따라서 토양수분함량 10%의 잎말림 및 첫 번째 잎의 잎말림 현상은 한발 내성 평가 지표에 적 합하지 않다. Fig. 5(d)는 토양수분함량 10%의 결과 및 첫 번째 잎의 결과를 제외한 그림으로, 토양수분함량 7% 및 5%에서 두 번째, 세 번째 잎의 잎말림 현상을 점수화하였 다. 또한 토양수분함량 7%~5%구간에서의 잎말림 현상의 평균을 표시하였다. 대체적으로 동남아시아 품종들이 이 구 간에서 잎말림 현상이 낮게 나타났으며, 한국품종에서는 강 다옥 및 평안옥이 비교적 잎말림 현상이 낮게 나타났다. 기 존 연구로 한발 내성이 약하다고 알려져 있는 B73 및 Ki3 의 경우 잎말림 현상이 비교적 높게 나타난 것을 보아 유묘 기 한발 내성도 강하지 않은 것으로 볼 수 있다. 반면 한발 저항성이 강한 것으로 알려져 있는 Ki11의 경우 잎말림 현 상이 보이지 않아 유묘기 한발 내성도 강한 것으로 볼 수 있다.
유묘기 잎말림 단계별 회복능력 평가
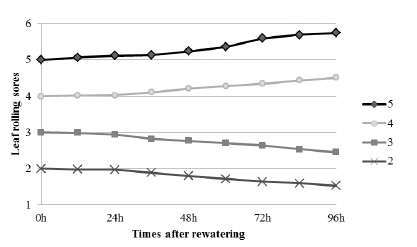
유묘기 옥수수의 한발 내성 평가를 위하여 잎말림 현상의 회복력을 측정하였다. 잎말림 현상은 광합성의 저해를 가져 오는 것으로 알려져 있으며, 수분 공급 시기에 따라 잎말림 현상이 회복되는 것으로 알려져 있다(Humbert et al., 2013). 잎말림 단계별 회복능력 평가를 위하여 수분 재공급 이후 4일 동안 잎말림 현상의 회복을 수치화하였다. 개체 및 품 종별 차이는 있었으나 통계적 유의성은 없었으며, 각 잎말 림 단계별 회복능력에서는 차이가 나타났다(Fig. 6). Fig. 6 는 처리 품종의 평균을 나타낸 것이며 대체적으로 잎말림 5단계가 넘어가는 경우 서서히 잎의 괴사가 진행되었으며, 회복은 불가능 한 것으로 보였다. 잎말림 4단계의 경우 전 체적으로 회복은 되지 않았으나, 괴사 및 변형은 보이지 않 았다. 반면 3단계와 2단계에서 잎말림은 품종 및 엽기에 관 계없이 서서히 회복되는 현상이 나타났다.
잎별 잎말림 현상(Fig. 5) 및 잎말림 회복능력(Fig. 6)을 고려할 때, 두 번째와 세 번째 잎에서 잎말림이 3단계 이상 을 보이는 경우 한발 내성이 낮은 것으로 평가할 수 있다. 대부분의 옥수수 품종에서 첫 번째 잎은 일정 한발 수준에 따라 빠르게 말리는 것을 볼 수 있었으며, 이는 추후 성장에 도움이 되지 않을 것으로 생각된다. 반면, 2, 3엽에서 잎말 림이 3단계를 넘어가지 않으면 유묘기 한발 내성에 높을 것 으로 생각된다.
유묘기 한발 내성 지표의 경우 수정률과 등숙에 직접적인 영향을 확인할 수 있는 ASI와 달리 가시적 비교가 어렵고, 유묘기의 한발 스트레스가 옥수수 수확량에 미치는 영향을 명확하게 밝혀지지 않아 기준 설정에 어려움이 따른다. 이를 극복하기 위해 간접적인 지표인 antioxidant system, ABA의 측정이 이뤄지고 있으나(Li et al., 1998; Zhang et al., 2012), 뚜렷한 기준이 제시되지 않았다. 최근 기후변화로 인한 국 내 봄 가뭄이 반복될 것으로 예상되고 있으나, 이 시기에 해 당하는 유묘기 한발 내성 평가를 위한 지표설정이 이뤄지지 않았다. 봄 가뭄은 유묘기 작물에 한발피해를 입혀 추후 성 장에 저해를 가져올 수 있으므로, 유묘기에 맞는 한발 내성 지표가 필요하다. 다른 작물들과는 달리 옥수수는 토양수분 함량 10%에서는 큰 피해를 입지 않는 것을 볼 수 있었으며, 토양수분함량 7%에서부터 잎말림 현상이 심하게 나타나는 것을 확인하였다. 토양수분함량 별 잎말림 현상 및 수분 재 공급 시 잎말림 회복 결과로 유추한다면, 토양수분함량 5~7% 의 구간에서 두 번째, 세 번째 잎의 잎말림 현상이 3단계를 넘어갈 경우 유묘기 한발 내성이 낮은 것으로 평가할 수 있 다. 상대적으로 이 구간에서 동남아시아 품종 및 한발 내성 이 강하다고 평가된 Ki11은 잎말림 현상의 평균이 2.5이하 로 나타났으므로, 약 2.5 이하의 잎말림 현상을 보일 시 유 묘기 한발 내성이 높다고 볼 수 있다. 본 연구결과는 옥수수 유묘기의 한발 내성을 평가한 기초 자료로서, 개화기의 한 발 내성 평가 지표인 ASI와의 연계, 그리고 유묘기 한발 스 트레스가 생장 및 수확량에 미치는 영향에 대한 연구 등 향 후 유용한 자료로 쓰일 것으로 기대한다.
적 요
본 연구는 국내 및 해외 유전자원을 이용하여 옥수수 유 묘기의 한발 내성 평가를 수행하였다.
약한 한발 환경에서는 장다옥과 청다옥을 제외한 모든 품종에서 2, 3엽의 잎말림 현상을 찾아볼 수 없었다. 장다옥과 청다옥은 첫 번째 잎의 잎말림 현상이 다른 품종에 비해 높게 나타났다. 동남아시아 품종인 DK9955 에서도 첫 번째 잎의 잎말림 현상이 나타났으나, 장다 옥과 청다옥에 비해 낮은 수준이었다.
심한 한발 환경에서는 대부분의 품종들이 첫 번째 잎 에서 3단계 이상의 잎말림 현상을 보였으며, 특히 한 국 품종에서 잎말림 현상이 높게 나타났다. 또한, 동남 아시아 품종 중 DK9955, Ki3, CML333에서도 첫 번째 잎의 잎말림 현상이 높게 나타났다. 2, 3엽에서는 한국 품종인 광평옥, 다평옥, 장다옥, 청다옥 등이 심한 잎말 림을 보였으며, 한발 내성이 약하다고 보고된 Ki3와 B73도 두 번째 잎에서 높은 잎말림 현상이 나타났다.
극심한 한발 환경에서는 모든 품종에서 첫 번째 잎의 잎말림 현상이 높게 나타났다. 대부분의 품종이 세 번 째 잎에서는 잎말림 현상이 없었으나, CML247, 다평 옥, 장다옥, 청다옥의 경우 3단계 이상의 잎말림이 나타 났다. 한발 내성이 강한 것으로 알려져 있는 Ki11과 동 남아시아 품종인 LVN10과 LVN99는 극심한 한발 수 준에서도 상대적으로 낮은 잎말림 현상이 관찰되었다.
잎말림 회복을 측정한 결과, 2단계 및 3단계의 경우 품종과 엽기에 관계없이 회복 가능하였으나, 4단계 이 상의 잎말림 현상이 진행된 경우 회복이 불가하다는 것으로 확인하였다.
종합적으로 토양수분함량 5~7%에서 두 번째와 세 번 째 잎의 잎말림 평균이 2.5이하를 보이는 품종들은 유 묘기 한발 내성이 강한 것으로 보인다.