서 론
토양에서 식물뿌리를 분리하지 않고 분석하는 방법
토양에서 식물뿌리를 분리하여 분석하는 방법
뿌리 이미지 분석용 프로그램
Digital Image of Root Traits (DIRT)
적 요
서 론
작물에서 뿌리는 물리적으로 식물체를 지지하는 역할을 할 뿐만 아니라 토양으로부터 양분과 수분을 흡수하는 중요한 역할을 한다(Kim et al., 2021). 그래서 작물내 양분 및 수분의 흡수 및 이용효율을 높이기 위해 뿌리의 형태적 또는 구조적특성을 분석하기 위한 다양한 노력을 기울이고 있으나, 뿌리가 지상부와는 달리 토양속에 있기 때문에 분석이 어렵고 시간이 많이 들기 때문에 지상부 연구와 비교했을 때 상대적으로 제한된 연구가 수행되고 있는 실정이다(Tripathi et al., 2021; Zhao et al., 2017). 특히, 작물육종분야에서 뿌리는 중요한 형질 중 하나임에도 불구하고 측정에 어려움으로 인해 제한된 뿌리표현형(길이, 무게)을 육종에 이용하거나 또는 지상부의 표현형을 통해 뿌리의 표현형을 간접적으로 예측하는 방식을 활용하였다(Kim et al., 2020; Walter et al., 2015).
최근 영상장비의 해상도가 높아지고, 영상을 분석할 수 있는 다양한 소프트웨어들이 급속히 발달하게 되면서 농업분야에서도 표현형분석에 다양한 이미지 분석 기술이 활용되고 있다(Chung et al., 2020; Water et al., 2015). 특히, 데이터 처리속도의 증가, 인공지능기술의 보급으로 이미지를 통해 획득된 작물의 표현형의 활용범위가 넓어지면서 육종학, 재배학, 및 생리학과 같은 주요 학문분야에 활용되거나 적용을 시도하고 있다(Kim et al., 2019). 이미지를 활용하여 작물의 주요형질을 분석하는 연구를 표현체학(Phenomics)이라고 하며, 작물의 품종개량, 생산량예측, 병해충 피해 진단 및 예측과 같은 분야에 응용되고 있다(Noh & Kim, 2018).
Tripathi et al. (2021)의 보고에 따르면 콩 뿌리의 형태적 및 구조적 특성을 RGB카메라를 통해 획득된 이차원(Two-dimension, 2D) 이미지를 기반으로 분석하였고, Chung et al. (2020)는 RGB카메라를 통해 획득한 콩 뿌리 2D 이미지를 이용하여 뿌리혹의 크기와 수를 U-net 알고리즘을 활용하여 분석하였다. 이처럼 이미지를 이용하여 다양한 작물에서 뿌리의 형태적 및 구조적 특성 분석이 가능함이 보고되면서 국내에서도 뿌리 분석에 대한 관심이 높지만, 분석하고자 하는 연구자들의 연구실 상황과 연구목적에 맞는 방법에 대한 정보를 쉽게 얻을 수 없는 것이 현실이다. 이런 이유에서 본 리뷰에서는 이미지정보를 활용한 뿌리분석 방법들과 이들의 장, 단점을 소개하여 뿌리 분석을 시도하려는 연구자들에게 도움이 되고자 하였다.
토양에서 식물뿌리를 분리하지 않고 분석하는 방법
식물 뿌리의 종적구조는 근관(root cap), 분열대(meristematic zone), 신장대(elongation zone)와 성숙대(maturation zone)로 구성되어 있고, 횡적구조는 표피조직, 기본조직 및 유관속조직으로 구성되어 있다(Wachsman et al., 2015). 식물 뿌리의 표피조직에는 동일세포에서 분화되어 발달한 뿌리털이 있으며, 뿌리털은 토양과의 접촉하는 면적을 확대하여 토양으로부터 수분 및 양분을 흡수하기 용이하게 한다(Ma et al., 2001). 벼에서 뿌리털은 총 흡수된 인(phosphorus)의 63%가량을 흡수하는 것으로 보고하였고, 3개월 자란 밀에서 뿌리털의 면적이 총 뿌리표면적에 60%에 달한다고 보고하였다(Ma et al., 2001; Yamaguchi, 2002). 따라서 식물의 양분 및 수분의 흡수이용효율과 관련된 연구를 진행하기 위해서는 뿌리털에 대한 관찰과 분석이 필요하다. 뿌리털은 뿌리의 표피세포에서 분화된 단일세포이면서 토양입자들과 긴밀하게 밀접하고 있기 때문에 토양에서 식물체를 분리할 경우 대부분의 뿌리털을 소실된다(Kim et al., 2020). 이런 이유에서 대부분의 뿌리털 분석과 관련된 연구는 인공배지 혹은 수경재배 조건에서 진행되어져 왔다(Ma et al., 2001). 그러므로 실제 토양에서 생육중인 작물을 대상으로 뿌리털을 분석할 수 있는 기술이 필요하다.
Field rhizotron 활용
Rhizotron이란 용어는 미국 United States Department of Agriculture (USDA)의 Norther Research Station에 있는 연구자들이 토양내 근권을 좀 더 면밀히 관찰하고자 고안하였다(Busch et al., 2006). 위 방법은 강철 소재의 관을 drilling bit에 결합하여 토양 내에서 일정간격으로 타공한 뒤 투명한 관을 삽입하여 field rhizotron을 조성한 다음 지상부에서 작물을 재배하면서 뿌리의 발달 정도를 투명한 관 속에 카메라를 삽입하여 관찰하는 것이다(Fig. 1A). Rhizotron의 장점은 노지조건에서 실험을 진행할 수 있으므로 여러 작물들의 유전자원들을 대상으로 각각의 자원들간 뿌리의 형태적, 구조적 특성을 분석하는데 용이할 뿐만 아니라 뿌리털 분석도 가능하다는 것이다. 하지만 filed rhizotron 구축과 운용에 많은 비용이 들기 때문에 국가기관에 아니면 장비의 설치 및 운용이 어려운 단점을 가지고 있고, 유압으로 작동하는 기계를 이용해야 하기 때문에 이용에 있어서도 제약이 따른다(Table 1). 또한 rhizotron은 토양에서 한 작물뿌리의 전장을 관측할 수 없기 때문에 투명관을 통해 획득된 뿌리표현형은 실제 작물뿌리에서 일부영역에 지나지 않는다는 것이다. 게다가 작물의 생육초기에는 뿌리의 색이 밝은색(흰색)을 나타내기 때문에 토양과 확연하게 구분되지만 생육후기로 접어들수록 뿌리의 색이 어두운색(토양색과 유사함)을 나타내어 토양과 구분하기 어려운 단점을 가지고 있다(Fig. 1) (Table 1).
Table 1.
Root analysis methods under field conditions.
| Type | Name and description | Pros and Cons | Reference |
| Non-destruction | Field rhizotron • Using a drilling bit, make the hole horizontally, then put the transparent tube into the hole • Small camera push into the established tube, then measure root traits | Pros • Measurement of root trait in field condition • Full lifespan of plant possible • Detection of root hair possible Cons • A small part of the root is visible • The difficulty of separation between root and soil depending on root growth stage • To establish system, a huge amount of money required | Bush et al., 2006 |
| Slanted tube insertion • Using a soil coring machine, make the slant hole, then put the transparent plastic tube into the hole • Small camera push into the established tube, then measure root traits | Pros • Measurement of root trait in field condition • Full lifespan of plant possible • Detection of root hair is possible • Establish-expense is cheaper than rhizotron • Easy to remove plastic tube Cons • A small part of the root is visible • Difficulty of separation between root and soil depending on root growth stage • Insertion of the tube is difficult depending on soil type | Iversen et al., 2011 | |
| Destruction | Mini studio • Using wood panel, set up a mini studio. Back side of the panel replaces with LED lamp to supply backlight. This method can easily collect clear contrast root image • Root samples hang on a clip that is attached to the roof • Small camera place in front of a root, then collect root image | Pros • Cheap and easy to move • Measurement of root trait in field condition • High quality of an image • Detection of root traits everywhere Cons • Measurement of the whole root system is impossible • Disconnection of root particles when root samples take off • Much time is required for separation and wash of root depending on soil type | Chung et al., 2020; Tripathi et al., 2021; Kim et al., 2020 |
| Scanner • After root washing, the root sample place on a transparent plate containing clean water, then capture root image | Pros • High quality of an image • Various types of images can be collected • Maximize in detection of root sample early growth stage Cons • To reduce noise, the overhead light is required • The scanner size is restricted, so the big size of the root can’t measure | Pang et al., 2011 |
Slanted tube insertion 방법
Field rhizotron은 비용적인 문제로 인해 연구실단위에서 시설을 구축하기 어려운 것이 현실이다. 이를 개선하고자 고안한 방법이 slanted tube insertion 방법이다(Iversen et al., 2011). 위 방법은 식물을 파종한 뒤 발아하여 유식물체 단계에 이르렀을 때 식물체 주변에 투명한 플라스틱 관을 비스듬한 방향(약 45°)으로 삽입하여 작물의 뿌리를 관찰하는 방법이다(Fig. 1B). 이 방법은 실험대상작물, 토양조건, 및 실험목적에 따라 삽입하는 투명 플라스틱관의 수를 조절할 수 있어 뿌리의 표현형을 관찰하기에 효과적인 방법이다. 또한 위 방법은 토양관의 비용이 저렴하고, 실험 종료 후 토양으로부터 관을 제거하여 다시 사용할 수 있기 때문에 경제적으로 효과적이다(Table 1). 토양에 플라스틱관을 삽입한 뒤 작물의 생육기간 동안 연구자의 목적에 맞게 일정 주기로 카메라를 토양관 내 일정 깊이로 넣어 뿌리를 관찰할 수 있으며, 위 방법을 통해 토양내에서 깊이에 따른 뿌리의 발달과정을 관찰할 수 있을 뿐만 아니라 뿌리털의 발생량 및 발생패턴 등도 관찰할 수 있다. 반면 slanted tube insertion 방법의 단점은 플라스틱관을 삽입하기 위해서 soil coring machine이 필요하고 토성에 따라 플라스틱관 삽입에 난이도가 발생될 수 있고, rhizotron방법에서 언급한 것과 같이 카메라를 통해 획득된 뿌리 영상정보가 대상작물의 생육시기에 따라 토양과 구분하는데 어려움이 따를 수 있다(Fig. 1C) (Table 1).

Fig. 1.
Root sample collection by a non-destruction method. Fig. 1A and B show field rhizotron and slanted tube insertion, respectively. Fig. 1C reveals the actual root images using both root sample collection methods. As seen in Fig. 1C, the initial white color of the root gradually turns to a dark color, similar to the color of soil. Thus, annotation of root area is more difficult in the late growth stage than in the early growth stage.
토양에서 식물뿌리를 분리하여 분석하는 방법
작물뿌리 연구에서 가장 보편적으로 사용되는 방식이 토양에서 뿌리를 제거한 뒤 물로 세척하여 분석하는 방법으로 이미지분석방법이 보편화되기 전에는 세척된 뿌리를 이용해 뿌리각도 및 측근개수와 같은 형질들을 수작업으로 측정하였다(Trachsel et al., 2010). 그래서 작물뿌리 연구에는 많은 시간과 노동력을 요하는 작업으로 간주되었다(Chung et al., 2020). 하지만 최근 들어 이미지를 분석할 수 있는 다양한 프로그램들이 개발되면서 작물 뿌리의 다양한 형태적 구조적 특성 분석에 이미지의 활용 가능성을 타진하고 있다(Chung et al., 2020; Kim et al., 2020; Tripathi et al., 2021).
Mini studio 활용
Mini studio는 노지조건에서 뿌리 이미지를 촬영하기 위해 고안한 것으로 가로, 세로, 높이가 각각 60 cm가량 되는 나무판(플라스틱도 가능함)을 조립하여 간이 촬영스튜디오를 설치한 뒤 이미지를 촬영하는 방법이다. Mini studio는 가로, 세로가 각각 60 cm가량 되는 정육면체를 생각하면 쉽게 이해할 수 있다(Fig. 1A). 촬영된 이미지의 질을 높이기 위해 뿌리가 촬영되는 뒷면은 나무판 대신 동일한 사이즈의 LED등을 설치하고 맞은편은 오픈하여 카메라를 고정할 수 있도록 설계한다(Fig. 2A). 영상촬영의 대상이 되는 뿌리는 mini studio에 윗면에 고정한 장치에 연결하여 이미지를 촬영하며, 이미지 촬영기간 동안에는 피사체(뿌리) 뒷면에 설치한 LED등을 켜 피사체가 역광이 되도록 유도한다(Fig. 2A). 뿌리를 역광에서 촬영하는 이유는 획득된 뿌리를 분석하기 위해서는 배경과 대조를 이루도록 보정하는 작업이 필요하며 이 작업과정에서 일부 뿌리 영역이 영향을 받게 된다. 하지만 실제 촬영된 영상에서부터 역광조건을 부여하게 되면 영상을 보정하는 과정에서 일어날 수 있는 이미지의 소실현상을 어느 정도 줄일 수 있기 때문에 보다 선명한 이미지를 얻을 수 있다(Fig. 2A). 그리고 뿌리를 보다 쉽게 설치하고 제거하기 위해서는 mini studio 위쪽은 뿌리를 넣고 뺄 수 있도록 문을 제작하는 것이 촬영속도를 높이는데 효과적이다(Fig. 2A). Mini studio의 장점은 분해, 조립이 가능한 방법이기 때문에 장소에 큰 제약 없이 뿌리영상촬영이 가능하며, 뿌리를 역광으로 촬영하기 때문에 선명한 이미지를 획득할 수 있는 장점이 있다. 하지만 토양에서 뿌리를 분리한 뒤 분석하기 때문에 전체 뿌리에 대한 정보를 얻을 수 없으며, 쌍자엽식물의 뿌리를 분석할 경우 주로 큰 뿌리들의 형태적 및 구조적 특성분석에 특화되어 있고, 단자엽식물의 뿌리를 분석할 경우 뿌리들이 서로 겹쳐진 부분이 많으므로 형태적, 구조적 특성분석보다는 전체적인 표면적 분석에 효과적이다(Table 1). 또한, 토성에 따라 작물 뿌리 샘플채취 및 분석에 어려움이 따를 수 있으며, 소실되는 뿌리들이 많이 발생할 수 있으므로 의미 있는 데이터를 생성하기 위해서는 반복수를 늘려야 하는 단점이 있다(Table 1).
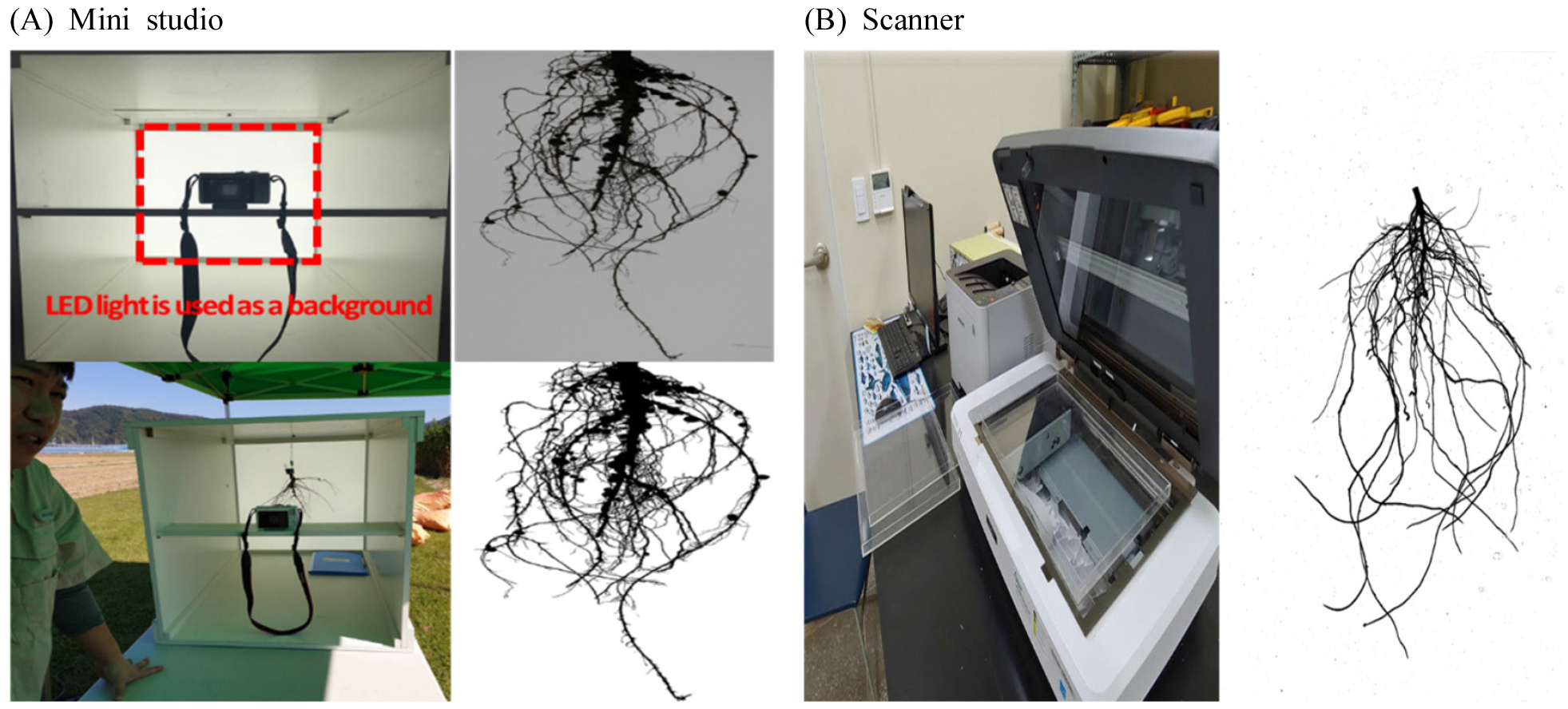
Fig. 2.
Root sample collection by a destructive method. In Fig. 2A, the box with the red dotted line indicates the LED light which is used for the backlight to collect the monochrome image. Fig. 2B shows a scanner for the detection of root phenotype. To collect root images, washed root samples are required. Root images are captured by spreading roots on a transparent acyl plate containing clean water.
스캐너활용
노지에서 뿌리를 수확 후 세척한 다음 뿌리를 스캐너에 넣어 촬영하는 방법으로 노이즈가 없는 깨끗한 이미지를 촬영할 수 있는 것이 가장 큰 장점이다(Kim et al., 2021; Pang et al., 2011). 뿌리를 스캔하기 위해서는 특별한 장치들이 추가적으로 요구되는데 첫 번째는 아크릴로 제작한 투명한 트레이가 필요하다. 투명한 아크릴 트레이에 물을 넣은 후 뿌리를 물위에 뜨게 한 뒤 영상을 촬영하기 때문에 비교적 뿌리의 세세한 부위까지 깨끗하게 촬영이 가능하다. 두 번째는 위쪽과 아래쪽에서 광조사가 가능한 스캐너가 필요하다. 일반적인 스캐너는 아래쪽에서만 빛이 조사되기 때문에 아크릴 트레이에 뿌리를 넣어 촬영하게 되면 뿌리영역 주변에 그늘이 발생하는 노이즈 문제가 있다. 이를 해결하기 위해서는 위쪽에서도 광이 공급되는 스캐너가 필요하다. Espon에서 출시되는 고사양 스캐너 중에는 위쪽과 아래쪽에서 동시에 광이 공급되는 모델이 있어 스캐너를 통한 이미지 정보 획득에 적합하다. 스캐너를 이용한 뿌리 이미지 측정의 장점은 고화질의 선명한 이미지를 획득할 수 있으며, 측정된 이미지는 다양한 파일형식으로 변환하기 쉬운 장점을 지니고 있다. 하지만 스캐너의 크기가 한정적이기 때문[최대 사이즈: 30 cm (가로) × 40 cm (세로)]에 작물 뿌리의 표면적이 클 경우 측정이 불가능할 수 있다. 또한 작물의 뿌리가 생육 후기로 갈수록 폭이 넓어지고 뿌리조직도 목질화되기 때문에 폭이 좁은 스캐너에서 바로 측정하기 어려울 수 있다. 이럴 경우 뿌리를 여러 단편으로 절단하여 뿌리를 측정해야 하기 때문에 뿌리의 구조적 특성은 분석할 수 없다. 위 내용을 종합해 볼 때 스캐너를 이용하는 방법은 노지에서 대상작물의 뿌리규모가 클 경우 분석에 어려움이 있지만 뿌리를 세밀하게 관찰할 수 있는 장점이 있어 노지보다는 온실 내 포트에서 생장한 작물의 뿌리를 분석하는데 더 효과적이라 할 수 있다(Table 1).
뿌리 이미지 분석용 프로그램
본 리뷰에서는 유료, 무료로 사용할 수 있는 뿌리 분석용 프로그램을 각 1개씩 소개하였지만 이들 프로그램 이외에도 뿌리를 분석할 수 있는 프로그램은 다양하다. Lobet et al. (2013)가 발표한 논문에 수록된 홈페이지 www.plant-image-analysis.org에 접속하면 보다 많은 정보를 확인할 수 있다. 따라서 연구자들의 목적에 맞은 프로그램을 찾아 활용하면 될 것으로 생각된다.
WinRHIZO
작물의 뿌리를 촬영한 뒤 표현형 결과를 도출하기 위해서는 이미지분석용 프로그램을 이용해야 한다. WinRHIZO (Regent Instruments, Inc, Canada)는 뿌리 이미지 분석을 위해 고안된 전용프로그램으로 컴퓨터에 연결된 스캐너를 통해 획득한 이미지를 기반으로 뿌리의 형태적, 구조적 특성을 분석하는데 최적화되어 있다(Pang et al., 2011) (Table 1). WinRHIZO 프로그램을 개발한 Regent Instruments Inc.는 1991년부터 식물의 이미지 분석용 소프트웨어를 개발한 회사로 2021년 기준 WinRHIZO 2021a버전까지 업데이트되어 있다(https://regent.qc.ca/assets/winrhizo_about.html). 이 프로그램의 장점은 오랜 기간 동안 축적된 데이터를 기반으로 뿌리 이미지 분석에 최적화된 제품이란 것이다. 또한 WinRHIZO는 결합된 스캐너에서 측정된 이미지가 아닌 다른 하드웨어(RGB카메라)에서 수집된 이미지도 calibration 정보만 정확하게 입력하면 비교적 정확한 뿌리 표현형 분석이 가능하다(Table 1). 또한 WinRHIZO 프로그램은 4개의 버전이 있어 각기 기능과 가격이 다르기 때문에 사용자의 목적에 맞는 제품을 구매하여 사용할 수 있는 것이 장점이다. 하지만 성능이 우수한 대신 가격이 비싸고, 프로그램 실행을 위한 usb를 분실할 경우 프로그램을 새로 구매해야 하며, 최신버전으로 업데이트 하기 위해서는 추가적인 비용이 필요하다는 것이 단점이다.
Digital Image of Root Traits (DIRT)
DIRT 프로그램은 전통적인 뿌리 분석방식인 shovelomics에서 영감을 받아 만들어진 뿌리분석용 프로그램이다(Bucksch et al., 2014) (http://dirt.cyverse.org). DIRT 프로그램의 가장 큰 장점은 무료로 이용할 수 있다는 것이다(Table 1). 뿌리분석을 희망하는 사용자가 DIRT 프로토콜에서 요구하는 방식으로 뿌리 이미지를 측정하고 난 뒤 해당 이미지를 웹사이트에 접속하여 업로드하면 된다. 업로드 방식은 홈페이지에 자세하게 설명하고 있으므로 참고하면 된다. 업로드를 마친 이미지는 calibration과정을 거치고 난 뒤 뿌리영역은 흰색으로 배경은 검은색으로 변환되어 뿌리영역에 해당하는 표현형들을 획득할 수 있다(Das et al., 2015). 홈페이지에 소개된 내용에 따르면 약 70여 가지의 뿌리 표현형 분석이 가능하고, 식물의 종류 구분 없이 단자엽, 쌍자엽 모두 분석이 가능하다. DIRT 프로그램이 무료로 이용할 수 있는 것은 장점이지만 데이터를 분석하는 소요되는 시간은 상대적으로 긴 단점을 가지고 있다. 또한 사용 중 프로그램에 문제가 발생했을 때 이를 조치하기 위해서는 DIRT 프로그램을 개발한 그룹들이 직접 해결해야 하므로 사정에 따라 많은 시간이 필요할 수도 있다. 마지막으로 DIRT를 무료로 이용할 수 있지만 분석된 결과를 공유해야 한다는 것은 연구자들에게 부담으로 작용할 수 있다(Table 1).
적 요
뿌리는 식물에서 양분과 수분을 흡수하는 가장 중요한 기관임에도 불구하고 분석방법에 어려움으로 인해 지상부에 비해 연구가 상대적으로 미비한 실정이다. 최근 이미지를 기반으로 작물의 표현형을 분석하는 기술이 급격하게 발달하고 있으며, 뿌리 연구에 있어서도 이미지를 다양하게 활용하고 있다. 뿌리분석은 목적에 따라 토양에서 분리 후 측정하는 방법과 토양에서 바로 측정하는 방식이 있으며, 각각의 방식들마다 장점과 단점이 있으므로 연구자의 상황에 맞게 활용할 수 있다. 이런 이유에서 본 리뷰에서는 이미지를 활용한 뿌리분석 방법들에 대해 소개하여 국내 연구자들의 뿌리 연구에 이용되기를 바란다.




