서 론
재료 및 방법
실험재료 및 저온 처리
유채 Proline 분석
Total RNA 분리 및 RNA-Seq 분석
유전자 발현 및 DEG 분석
유전자 기능 분석
RT-PCR 분석
결과 및 고찰
0°C 이하의 저온 스트레스 처리에 따른 유채 proline 함량 및 생존율 변화
저온 처리 전후 유채 2 계통 전사체 분석
저온 처리로 인한 유채 2 계통 DEG의 기능적 분석(Functional analysis)
저온 스트레스에 반응하는 Proline 물질대사 관련 유전자 발현 비교
저온 스트레스에 관여하는 생리반응 경로 관련 유전자 발현 비교
저온 스트레스에 반응하는 유전자 발현 확인
적 요
서 론
0°C 이하의 저온 스트레스(Freezing stress)는 식물체가 0°C 이하의 온도 조건에 노출되었을 때 발생하는 비생물학적 스트레스의 일종이다. 식물이 0°C 이하의 저온에 노출되면 세포 간극의 수분이 얼게 되면서 얼음결정(ice formation)을 생성하게 되고 이러한 얼음 결정은 삼투 스트레스를 일으켜 세포 내 탈수 스트레스를 유발 한다(Trischuk et al., 2006; Sakai et al., 2012). 또한 0°C 이하의 저온 스트레스는 식물 세포의 원형질막의 유동성을 떨어뜨려 안정성을 저해시키며, 외부자극에 반응하는 통로를 차단하거나 단백질 파괴 등을 유발한다(Ruelland et al., 2009). 이로 인해 식물은 생장 및 발달과 작물의 생산성 및 품질에 심각한 피해를 입게 된다(Sanghera et al., 2011; Pu et al., 2019).
많은 식물들은 동해 전 0°C 이상의 일정한 저온에 노출되게 되면 내동성이 증가하게 되는 데, 이러한 현상은 ‘저온 순화(cold acclimation)’라고 보고되었다(Thomashow, 1999). 저온 순화는 매우 복잡한 과정으로, 수백 개의 유전자 발현 변화를 통해 많은 생화학 및 생리적 변화를 유발한다(Guy, 1990; Xin & Browse, 2000; Shi et al., 2018.). 저온 순화로 인한 변화는 식물의 생장을 억제하여 조직 내 수분 함량을 감소시키고, ABA (Abscisic acid) 호르몬 함량을 증가시키며, 막 지질 구성요소를 변화시키고, proline, betaine, soluble sugars와 같은 삼투 스트레스에 저항할 수 있는 물질을 축적시킨다(Levitt, 1980; Chen et al., 1983; Lynch & Steponkus, 1987; Koster & Lynch, 1992; TaO et al., 1998).
Proline은 식물체 내에서 많은 스트레스에 반응하며 함량이 증가된다. Proline은 비생물학적 스트레스를 막기 위해 식물체 내에서 생합성되고, 세포질 내 축적되어 molecular chaperon으로써 단백질 구조를 안정화 시키고, 세포질 pH에 대해 완충 역할을 하며 세포 내 산화환원 반응을 유지시켜, 세포 파괴를 막는다고 알려져 있다(Verbruggen & Hermans, 2008; Szabados & Amould, 2010; Hayat et al., 2012). 또한 ABA 호르몬은 대표적인 스트레스에 반응하는 식물 호르몬으로 기공의 개폐 조절 등에 관여하고 생장과 발달에 영향을 미치며, 가뭄, 저온, 고온 등의 스트레스 조건에서 식물이 살아남을 수 있는 저항성을 갖게 한다(Shinozaki & Yamaguch-Shinozaki, 2000; Schroeder et al., 2001). 또한 이러한 저온 순화에 기여하는 저온 반응 유전자 발현을 조절하는 기작으로는 ICE (Inducer of CBF expression) - CBF (C-repeat-binding factor) - COR (Cold-regulated) 신호 경로가 있다(Shi et al., 2018). 저온에 감응하여 과발현된 ICE는 CBF와 결합하여 COR 유전자를 발현시키고 저온 순화와 관련된 COR 유전자의 downstream 유전자들이 발현되어 내동성을 갖는다고 보고되었다(Xin & Browse, 2000; Chinnusamy et al., 2007; Ritonga & Chen, 2020).
유채는 전세계적으로 소비되는 카놀라(canola)유를 생산하는 작물로, 중국, 유럽, 우리나라 등에서는 가을에 재배하여 이듬해 봄, 여름에 수확하는 동계작물이다(Burbulis et al., 2011; Pu et al., 2019; Xin et al., 2019). 동계작물인 유채는 생육기간 중 저온과 0°C 이하의 저온 스트레스에 노출될 수밖에 없는데, 이와 관련된 여러 연구들이 보고되었다. 기존 연구 결과에서 유채 10 품종을 대상으로 한 0°C 이하의 저온 노출 기간에 따른 생존율 등의 조사에서 내성을 갖는 ‘Tosca’ 품종을 선발하였다(Waalen et al., 2011). 또한 7개 유채 품종을 대상으로 4°C 저온 순화 기간에 따라 내동성을 확인한 결과, proline 및 soluble sugar 함량이 증가함을 확인하였고 ‘Valesca’ 품종에서 이온 누출도가 낮고 생장 피해를 덜 입는 다는 결과가 보고되었다(Burbulis et al., 2011).
유채의 이러한 내동성 기작에 관한 연구는 차세대염기서열분석(Next generation sequencing) 기술이 발달하여 염기서열 연구 변화가 대량화됨에 따라 염기서열 연구 분야에서도 수행되어왔다. 최근 연구에서는 중국의 유채 계통인 ‘2016TS(G)10’을 대상으로 저온 및 0°C 이하의 저온 스트레스를 처리한 결과, 저온 순화 조건에서 soluble sugar, proline, MDA (Malondialdehyde) 함량이 증가하고 세포 내 전분이 축적되는 결과를 확인하였으며, 이를 바탕으로 저온 순화 조건에서 전사체 분석 연구가 수행되어 관련 기작에 대해 보고되었다(Pu et al., 2019). 또한 유채 ‘HX17’과 ‘HX58’ 품종의 서로 다른 내동성을 확인하고 두 품종을 저온(4°C)과 0°C 이하의 저온(-4°C) 스트레스에 노출 시켰을 때 전사체의 발현 양상을 비교하는 연구도 수행되었다(Xin et al., 2019). 국내에서도 국내 육성 5개의 유채 품종의 내동성을 확인하였으며, microarray 분석을 통해 내성을 갖는 ‘내한’ 품종과 중간 내성 ‘영산’, 민감성 ‘탐미’ 품종의 발현된 유전자군을 비교한 연구가 수행되었다(Jeong et al., 2012).
따라서 본 연구는 국내에서 육성한 유채 2 계통 ‘J8634- B-30’과 ‘EMS26’을 대상으로 0°C 이하의 저온 스트레스를 처리하여 이에 따른 생리적 변화를 확인하고 이와 관련된 저온 순화 시 유전자들의 발현 양상을 전사체 수준에서 확인하여, 국내 유채 계통의 내동성 향상을 위한 저온순화 기작을 이해함으로써 내동성을 갖는 유채 품종 육종에 기초 자료로 활용하기 위해 수행되었다.
재료 및 방법
실험재료 및 저온 처리
본 시험에 사용된 유채 계통은 국립식량과학원에서 육성한 ‘J8634-B-30’과 ‘EMS26’이었다. ‘J8634-B-30’ 유채 계통은 기존 내동성 검정 시험 결과 내동성 계통으로 선발된 계통이었으며, ‘EMS26’ 유채 계통은 유채 ‘탐라’ 계통에 EMS (Ethyl Methane Sulfonate)를 처리하여 인위적인 돌연변이를 유도하고 자가 수정을 통해 6세대까지 세대를 전개 시킨 계통으로 지방산 조성 중 올레산 함량이 70%가 넘는 우수한 식용유 품질을 갖는 계통이다.
유채 두 계통을 대상으로 각 계통 당 72공 트레이에 12공(1립씩 파종, 1 개체)을 한 세트로 5세트(전체 60 개체)를 준비하여 스트레스를 처리하였다. 이 중 2 세트(24 개체)에서 처리 전후 proline 분석을 위해 지상부 3 개체 시료(총 15 개체)를 채취하여 각 시점 당 3 반복으로 사용하였으며, RNA 분석을 위하여 처리 전, 후 2 개체 시료(총 4 개체)를 반복으로 사용하였다. 남은 3세트는 12 개체를 기준으로 스트레스 처리 후 생존율 확인을 위한 3반복으로 사용하였다.
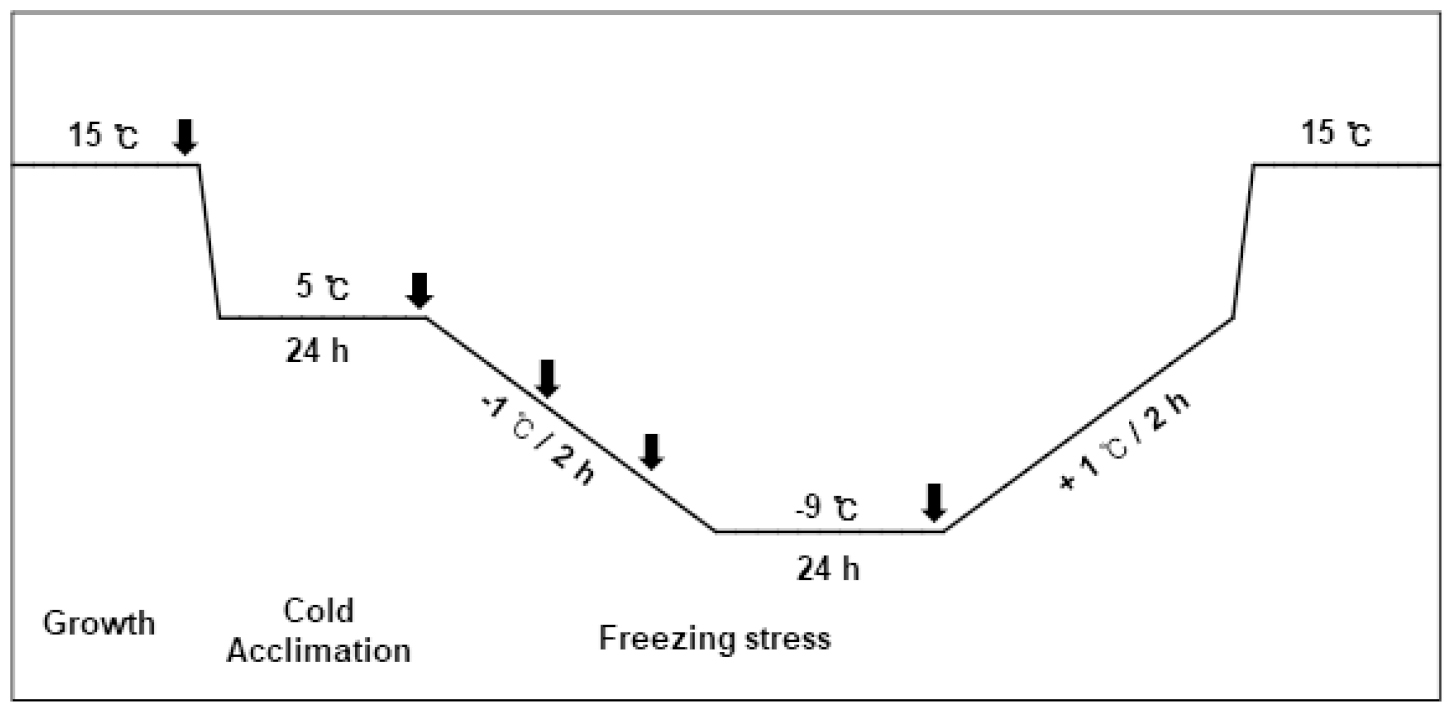
0°C 이하의 저온 스트레스 처리 조건은 Jeong et al. (2012)을 참조하여 다음과 같이 변형하여 처리하였다(Fig. S1). 0°C 이하의 저온 스트레스 처리는 15°C 조건에서 생육한 본엽 3∼4기의 유채를 5°C에서 24시간 동안 저온 순화(Cold acclimation) 시킨 후, 2시간에 1°C씩 온도를 내려 -9°C에서 24시간 동안 0°C 이하의 저온 스트레스 처리(Freezing stress)하였다. 이후 2시간에 1°C씩 15°C까지 온도를 올린 후 저온 처리를 마무리하였다. Proline 등을 조사하기 위해 처리전(15°C), 저온순화 후(5°C), 온도 감온 2시기(0°C와 -5°C), 0°C 이하의 저온 스트레스 처리 후(-9°C) 유채 지상부를 채취하였다. RNA seq 분석을 위한 시료는 처리전(15°C)과 저온순화 후(5°C) 유채 지상부를 채취하였다.
생존율은 0°C 이하의 저온 스트레스 처리 종료 일주일 및 한 달 후 살아남은 유채 개체를 조사하여 확인하였다. 생존율은 12 개체(1세트)를 1 반복으로 다음과 같이 3반복으로 조사하였다: [(일주일 혹은 한 달 후 살아남은 개체)/처리 전 개체(12 개체)] × 100.
유채 Proline 분석
유채 proline 함량은 ninhydrin 방법을 변형하여 측정하였다(McClinchey et al., 2008). 지상부 시료 0.3 g에 증류수를 넣고 100°C에서 30분간 가열 후, 상등액 200 μl과 acid ninhydrin (ninhydrin 0.25 g + acetic acid 15 ml + 증류수 10 ml) 1 ml, 증류수 400 ml를 넣고 20분간 100°C에서 가열하였다. 가열된 분석액을 냉각시킨 후 toluene 3 ml를 첨가하여 암조건에서 2시간 반응시켰다. 이후 520 nm 흡광도를 측정하였으며, L-proline으로 표준곡선을 작성한 후 proline 함량은 3 반복으로 계산하였다. Proline 함량 간의 평균에 대한 통계분석은 ANOVA 분석 후, Duncan 다중 검정을 실시하였다(R version 3.6.1).
Total RNA 분리 및 RNA-Seq 분석
Total RNA는 채취한 유채 지상부 0.1 g의 시료를 Mini BEST Plant RNA extraction kit (TaKaRa Bio Inc, Japan)를 이용하여 분리하였고, Bioanalyzer (Agilent Technologies, USA)를 사용하여 농도를 측정하다. 분리된 total RNA 2 μg은 Illumina TruSeq RNA Sample Preparation Kit를 사용하여 300 bp insert size로 RNA-Seq library를 제작하였고, Illumina HiSeq X platform (Illumina, SanDiego, CA)을 이용하여 101 bp paired-end reads를 생성하였다(Macrogen Co, Seoul, Korea). 낮은 품질과 duplicated된 reads, adapter sequence들은 Trimmomatic (ver. 0.38, Bolger et al., 2014)를 이용하여 제거하였다.
유전자 발현 및 DEG 분석
정제된 RNA-Seq read들은 HISAT2 (Kim et al., 2015) 프로그램을 이용하여 유채 표준유전체 서열(v4.1, http://www. genoscope.cns.fr/brassicanapus/, Chalhoub et al., 2014)에 맵핑하였다. 이후 HTSeq-count (Anders et al., 2015)를 사용하여 단백질 코딩 서열에 맵핑된 RNA read들을 계산하였고, 이를 FPKM (Fragment Per Kilobase of transcript per Million mapped reads) 계산에 사용하였다.
유채 두 계통의 처리전과 저온순화 후 전사체 사이의 DEG (Differentially-expressed genes)는 각 시료당 2반복으로 비교하고자 하는 시료의 count 값을 기반으로 Bioconductor package DESeq (Anders & Huber, 2010)를 이용하여 DESeq Normalization 값을 산출하였다. 이를 이용하여 산출된 유전자들 중 P-value 값을 Benjamini-Hochberg의 방법으로 조절한 FDR (False Discovery Rate) 값을 이용하여 보정된 adjusted P-value 값이 0.05 이하 값을 만족하는 유전자들을 대상으로 Log2 fold change를 사용한 up/down regulation 분석을 실시하였다. 이중 Log2 fold chage 값이 절대값 1 이상이면, 발현량이 2배 이상 차이를 보인다는 것으로 판단하여 이를 기준으로 DEG로 선별하였다.
유전자 기능 분석
GO (Gene ontology) enrichment 분석은 BLAST2GO 프로그램(v5.2)을 사용하여 Fisher’s exact test 방법(adjusted P-value < 0.05)으로 DEG 유전자들을 분석하였으며, p- value < 0.01, FDR (False discovery rate) < 0.01, 선택된 유전자의 fold change가 전체 유전자 대비 2배 이상의 조건으로 필터링하였다. 이후 선택된 유전자를 생물학적 기능(Biological processes), 분자 기능(Molecular function), 그리고 세포 요소(Cellular component)로 분류하였다. 기능이 확인된 DEG들을중 Proline metabolism, ABA pathway, 저온 관련 유전자 등을 탐색 하여 선발한 후, MeV (v.4.9.0) 프로그램을 사용하여 heatmap을 그렸다.
RT-PCR 분석
특이적인 발현이 확인된 DEG들의 유전자 발현을 확인하기 위하여, 처리전(15°C), 저온순화 후(5°C), 온도 감온시기(-5°C), 0°C 이하의 저온 스트레스 처리 후(-9°C) 유채 지상부를 채취하였다. 채취한 유채 지상부는 앞선 방법과 동일하게 RNA를 분리하였으며, 동량의 RNA를 사용하여 1st strand cDNA synthesis kit (TaKaRa Bio Inc, Japan)를 이용하여 cDNA를 합성하였다. 유전자 발현 확인 위해 선별된 DEG의 primer 목록은 Table S1과 같으며, Bactin은 internal control로 사용하였다(Lee et al., 2013).
결과 및 고찰
0°C 이하의 저온 스트레스 처리에 따른 유채 proline 함량 및 생존율 변화
0°C 이하의 저온 스트레스 처리 후 두 유채 계통에서는 proline 함량에서 다른 변화를 보였다(Fig. 1a). 처리 전 proline의 함량은 ‘EMS26’에서 0.76 mM/g FW로 ‘J8634-B-30’ 0.23 mM/g FW보다 약 3.3배 높았다. 그러나 저온 순화를 한 ‘J8634-B-30’ 계통에서 proline 함량이 2.02 mM/g FW로 처리 전보다 8.7배 높아졌으나, ‘EMS26’ 계통에서는 0.80 mM/g FW으로 차이를 보이지 않았으며 처리 전반적으로 통계적 유의성을 보이지 않았다. 저온 순화 후 0°C에서 ‘J8634-B-30’ 계통의 proline 함량은 2.28 mM/g FW, -5°C에서 2.33 mM/g FW로 높게 유지되었다. 이후 -9°C에서 24시간 처리 후 ‘J8634-B-30’ 계통의 proline 함량은 1.21 mM/g FW으로 약간 감소하였다. 다만, 식물체 내에서 식물 0°C 이하의 저온 스트레스 피해의 지표로 많이 사용되고 있는 엽록소 함량, 이온 누출도의 경우 두 유채 계통간의 차이는 발견되지 않았다(Data not shown). 이러한 연구 결과는 내한성 유채 품종을 선발하기 위한 기존 연구에서도 proline 함량 증가만이 0°C 이하의 저온 스트레스 처리 후 높은 생존율과 연관성이 있다는 보고와 유사한 결과였다(Kim, 2015).
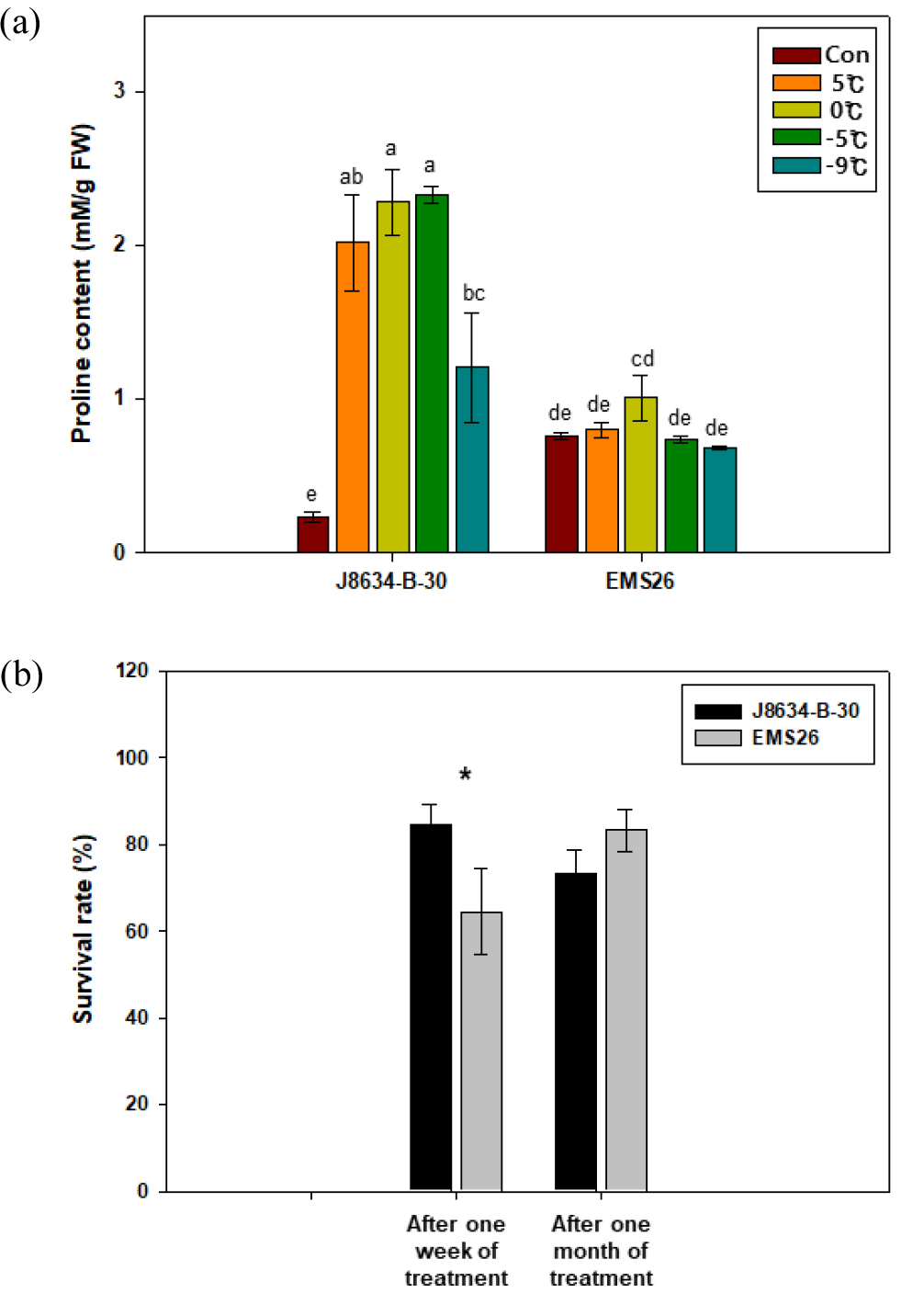
Fig. 1.
Changes in proline content (a) and survival rate (b) of two rapeseed lines according to freezing treatment. Con (Control) indicates 15°C. Bars represent standard error. Different lowercase letters indicate significant difference at P < 0.05 according to Duncan’s multiple range test. The asterisk indicates significant difference at P < 0.05 according to T-test.
0°C 이하의 저온 스트레스 처리 종료 일주일 후 유채 두 계통의 생존율을 조사한 결과, ‘J8634-B-30’ 계통에서 84.6%로 ‘EMS26’ 계통의 생존율 64.4% 보다 높아 초기 0°C 이하의 저온 스트레스 피해에 내성을 보였다(Fig. 1b). 이후 처리 한 달 뒤 유채 두 계통의 생존율을 조사한 결과, ‘J8634- B-30’에서 73.4%, ‘EMS26’ 계통에서 83.3%로 차이를 보이지 않았다. 이는 ‘EMS26’ 계통 중 본엽이 모두 고사하였다고 판단한 개체에서 새 잎이 생장하여 생존 개체 수가 변화하였기 때문으로 판단된다. 이러한 결과는 ‘EMS26’ 개체가 0°C 이하의 저온 스트레스에 대해 장기적인 내동성을 보여 최종적으로 유채 두 계통에서의 0°C 이하의 저온 스트레스에 대한 내성이 비슷한 수준으로 나타난 것으로 판단된다.
저온 처리 전후 유채 2 계통 전사체 분석
유채의 초기 내동성과 관련된 기작을 확인하가 위해, 0°C 이하의 저온 스트레스 처리로 proline 함량이 급격한 변화를 보인 5°C 처리 유채 시료와 처리 전(15°C) 유채 시료의 전사체를 각각 유채 2 계통에서 비교 분석하였다(Table 1). 전체 정제된 read들의 개수는 50,111,336∼60,133,544개였으며, 전체 read 길이는 7.3∼8.8 Gb였다. Read의 품질을 나타내는 Q30 이상의 read들은 전체 read들의 98.0∼98.1%로 나타났으며, 전체 read들의 86.0∼90.5%가 유채 표준유전체에 맵핑되었다. 발현된 전사체 비율은 전체 표준유전체의 전사체에 대해 시료 read가 적어도 1개 이상 맵핑된 전사체(유전자)의 비율로써 표준유전체 대비 61.0∼65.3%가 시료 전사체에서 맵핑되었다.
Table 1.
The alignment statistics data of the reference gene for B. napus samples.
| Sample name | Trimmed reads | Read Bases | GC (%) | %≥Q30 | Mapped reads (%) | Expressed genes (%) |
| J8634_Con_1 | 50,111,336 | 7,343,661,008 | 46.41 | 98.08 | 89.21 | 65.27 |
| J8634_Con_2 | 56,626,338 | 8,269,505,242 | 46.65 | 98.08 | 85.96 | 64.47 |
| J8634_Treat_1 | 60,133,544 | 8,803,705,393 | 47.68 | 98.07 | 90.03 | 63.85 |
| J8634_Treat_2 | 52,787,030 | 7,734,751,081 | 47.51 | 98.06 | 89.81 | 63.41 |
| EMS26_Con_1 | 55,220,650 | 8,101,701,706 | 46.46 | 98.08 | 90.00 | 64.09 |
| EMS26_Con_2 | 52,359,812 | 7,627,197,929 | 46.60 | 98.10 | 90.47 | 64.88 |
| EMS26_Treat_1 | 50,938,796 | 7,444,117,983 | 46.42 | 98.09 | 90.07 | 61.01 |
| EMS26_Treat_2 | 54,792,402 | 8,009,480,373 | 47.09 | 98.03 | 90.47 | 61.24 |
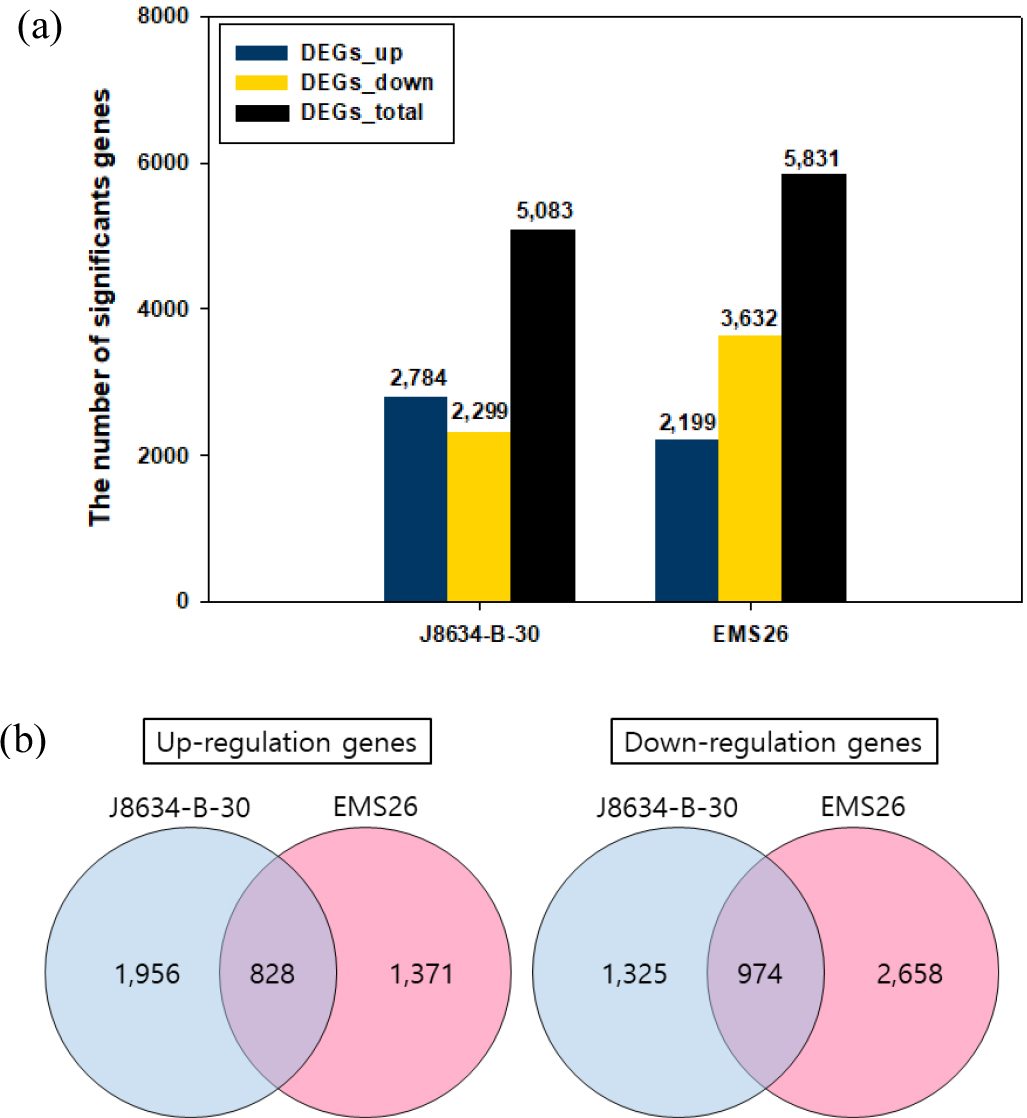
저온 처리 전과 후 전사체의 DEG는 ‘J8634-B-30’과 ‘EMS 26’에서 각각 5,083개, 5,831개였다(Fig. 2a). ‘J8634-B-30’ 계통의 DEG는 발현이 유도된 유전자의 수가 2,784개로 발현이 억제된 유전자 2,299개 보다 많았으나, ‘EMS26’ 계통의 DEG는 발현이 유도된 유전자 수가 2,199개로, 발현이 억제된 유전자 수 3,632개 보다 적었다. 두 계통에서 공통적으로 발현이 유도된 DEG는 828개였으며, 발현이 억제된 DEG는 974개였다(Fig. 2b).
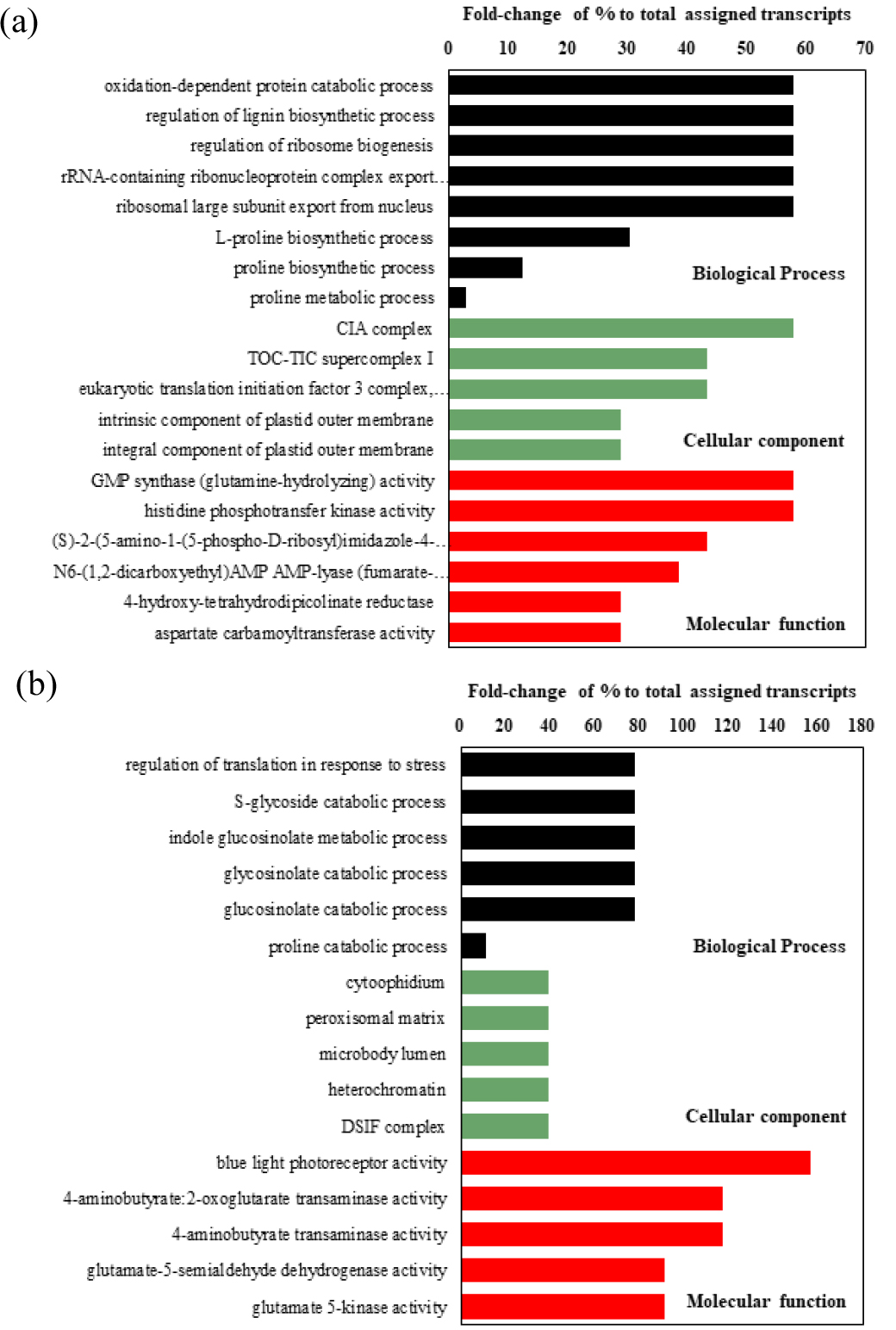
DEG를 바탕으로 GO 분석을 실시하고 각 주요 GO 3 그룹별로 분류하여 각 그룹의 상위 5개 GO term을 분석한 결과, ‘J8634-B-30’ 계통에서는 oxidation-dependent protein catabolic process, lignin 생합성 과정 조절, ribosome biogenesis 관련 GO 발현이 높았으며, proline 관련 GO term도 3종류 발현이 높은 것을 확인 할 수 있었다(Fig. 3a, Table S2). 반면, (+)-abscisic acid D-glucopyranosyl ester transmembrane transport, (+)-abscisic acid D-glucopyranosyl ester transmembrane transporter activity 등 ABA transport와 관련된 GO term의 발현이 억제되는 것을 확인 할 수 있었다(Table S3).
‘EMS26’ 계통에서는 스트레스에 반응하는 translation 조절, S-glycoside catabolic 과정 등에서 발현이 높은 양상을 보였으며, proline 관련 GO term은 1 종류에서 발현이 높은 것을 확인 할 수 있었다(Fig. 3b, Table S4). 반면, shikimate metabolic process, cellular response to sulfur starvation, shikimate 3-dehydrogenase (NADP+) activity 관련 GO term의 발현이 억제되는 것을 확인 할 수 있었다(Table S5).
저온 처리로 인한 유채 2 계통 DEG의 기능적 분석(Functional analysis)
유채 2 계통의 전사체 발현 비교를 위해, 2 계통의 각각의 상위 100개 DEG를 선발하고 발현 패턴을 비교하였다(Fig. 4). 발현이 강하게 유도된 각각의 상위 100개의 DEG 중 21개의 DEG가 공통적으로 상위 100개의 DEG로 선별되어 총 179개의 DEG의 발현을 두 계통에서 비교하였으며(Fig. 4a, Table S6), 발현이 강하게 억제된 각 계통의 상위 100개 DEG 중 11개의 DEG가 공통적으로 확인되어 총 189개의 DEG의 발현을 두 계통에서 비교하였다(Fig. 4b, Table S7).
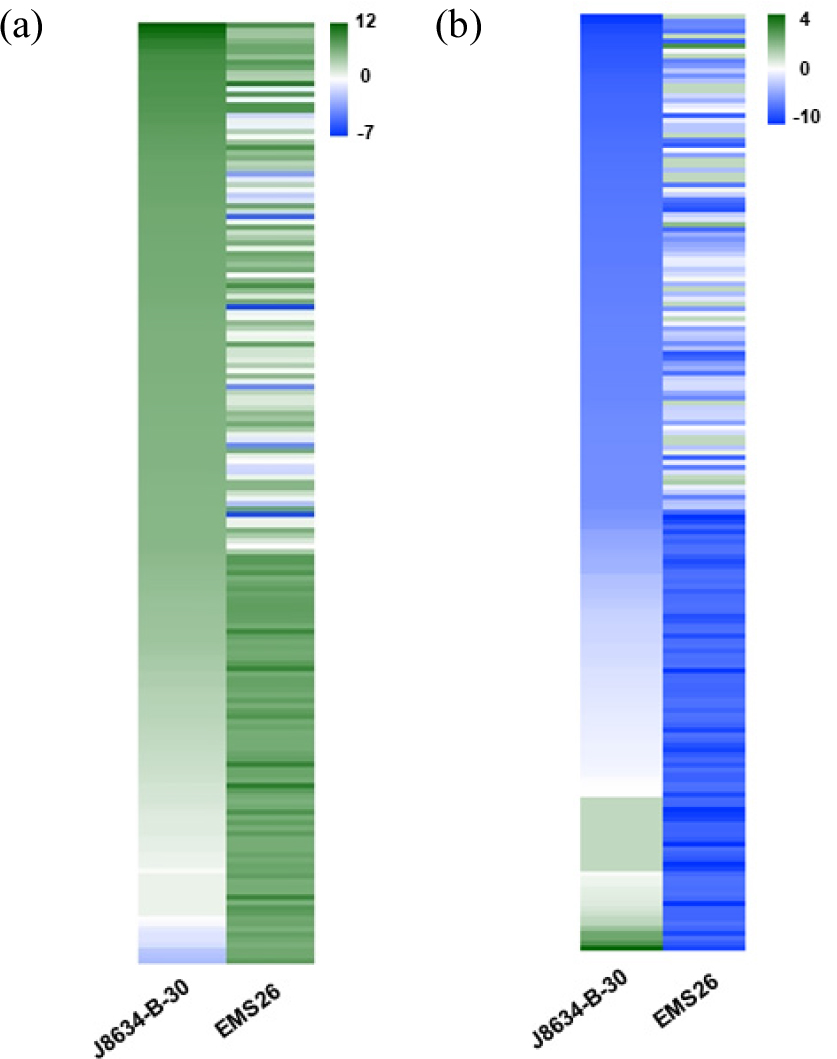
Fig. 4.
Heatmap analysis of Top 100 up- and down-regulated DEGs in two rapeseed lines. The heatmap represent up (a) or down (b) regulated top 100 DEGs under cold treatment in two rapeseed lines. Twenty-one DEGs were the common up-regulated DEGs between ‘J8634-B-30’ and ‘EMS26’. Eleven DEGs were the common down- regulated DEGs between ‘J8634-B-30’ and ‘EMS26’. The expression levels of each gene (log2 fold change) are indicated by different colors. Green and blue means up- and down- regulation, respectively.
발현이 강하게 유도된 각각의 상위 100개의 DEG를 비교한 결과, BnaA10g21640D, BnaAnng32690D, BnaC06g23700D 같은 유전자는 ‘EMS26’ 대비 ‘J8634-B-30’ 계통에서 강하게 발현이 유도되었다(Fig. 4a). BnaA10g21640D (Flowering- promoting factor 1-like protein 2)는 flowering- promoting factor 관련 유전자로 Litchi chinensis에서는 저온과 ROS (Reactive Oxygen Species) 반응과 관련된 유전자로 분류되어 저온 처리 후 발현이 유도된다고 보고된 바 있다(Lu et al., 2017). BnaAnng32690D와 BnaC06g23700D는 각각 peroxidase, 식물체 병원균 방어 기제에 관여하는 kunitz trypsin inhibitor 1-like 관련 유전자로, Pu (2019) 등은 유채 0°C 이하의 저온 스트레스 반응 시 식물-병원균 상호작용 관련 유전자군의 발현이 증가했다고 보고하여 이와 관련이 있을 것으로 판단된다. 0°C 이하의 저온 스트레스 내성에 관련된 proline 합성 관련 BnaA04g22810D, BmaC04g46630D 유전자 역시 ‘J8634-B-30’ 계통에서는 log2 fold chage 값이 각각 7.0, 6.5로 발현이 강하게 유도되었다. 또한 cytochrome P450 관련 BnaC01g01500D 유전자는 ‘J8634-B-30’ 계통의 DEG 에서는 발현이 유도되었지만, ‘EMS26’ 계통에서는 발현이 크게 감소하여 상반된 발현 패턴을 보였다. Cytochrome P450 단백질은 생물적 및 비 생물적 스트레스의 방어기작에 관여한다고 보고되었으며, 특히 수수의 전사체 분석에서는 저온 스트레스하에 발현이 유도됐다고 보고된 바 있다(Narusaka et al., 2004; Chopra et al., 2015).
발현이 많이 억제된 각각의 상위 100개의 DEG의 경우, 두 계통에서 공통적으로 강하게 억제되는 BnaA03g57560D, BnaC03g38520D, BnaC07g05770D 등의 유전자들은 아직 기능이 밝혀지지 않은 것으로 나타났다(Fig. 4b). ‘EMS26’ 계통의 DEG 중 ‘J8634-B-30’ 계통 대비 발현이 억제된 유전자는 BnaC02g41180D, BnaC01g12610D, BnaC02g31910D 등이었다. BnaC02g41180D는 heavy metal-associated isoprenylated plant protein을 코딩하는 유전자로, 벼에서 저온과 가뭄 스트레스 조건에서 품종에 따라 발현이 유도되어 환경 스트레스 반응에 역할을 할 것이라 보고된 바 있다(de Abreu-Neto et al., 2013). BnaC01g12610D와 BnaC02g31910D는 각각 gibberellin 2-beta-dioxygenase과 senescence-specific cystein protease SAG12 유전자로 식물체 생장과 관련된 유전자였다.
저온 스트레스에 반응하는 Proline 물질대사 관련 유전자 발현 비교
식물 내 proline 축적은 생합성과 이화작용(Cataboilsm) 사이의 균형에 의해 좌우된다(Sharma et al., 2011). 식물에서 proline은 glutamate pathway와 ornithine pathway에 의해 생합성된다고 알려져 있다(Fig. 5a). 먼저 glutamate는 Δ’- pyrroline-5-carboxylate synthetase (P5CS)에 의해 Δ’-pyrroline- 5-carboxylate (P5C)로 변환되고, 이후 Δ’-pyrroline-5-carboxylate reductase (P5CR)에 의해 proline으로 생합성된다(Hu et al., 1992; Savouré et al., 1995). Proline의 이화작용은 미토콘드리아 안에서 일어나며, proline dehydrogenase (PDH)에 의해 P5C로 전환 된 후, P5C dehydrogenase (P5CDH)에 의해 다시 glutamate로 변환된다(Deuschle et al., 2001; Ribarits et al., 2007).
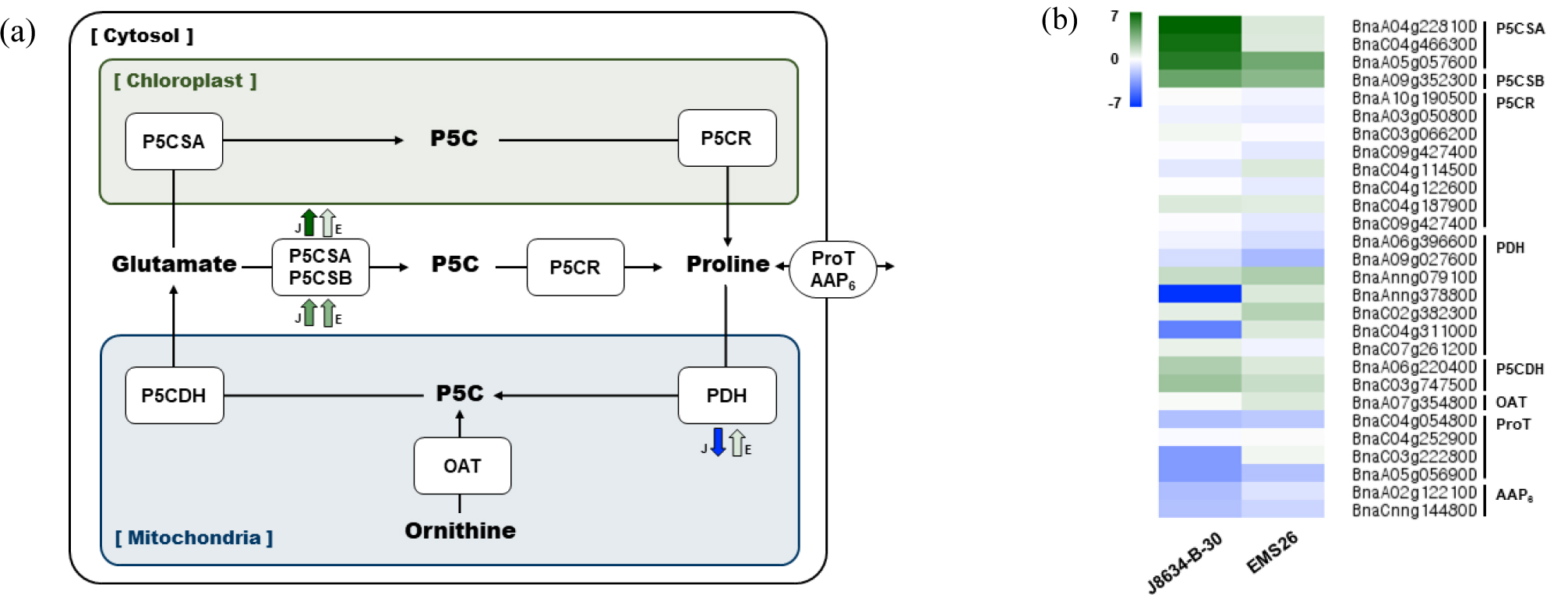
Fig. 5.
Proline metabolism in plants. (a) Proline metabolism step. ‘J’; ‘J8634-B-30, ‘E’; ‘EMS26’. The arrows indicate up- or down- regulated DEGs. (Figure adapted from Hayat et al., 2012). (b) Heatmap analysis of genes involved in proline metabolism in two rapeseed lines. P5CS (Δ’-pyrroline-5-carboxylate synthetase), P5CR (Δ’-pyrroline-5-carboxylate reductase), PDH (Proline dehydrogenase), P5CDH (P5C dehydrogenase), OAT (Orinithine-delta-aminotransferase), ProT (Proline transporter), and AAP6 (Amino acid permease 6). The expression levels of each gene (log2 fold change) are indicated by different colors. Green and blue means up- and down- regulation, respectively.
0°C 이하의 저온 스트레스 처리에 의한 유채 2 계통의 DEG 중 proline 생합성과 이화작용에 관여하는 유전자들의 발현 양상은 계통 간 차이를 보였다(Fig. 5b). P5CS 유전자 중 P5CSA 유전자인 BnaA04g22810D와 BnaC04g46630D 유전자들은 ’EMS26’ 계통에서는 거의 발현이 되지 않았지만, ‘J8634-B-30’ 계통에서는 log2 fold change 값이 각각 7.0, 6.5로 나타나 강하게 발현이 유도되었다. P5CSB 유전자인 BnaA09g35230D는 두 계통에서 유사한 발현 패턴을 보였다. 또한, ornithine를 P5C로 변환시키는 OAT 유전자(Verbruggen & Christian, 2008; Hayat et al., 2012)에서는 두 유채 계통 모두 특이적인 발현 변화를 보이지 않았다. Proline을 다른 세포로 운반시키는 transporter인 proline transporter (ProT)와 amino acid permease 6 (AAP6)의 발현은 두 유채 계통에서 유사하게 발현이 억제되어 세포 내 축적을 유도한다는 것을 확인하였다. 식물체내 proline의 생합성은 주로 P5CS 유전자에 의해 강력하게 조절된다고 보고되고 있어(Szabados & Amould, 2010; Sharma et al., 2011; Pu et al., 2019), 본 결과 또한 P5CSA 유전자가 강하게 발현이 유도되어 ‘J8634-B-30’ 계통에서 proline이 축적된 것으로 판단된다.
유채의 proline 이화작용과 관련된 유전자 중 PDH를 코딩하는 BnaAnng37880D와 BnaC04g31100D 유전자들은 ‘EMS26’ 계통에서는 발현 변화가 없었으나, ‘J8634-B-30’ 계통에서는 log2 fold change 값이 각각 -7.6, -4.3으로 강력하게 발현이 억제됨을 확인하였다(Fig. 5b). 이러한 결과들을 종합해 볼 때, proline의 생합성을 유도하는 P5CS 유전자가 강하게 유도되고 proline을 분해시키는 PDH 유전자가 억제됨으로써, ‘J8634-B-30’ 계통에서 저온 처리에 의한 proline 함량이 증가한 것으로 판단된다.
저온 스트레스에 관여하는 생리반응 경로 관련 유전자 발현 비교
식물의 저온 피해에 반응하는 대표적인 호르몬인 ABA 신호 체계가 유채 두 계통의 저온 반응에 미치는 영향을 확인하기 위해 관련 유전자를 선별하여 발현 양상을 확인하였다(Fig. 6a). ABA 수용체로 알려진 PYR (Pyrabactin resistance)와 PYL (Pyrabactin resistance-like protein)는 ABA가 존재할 때, SRK2 (SNF1-related kinase 2)를 억제하고 있는 PP2C (Protein phosphatase 2C)와 결합하여 SRK2를 활성화 시킨다(Ng et al., 2014; Sah et al., 2016). 이후 SRK2는 transcription factor 같은 downstream 유전자들을 활성화 시켜, 이온 이동, 유전자 발현, 대사 작용을 유도하고 이로 인해 식물체는 비생물학적 스트레스에 내성을 갖게 된다(Hrabak et al., 2003; Saruhashi et al., 2015). ABA 수용체인 PYL5 유전자를 코딩하는 BnaAnng40650D는 ‘J8634-B-30’ 계통에서 log2 fold change 값이 4.2로 강하게 발현되는 것을 확인하였으며, PYL9 유전자인 BnaA07g38130D와 BnaC06g17940D 또한 ‘J8634-B-30’ 계통에서만 발현이 강하게 유도됨을 확인하였다(Fig. 6a). 벼에서 확인된 OsPYL9 유전자는 가뭄과 저온에 반응하는 ABA receptor로 이 유전자를 과발현시킨 벼에서는 저온 스트레스에 내성이 향상된다는 결과가 보고되었다(Tian et al., 2015). PYL7인 BnaC03g31730D 유전자는 ‘J8634-B-30’와 ‘EMS26’ 계통에서 log2 fold change 값이 각각 3.4, 5.0으로 나타나 두 계통에서 공통적으로 강하게 발현이 유도되었으며, 본 결과와 유사하게 기존 유채에서 저온과 0°C 이하의 저온 스트레스 처리에 의해 PYL7 유전자의 발현이 유도된다고 보고된 바 있다(Xin et al., 2019).

Fig. 6.
Heatmap analysis of the genes in ABA signal pathway (a) CE-DREB-COR signal pathway (b), cold shock domain related protein (c) and vernalization pathway (d). PYR (Pyrabactin resistance); PYL (Pyrabactin resistance-like protein); ABA receptor, ABI (Abscisic acid- insensitive); bZIP transcription factor, HAB (Hypersensitive to ABA); Protein phosphatase 2C, AHG (ABA-hypersensitive germination); Protein phosphatase 2C, SRK2 (SNF1-related kinase 2); Serine/threonine- protein kinase. ICE (Inducer of CBF expression); bHLH transcription factor, DREB (Dehydration responsive element- binding); CBF (C-repeat-binding factor), COR (Cold-regulated), VRN (Vernalization); B3 domain-containing transcripton factor and Zinc finger protein, VIN (Vernalization insensitive); PHD finger protein, VIL (VIN3-like protein), FLC (Flowering locus C); MADS-box protein. The expression levels of each gene (log2 fold change) are indicated by different colors. Green and blue means up- and down- regulation, respectively.
유채 두 계통의 PP2C (Protein phosphatase 2C) 그룹 중 ABI (Abscisic acid-insensitive) 유전자군과 SRK2 유전자군에서는 특이적인 발현 변화를 보이지 않았으며, SRK2J인 BnaC04g35560D 유전자는 ‘J8634-B-30’ 계통에서 발현이 강하게 억제되는 것을 확인하였다. SRK2J 유전자는 삼투압 스트레스에 반응한다고 알려져 있으며, SRK2A, SRK2D, SRK2E, SRK2I 유전자와 함께, SRK2 subclass 중 ABA에 반응하지 않다고 보고된바 있다(Boudsocq et al., 2004; Ng et al., 2014).
식물체의 저온순화와 관련된 대표적인 신호체계에는 ICE- CBF-COR 신호 회로가 있다. 저온 처리 초기 ICE는 transcription factor로 CBF와 함께 COR 유전자 promoter의 cis-element에 결합하여 COR 유전자의 발현을 유도한다(Chinnusamy et al., 2007; Ritonga & Chen, 2020). CBF는 DREB1 (dehydration- responsive element-binding proteins)에 속하는 단백질로 식물체 내에서 건조 및 저온 스트레스하에 발현이 유도된다고 보고되었다(Sakuma et al., 2002; Borba et al., 2018).
유채 2 계통의 DREB1를 코딩하는 유전자 중 BnaC03g 71900D, BnaA03g13620D, BnaA10g07630D는 ‘EMS26’에서만 발현이 강하게 유도되었으며, BnaCnng49280D는 두 계통 모두 발현이 강하게 유도되었다(Fig, 6b). BnaCnng49280D는 이전 연구에서도 유채의 ‘HX17’, ‘HX58’ 계통에서도 강하게 발현이 유도된다고 보고되었다(Xin et al., 2019). 반면, DREB3 유전자 BnaA10g20950D, BnaC02g03940D, BnaC09g45000D는 유채 2 계통에서 모두 발현이 억제되었다. DREB3는 저온 스트레스에 반응한다는 결과보다 과발현 시켰을 시 고온과 염스트레스에 내성이 보인다는 결과가 보고된 바 있어(Niu et al., 2020), 이러한 결과가 나타났을 것으로 판단된다.
저온에 반응하는 COR15A와 COR15B 유전자의 발현은 유채 2 계통 모두 발현에 변화를 보이지 않았지만, COR413 유전자 BnaA08g15470D와 BnaC03g61740D는 ‘J8634-B-30’ 계통에서만 발현이 강하게 유도되는 결과를 보였다(Fig. 6b). COR413 유전자는 원형질막 단백질로 알려져 있으며, 건조 및 저온 스트레스하에 식물체의 원형질막을 안정화 시켜, 스트레스에 내성을 갖게 한다고 보고되었다(Guo et al., 2019; Ritonga & Chen, 2020). 또한, 저온과 관련된 cold shock domain, cold responsive protein kinase 등과 관련된 단백질들을 선별하여 유채 2 계통에서 저온 처리에 의한 발현 변화를 비교하였다(Fig. 6c). Cold shock protein 2를 코딩하는 BnaC07g11440D는 ‘EMS 26’에서만 발현이 억제되었으며, cold responsive protein kinase 1인 BnaC05g12740D는 ‘J8634-B-30’에서만 발현이 유도되는 결과를 확인하였다. 두 유전자는 기능이 확실히 보고되지 않았지만, 단백질 도메인 예측 프로그램으로 저온에 반응하는 단백질 관련 도메인을 포함하고 있다고 예측되어, 추후 저온에서 두 유전자의 기능을 더 연구할 필요가 있을 것이다.
마지막으로 저온에 반응하는 기작 중 춘화처리(Vernalization)와 관련된 유전자를 선별하여 두 유채 계통의 DEG 발현을 비교하였다(Fig. 6d). VRN (Vernalization)은 DNA binding 단백질로 식물체의 개화에 관여하며, 밀과 같은 동계작물이 저온에 노출될 때 발현이 유도된다고 보고되었다(Yan et al., 2003; Amasino, 2004). PHD (Histone binding motif) 도메인을 포함하는 VIN3 (Vernalization insensitive)과 VIL (VIN3-like protein)은 FLC (Flowering locus C)을 억제하는 단백질로, 식물의 개화를 억제하고 있는 FLC를 억제함으로써 개화를 유도한다고 보고되었다(Sheldon et al., 1999; Amasino, 2004). VIN3를 코딩하는 BnaA02g08140D와 BnaC02g11530D는 두 유채계통에서 공통적으로 발현이 유도되었으며, FLC 유전자인 BnaA07g13680D에서는 두 계통에서 모두 발현이 감소되는 결과를 확인하였다. 이는 저온에 노출된 두 유채 계통 모두 춘화처리에 반응하여 봄철 개화가 유도되고 있다는 점을 나타낸다.
저온 스트레스에 반응하는 유전자 발현 확인
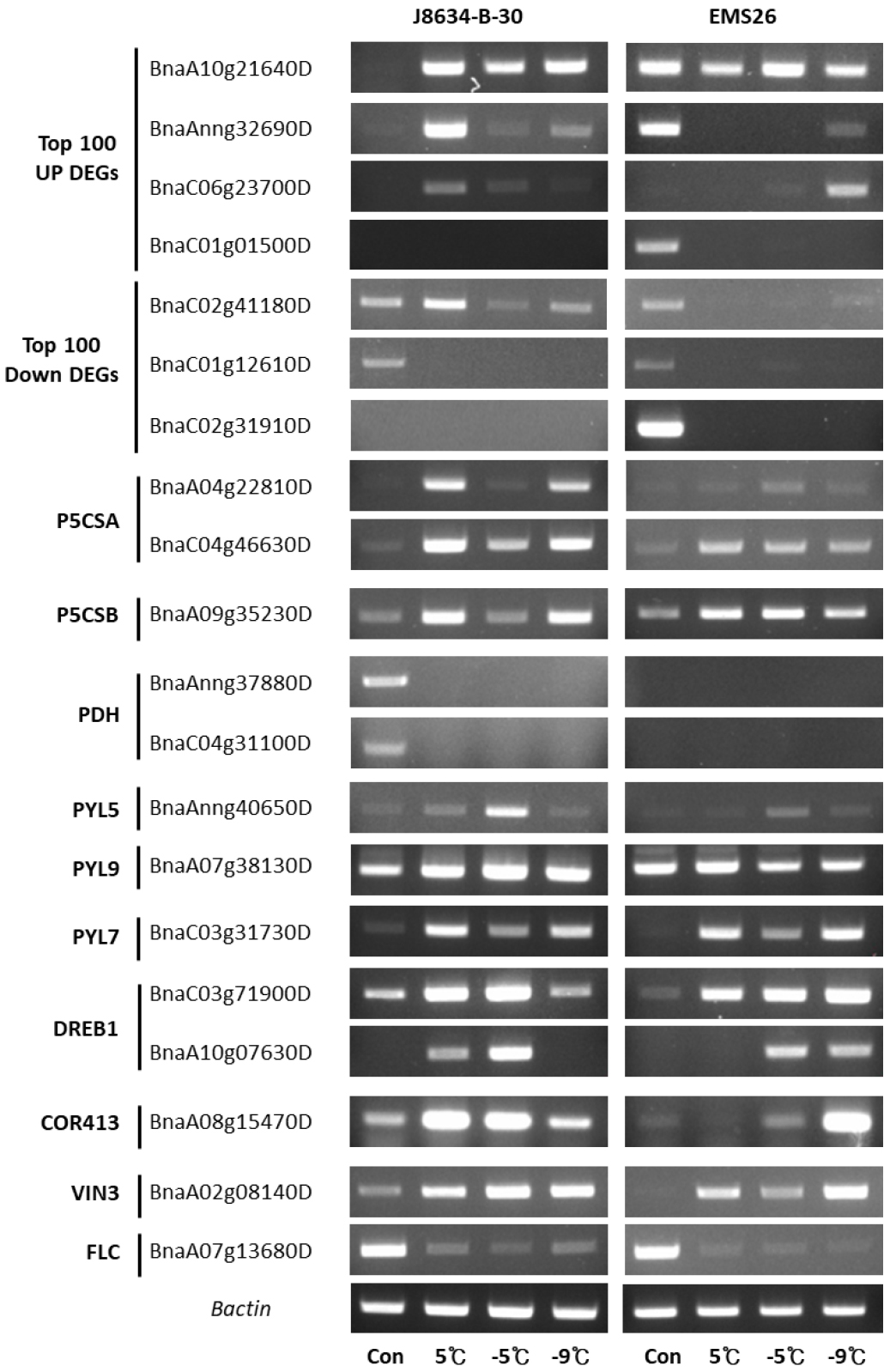
저온 스트레스에 특이적으로 반응하는 주요 DEG들의 발현을 확인하고, 저온 순화 이후 0°C 이하의 저온 스트레스 처리에도 어떠한 발현 변화를 보이는 지 확인하기 위해 RT-PCR을 실시하였다. RT-PCR의 결과는 전사체 분석 결과와 동일하였으며, 이후 0°C 이하의 저온 스트레스 처리에서 몇몇 유전자에서 유채 두 계통간의 발현 변화를 보였다(Fig. 7). DREB1 단백질을 코딩하는 BnaC03g71900D와 BnaA10g07630D, COR413 단백질을 코딩하는 BnaA08g 15470D 유전자의 발현의 경우, 초기 저온순화 과정에서는 ‘J8634-B-30’ 계통에서 강하게 발현하였으나, 이후 -9°C 처리 시 발현이 감소하였다. 반면, ‘EMS26’ 계통에서는 초기 저온순화 과정에서는 발현 변화가 없었으나, -5°C와 -9°C의 스트레스 조건하에서 강하게 발현되는 변화를 확인하였다. 이는 초기 저온순화 시 ‘J8634-B-30’ 계통에서 proline 함량이 높게 확인되고, 초기 생존율이 높은 결과와 일치하며, ‘EMS26’ 계통에서는 후기 생존율이 회복되는 결과와 유사한 것으로 판단된다.
본 연구 결과, 0°C 이하의 저온 스트레스 처리로 인해 유채 두 계통의 생리적 지표 중 proline 함량 및 초기 내동성에서 차이를 확인하였다. 이러한 변화와 관련된 기작을 확인하기 위해 두 유채 계통을 대상으로 전사체 비교 분석을 실시하였으며, 저온스트레스에 반응하는 proline 대사, ABA 호르몬 신호 경로, ICE-CBF-COR 신호 경로, 춘화처리와 관련된 유전자들의 발현을 비교하여 유채 두 계통에서의 발현 차이점을 구명하였다. 이러한 특이적인 발현 양상을 보인 유전자들은 추후 유전자 기능 구명 등을 통해 0°C 이하의 저온 스트레스 피해에 적응할 수 있는 유채 품종 육성 및 관련 기작 연구에 기여할 수 있을 것으로 판단된다.
적 요
본 연구에서는 유채 두 계통에 0°C 이하의 저온 스트레스를 처리하고 이에 따른 proline 함량 및 생존율 변화를 확인하고 이에 따른 저온에서의 유전자 발현 변화를 비교 분석하기 위해 수행되었으며, 결과는 다음과 같다.
1. 0°C 이하의 저온 스트레스 처리 전 저온 순화 후 유채 ‘J8634-B-30’ 계통에서 proline 함량이 2.02 mM/g FW로 증가하여 처리 전보다 8.7배 증가하였으며, ‘EMS26’ 계통에서는 0°C 이하의 저온 스트레스 처리로 인한 proline 함량 변화를 보이지 않았다.
2. 저온 순화 전후 유채 두 계통의 전사체를 분석한 결과, ‘J8634-B-30’ 계통의 DEG는 발현이 유도된 DEG가 2,784개로, 발현이 억제된 DEG 2,299개보다 많았으며, ‘EMS 26’ 계통에서는 발현이 유도된 DEG가 2,199개로 발현이 억제된 DEG 3,632개로 적었다.
3. 저온 스트레스 처리에 의한 유채 두 계통의 상위 100개 DEG를 분석한 결과, ‘J8634-B-30’ 계통에서는 flowering- promoting factor (BnaA10g21640D) 유전자가 강하게 발현되었으며, 특히 proline 생합성 관련 유전자의 발현이 강하게 유도되었다. ‘EMS26’ 계통의 DEG에서는 식물체 생장과 관련된 유전자가 발현이 억제되었다.
4. ‘J8634-B-30’ 계통에서는 proline 생합성 관련 P5CSA (BnaA04g22810D, BnaC04g46630D) 유전자의 발현이 유도되었으며, proline 이화작용 관련 PDH (BnaAnng 37880D, BnaC04g31100D) 유전자 발현이 억제되어, 저온 처리에 의한 proline 함량 이 증가한 것으로 판단된다.
5. 저온 반응 관련 생리반응 경로 유전자 중 ABA 호르몬 수용체 PYL5 (BnaAnng40650D), PYL9 (BnaA07g38130D, BnaC06g17940D)는 ‘J8634-B-30’ 계통에서만 발현이 유도되었다. 또한, ICE-CBF-COR 신호 회로 중 원형질막 안정화에 관여하는 COR413 유전자(BnaA08g15470D, BnaC03g61740D)에서도 ‘J8634-B-30’ 계통에서만 발현이 유도되었다.
6. 이러한 저온 스트레스 반응과 관련된 유전자 발현 차이는 초기 저온 처리 후 두 유채 계통의 스트레스 반응에 관여했을 것으로 판단되며, 특이적인 발현 양상을 보인 유전자에 대해 향후 추가적인 기능을 분석하여 내동성 유채 품종 개발에 활용할 수 있을 것으로 판단된다.