서 론
재료 및 방법
식물 재료 및 생육 조건
대마 칸플라빈 추출
고성능 액체크로마토그래피 분석
‘청삼’ 캘러스 유도 및 직접 기관 발생
아그로박테리움 매개 형질전환
결과 및 고찰
‘청삼’의 칸플라빈 성분 및 함량
‘청삼’의 조직배양 효율
‘청삼’의 아그로박테리움 매개 유전자 발현 효율
적 요
서 론
대마(Cannabis sativa L.)는 삼과(Cannabaceae)에 속하는 주요한 약용 및 특용 작물로, 오랫동안 오일, 종자 식품(헴프씨드), 섬유, 의약품 등 생산에 활용되면서 다양한 산업 분야에서 큰 잠재력을 갖고 전 세계에서 재배되고 있다(Moon et al., 2005; Clarke & Merlin, 2016; Hesami et al., 2020). 최근 대마에서 칸나비노이드 화합물인 Δ-9-테트라하이드로칸나비놀(THC)와 칸나비디올(CBD)의 약리적 효능(항염, 통증 완화, 구토 억제, 신경 보호 등)이 알려지면서 전 세계적으로 의료용 대마의 합법화가 확대되고 있다(Gülck & Møller, 2020). 그러나 한국을 포함하는 일부 국가는 여전히 THC와 같은 화합물의 환각효과와 중독성 문제로 대마의 재배 및 산업적 사용을 엄격하게 제한하고 있다. 한국 재래종과 국외 저 마약형 대마 자원(IH3)의 교잡육종으로 육성된 품종인 ‘청삼(Cheungsam)’은 향정신성 화합물로 알려진 THC가 0.34%, 비향정신성 성분인 칸나비디올(CBD)을 1.34% 함유한 저 마약형 헴프(산업용 대마) 품종으로, 평균적으로 1.74% THC를 함유하는 한국 재래종보다 THC 성분은 현저히 낮고 CBD는 2.3배 많이 함유하고 있다(Moon et al., 2002; 농촌진흥청 농업기술포털(https://www.nongsaro.go.kr/)). 이러한 이유로 저 마약형 ‘청삼’은 주로 섬유(삼베)와 종자(오일, 단백질, 화장품)를 중심으로 산업화를 형성하며 재배가 장려되었다(Park et al., 2012; Jang et al., 2020).
대마에는 칸나비노이드 화합물(≧125개) 외에도, 플라보노이드(≧30개)와 터펜(≧100개) 등 다양한 생리활성 물질이 존재하며 이들 간 상호작용으로 약리학적 효과가 증진(Entourage effect)될 수 있어서 대마의 다른 생리활성 물질에 관한 관심도 증가하고 있다(Christensen et al., 2023). 특히, 대마에서 발견되는 독특한 플라보노이드인 칸플라빈(Cannflavins)은 프레닐화 플라보노이드 계열로 염증 유발 물질인 프로스타글란딘 E2(prostaglandin E2)를 억제하여 아스피린보다 30배 높은 항염증 효과를 가지며, 이외에 항암, 항산화, 신경보호에 대한 약리 효과도 보고되었다(Barrett et al., 1985; Erridge et al., 2020). 비향정신정 화합물인 칸플라빈은 주로 대마 잎과 꽃에서 칸플라빈 A(CFL-A), CFL-B, 그리고 CFL-C 세가지 성분이 검출되었으며, 일반적으로 건조 중량당 0.02% 미만으로 극소량 존재한다(Izzo et al., 2020; Abdel-Kader et al., 2023). 1980년대 초반 칸플라빈의 생리활성이 처음 보고된 이후 의료용 성분으로써 가능성이 제시됨에도 불구하고, 상대적으로 칸나비노이드보다 낮은 함량으로 인하여 칸플라빈의 산업적 활용이나 다양한 대마 유전자원에서 칸플라빈 특성 분석, 칸플라빈 함량을 증가시키기 위한 기술 개발 등에 관한 연구는 제한적으로 이루어져 있다.
오랫동안 산업용 또는 의료용에 적합한 대마 품종을 개발하고자, 섬유 수량 및 품질 향상, 칸나비노이드 함량 조절(저 THC, 고 CBD 함유), 개화 시기 조절 등을 목표로 전통 육종 방법을 통해 수백 종의 다양한 대마 품종이 보고되었다(Salentijn et al., 2015). 최근에는 생명공학 기술이 발전함에 따라 형질전환을 통한 우수 품종 개발을 위한 노력들이 이루어지고 있다. 식물 형질전환 기술 개발에 있어서 조직배양 기술을 이용한 식물체로의 재분화 조건 확립은 필수적이다(Hansen & Wright, 1999). 식물체 재분화를 위한 대표 방법으로는 조직 절편에서 캘러스를 형성하고 식물체를 분화하는 간접 기관 발생(Indirect organogenesis)과 조직 절편에서 직접 잎과 뿌리 같은 새로운 기관을 형성하는 직접 기관 발생(Direct organogenesis)이 있다(Long et al., 2022). 직접 기관 발생 방법은 캘러스 형성 단계를 거치지 않음으로 시간 단축과 함께 체세포 변이를 줄여 식물체의 유전적, 형질적 안정성을 높일 수 있다. 그래서 담배, 대두, 사탕수수, 감귤과 같은 다양한 식물에서 재분화 및 형질전환 기술 개발 연구에 직접 기관 발생 방법이 활용되었다(Horsch et al., 1985; Moore et al., 1992; Paz et al., 2006; Thorat et al., 2018).
대마는 품종 간 변이가 커서 조직배양 기술을 범용적으로 적용하기 어려우며, 성공적인 캘러스 유도와는 다르게 정상적인 신초 형성은 잘 일어나지 않거나 재분화 효율이 매우 낮아 기술 개발에 어려움이 있다. 또한 배지 조성과 식물생장조절제에 의해서도 품종 간 다른 반응으로 인하여 조직배양의 재현성 확보가 어렵다(Wielgus et al., 2008; Monthony et al., 2021). 대마의 조직배양과 형질전환에 대한 저항성으로 기술 개발에 어려움이 있지만, 리포터 유전자(GUS)와 유전자 편집 기술을 적용한 영구적 형질전환의 성공 사례가 보고되었고(Galán-Ávila et al., 2021; Zhang et al., 2021), 대마의 미성숙 배아, 유묘, 조직 절편 등을 이용한 일시적 형질전환 사례들도 보고되고 있다(Sorokin et al., 2020; Jeong et al., 2024; Li et al., 2024; Mohammad et al., 2024). 그러나 아직까지 최적화된 기술로 대마 조직배양 및 형질전환 사례의 반복적인 보고는 제한적이며, ‘청삼’ 품종을 활용한 조직배양으로 형질전환체 개발 또한 보고된 바 없다.
본 연구는 대마 ‘청삼’ 품종에서 칸플라빈 화합물 성분과 함량을 조사하고, 하배축 조직 절편을 이용한 직접 기관 발생 시스템을 확보하였다. 나아가 조직 배양 기술에 아그로박테리움(Agrobacterium tumefaciens) 매개 형질전환 방법을 도입하여 ‘청삼’ 품종에서 외래 유전자 일시발현 효율을 조사하였다. 이를 통해 한국 저 마약형 산업용 대마인 ‘청삼’의 생리활성 화합물인 칸플라빈과 유전형 특이성에 대한 정보를 제공하고, ‘청삼’의 품질 개선을 위한 조직배양과 형질전환 기술을 확립하고자 하였다.
재료 및 방법
식물 재료 및 생육 조건
본 연구는 식품의약품안전처로부터 마약류취급학술연구자 승인하에 수행되었으며, 한국 대마 품종인 ‘청삼’ 종자는 제이헴프코리아(주)에서 구매하여 사용하였다. ‘청삼’ 종자는 혼합상토(배양토:질석, 3:2)에 파종하여 기온 25±1℃, 상대습도 50%, 40,000 Lux의 광세기 조건의 생육 온실에서 단일조건(12시간 광조건:12시간 암조건)으로 재배하였다. 5주 정도 자란 대마 자성식물 상단 약 15 cm 부위의 미수정 암꽃과 잎을 각각 채취한 다음, 60℃의 강제순환건조기에서 4일간 건조시켰다. 건조 조직은 전동분쇄기로 마쇄한 다음 칸플라빈을 추출하기 전까지 4℃ 냉장고에 보관하였다.
유묘는 Sorokin et al.(2020)에 명시된 방법을 일부 수정하여 준비하였다. 종자를 1% (w/v) 과산화수소(H2O2) 용액(MerckⓇ)에 침지한 후 25°C 암조건에서 5일간 배양하며 발아시켰다. 매일 1% H2O2 용액을 교체하였으며, 5일 후 종피를 제거한 유묘는 1% H2O2 용액에 5분 소독하고, 멸균수로 5번 세척하여 1% H2O2 용액을 제거하였다. 표면 살균한 유묘는 1/2 MS 배양 배지[2.2 g/L MS (Duchefa Biochemie), 1.5% (w/v) sucrose (Duchefa Biochemie), 0.35% (w/v) Gelrite (Duchefa Biochemie), pH 5.8]로 옮겨 25°C, 장일조건(16시간 광조건/8시간 암조건) 하에서 추가로 5~7일간 생육시켰다. 이후, 유묘의 자엽, 본엽과 하배축 절편은 캘러스 유도 및 직접 재분화 실험에 사용하였다.
대마 칸플라빈 추출
대마 미수정 암꽃과 잎에 함유된 칸플라빈은 Pellati et al.(2018)에 명시된 방법을 약간 수정하여 추출하였다. 50 mg의 대마 건조 시료에 1 mL의 헥산(Hexane)을 첨가하여 15분간 교반기에서 흔들어주고, 3,500 rpm으로 5분간 원심분리한 다음 상층액을 제거하였다. 이 과정을 각각 1 mL과 0.5 mL의 헥산으로 반복하여 수행하였다. 대마 시료를 여과지에 올려 상온에서 건조시키고, 건조한 시료에 아세톤(Acetone)을 첨가하여 칸플라빈을 추출하였다. 시료에 1 mL의 아세톤을 첨가하여 15분간 흔들어주고 3,500 rpm으로 5분간 원심분리한 다음, 상등액을 새로운 튜브에 옮겨 담았다. 이 과정을 각각 1 mL과 0.5 mL의 아세톤으로 반복하고 상등액을 합친 용액(2.5 mL)을 진공 농축기(30℃)에서 농축시켰다. 농축된 칸플라빈 추출물은 다시 0.2 mL의 아세톤에 녹이고 0.45 ㎛ PTFE 필터로 추출물을 여과하고 10 μL를 고성능 액체크로마토그래피(HPLC) 분석에 사용하였다.
고성능 액체크로마토그래피 분석
HPLC 분석은 LC-20A HPLC system (Shimadzu, Koyto, Japan)으로 수행하였으며, Symmetry C18 column (4.6 mm × 250 mm, I.D., 5 µm, Waters, MA, USA)를 사용하였다. 이동상 용액은 water (0.1% formic acid, A)와 acetonitrile (0.1% formic acid, B)를 사용했으며, 분석 조건은 다음과 같다. 0~5분 40% B, 5~20분 40%에서 80% B, 20~35분 80%에서 90% B, 35~40분 90% B, 40~42분 90%에서 40% B, 그리고 40% B로 5분 동안 추가로 유지하였다. 1 mL/min 유속으로 컬럼 온도는 30℃로 설정하였다. UV/ DAD 검출 범위는 190~800 nm로 지정하였으며, 크로마토그램은 342 nm에서 확인하였다. 칸플라빈 화합물은 크로마토그래프에서 각각 표준물질의 검출 시간 및 UV 스펙트라와 비교하여 규명하였다.
‘청삼’ 캘러스 유도 및 직접 기관 발생
‘청삼’ 유묘(5일생)의 본엽(true leaf), 자엽(cotyledon), 하배축(hypocotyl) 절편을 캘러스 유도 실험의 시료로 사용하였다. 조직 절편은 Zhang et al.(2021)이 제시한 캘러스 유도 배지[4.4 g/L MS, 1 mg/L 니코틴산(nicotinic acid, Duchefa Biochemie), 1 mg/L 피리독신-HCl (pyridoxine-HCl, Duchefa Biochemie), 10 mg/L 티아민-HCl (thiamine-HCl, Duchefa Biochemie), 0.1 g/L 미오이노시톨(myo-inositol, Duchefa Biochemie), 3% (w/v) sucrose, 0.25% (w/v) Phytagel (Duchefa Biochemie), 1 mg/L 2,4-D (Duchefa Biochemie), 0.25 mg/L 키네틴(kinetin, Duchefa Biochemie), 100 mg/L 카제인 가수분해물(casein hydrolysate, MB cell), pH 5.6]에서 25°C, 장일 조건으로 28일간 배양하였다. 28일 배양 후, 조직 절편에 따른 캘러스 형성률을 계산하였다.
하배축 유래 직접 기관 발생 실험에는 7일생 ‘청삼’ 유묘를 사용하였으며, 유묘의 자엽 바로 아래 부위를 직경 약 0.3~ 0.7 cm 크기로 절단하여 하배축 절편을 준비하였다. 그리고 하배축 절편을 식물 생장 조절제[1 mg/L zeatin riboside (ZEARIB, Duchefa Biochemie) 및 0.02 mg/L α-naphthaleneacetic acid (NAA, Duchefa Biochemie)]가 포함된 또는 포함되지 않은 1/2 MS 고체 배지에 치상하였다(Galán- Ávila et al., 2020). 그리고 25°C에서 14일간 배양한 후, 신초 및 뿌리 형성률을 조사하였다.
아그로박테리움 매개 형질전환
표지 유전자인 RUBY (Addgene, plasmis #160908)를 이용하여 ‘청삼’에서 유전자 발현 효율을 조사하였다. 아그로박테리움 LBA4404, GV3101, AGL1 균주에 35S:RUBY 플라스미드 DNA를 형질전환 시킨 다음, Sorokin et al.(2020)에 보고된 방법을 이용하여 아그로형질주입(Agroinfiltration)에 따른 RUBY 유전자 발현 효율을 조사하였다. RUBY 유전자를 포함하는 아그로박테리움 세포를 YEP 배지에 접종하고 28°C에서 220 rpm으로 16시간 이상 배양시켰다. 아그로박테리움 셀은 원심분리를 통해 침전시키고, 상등액을 제거한 다음 3 mL의 10 mM MgSO4로 침전물을 용해시켰다. 이를 3번 반복한 다음 원심분리 후에 상등액을 제거하였다. 그리고 MS 액체 배지(4.43 g MS, 10 g sucrose, 500 mg MES, pH 5.7)로 아그로박테리움 셀 농도가 0.6(OD600)이 되도록 만들고 100 μM acetosyringone을 첨가하였다. Acetosyringone을 첨가한 30mL MS 액체배지에 1% H2O2 용액에서 자엽과 2개의 본엽이 형성된 유묘를 넣고 20분 진공(600 mm Hg)처리 하였다. 유묘는 멸균한 filter paper로 옮겨서 아그로박테리움 셀을 제거한 다음, MS 고체 배지(4.43 g MS, 8 g agar, pH 5.7)로 옮기고 25°C 암조건으로 3일간 공동 배양시켰다. 그리고 3일 후에 명조건에서 식물의 변화를 관찰하였다.
하배축 절편에 아그로박테리움 매개 유전자 형질전환을 시도하기 위하여, 35S:RUBY 플라스미드 DNA에 포함된 식물 선발 마커인 하이그로마이신(Hygromycin) 저항성 유전자 발현 카세트(NOSpro:Hyg:NOSter)를 HindIII/SalI 제한효소로 절단하여 제거하고, 카나마이신(Kanamycin) 저항성 유전자 발현 카세트(NOSpro:Kan:NOSter)를 삽입시켰다(RUBY_kan). RUBY_kan 플라스미드 DNA를 포함하는 AGL1 아그로박테리움 셀을 접종 배지[2.5% (w/v) LB, 0.05 g/L spectinomycin, 0.0392 g/L acetosyringone]에 희석하여 OD600=0.5의 농도로 조정한 후, 하배축 절편과 함께 암조건에서 40분 동안 배양하여 공동 감염을 유도하였다(Galán-Ávila et al., 2021). 이후, 감염된 하배축 절편을 공동 배양 고체 배지(1/2 MS, 1.5 % sucrose, 0.0392 g/L acetosyringone, 3.5 g/L gelrite) 위에 치상한 뒤, 암조건(25°C)에서 4일간 배양하였다. 4일 후, 감염된 절편을 멸균 증류수로 세 번 세척하고 cefotaxime (0.25 g/L)과 carbenecillin (0.25 g/L)이 포함된 30 mL 혼합 용액으로 추가 세척하였다. 세척한 하배축 절편을 선발 고체 배지(CCK; 0.25 g/L cefotaxime, 0.25 g/L carbenecillin, 0.1 g/L kanamycin, 3.5 g/L gelrite) 위에 치상한 뒤, 생육 조건(25°C, 장일 조건)에서 배양하였다. CCK 배지에서 14일 후 생존한 카나마이신 저항성 식물체들을 새로운 CCK 배지가 포함된 마젠타 박스로 옮겼다. 마젠타 박스에서 약 11~17일간 배양한 후, 식물체를 흙으로 이식하였으며, 25°C의 단일조건에서 배양하였다. 흙으로 이식한 뒤 약 26~31일 경과 후 자성 식물과 웅성 식물의 교배를 통해 종자를 확보하였다.
결과 및 고찰
‘청삼’의 칸플라빈 성분 및 함량
‘청삼’에서 대마의 주요 생리활성 물질로 알려진 칸나비노이드 화합물인 Δ9-Tetrahydrocannabinol (THC)과 Cannabidiol (CBD)의 함량은 보고되었지만(Moon et al., 2002), 대마 특이적 프레닐화 플라보노이드로 알려진 칸플라빈에 대해서는 아직까지 보고된 바 없다. ‘청삼’의 칸플라빈 특성을 자세히 이해하고자 생육 온실에서 5주 재배한 ‘청삼’ 자성식물의 미수정 암꽃과 잎에서 칸플라빈을 추출하고 이를 HPLC로 분석함으로써 칸플라빈 화합물의 종류별 함량을 조사하였다. ‘청삼’에서는 칸플라빈 A (CFL-A)와 CFL-B가 342 nm에서 각각 25.87분과 19.77분에 검출되었으며, 3개의 최대 흡수 파장대(UV λmax, CFL-A=221, 274, 341 nm, CFL-B=217, 274, 342 nm)가 확인되었다(Fig. 1A, Table 1). ‘청삼’ 미수정 암꽃에서 CFL-A와 CFL-B가 각각 105.2 μg/g (건중량)과 26.2 μg/g(건중량) 검출되었으며, 잎에서는 CFL-A와 CFL-B가 각각 31.8 μg/g(건중량)과 5.6 μg/g(건중량) 확인되었다(Fig. 1B). 식물 종과 조직별로 플라보노이드가 다양하게 존재한다는 사실과 유사하게 청삼 미수정 암꽃에 잎보다 약 3.5배 많은 칸플라빈이 축적되어 있음을 보여준다(Fig. 1B). 그리고 동일한 추출법으로 분석된 국외 대마 자원의 화서(inflorescence)에서 CFL-A가 59.9~163.4 μg/g, CFL-B는 21~100.9 μg/g 가량 존재한다는 기존 문헌처럼(Pellati et al., 2018), ‘청삼’ 미수정 암꽃에서도 CFL-A가 주요 성분으로 관찰되었으며 건중량당 0.015% 이하로 매우 소량 존재함을 확인하였다. 이는 중요한 생리활성을 보이는 칸플라빈의 함량을 증진시키기 위한 기술 개발이 필요함을 시사하는 바이다.
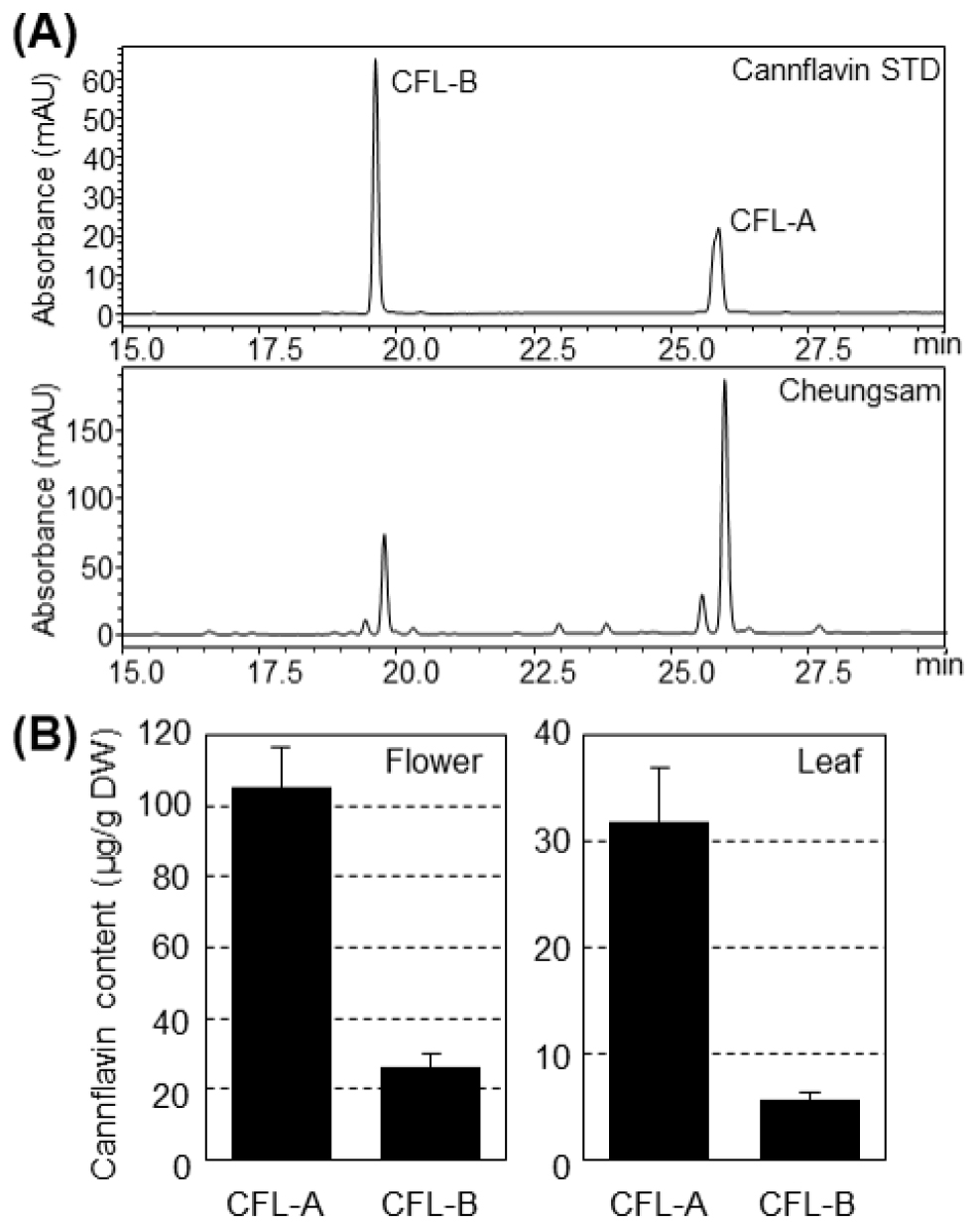
Fig. 1.
Cannflavin contents in immature inflorescences and leaves of Cannabis sativa cv. ‘Cheungsam’. (A) High- performance liquid chromatography (HPLC) chromatograms of cannflavin extracts from immature inflorescences. CFL-A, cannflavin A; CFL-B, cannflavin B. (B) Total contents of cannflavins in immature inflorescences (flowers) and leaves. Chemical extracts were prepared from six independent plants. Bars indicate standard deviation (SD) based on two replicates for immature inflorescences and three replicates for leaves.
Table 1.
Retention times and UV spectra of cannflavin A and cannflavin B.
| Chemicals | Compound | Chemical Formula | Rt (min) | UV λmax (nm) |
| Cannflavins | CFL-A | C26H28O6 | 25.87 | 221, 274, 341 |
| CFL-B | C21H20O6 | 19.77 | 217, 274, 342 |
‘청삼’의 조직배양 효율
‘청삼’의 캘러스 형성률 및 이를 통한 식물 재분화 조건을 탐색하기 위하여 ‘청삼’ 유묘의 본엽, 자엽, 하배축 절편으로부터 캘러스 형성률을 조사하였다. ‘청삼’ 종자를 1% (v/v) 과산화수소(H2O2) 용액에서 4일간 발아시킨 후, 유묘를 조직배양 배지로 옮겨 5일간 배양하였다(Fig. 2A, B). H2O2는 항균제로 작용할 뿐만 아니라 식물 생리학적으로 신호전달 분자로도 작용하며, 최근 연구에서는 대마의 종자 발아율을 향상시킬 수 있음이 보고된 바 있다(Wojtyla et al., 2016; Sorokin et al., 2020). 본엽이 전개된 유묘에서 잎, 자엽, 하배축을 절단하여 캘러스 유도 배지에서 배양하였다(Fig. 2C~E). 이후 28일간 배양하여 조직절편으로부터 캘러스 형성률을 조사한 결과, 자엽에서 94.2%, 하배축에서 86.7%, 잎에서는 96.7%의 캘러스 형성률을 보였으며(Table 2, Fig. 2F~H), 시료 간 유의적인 차이는 없었다. ‘청삼’ 조직 절편으로부터 형성된 캘러스는 녹색, 노랑 그리고 하얀색으로 다양한 형태가 관찰되었다. 비록 실험에서 사용한 조직 절편 모두 캘러스는 성공적으로 유도되었지만, 캘러스를 재분화 배지로 옮겨 신초(shoot) 형성을 유도하는 과정에서 식물체 재분화는 관찰되지 않았다. 이는 본 연구에서 사용한 재분화 배지 조건에서 ‘Yunma7’ 헴프 자원이 성공적으로 신초를 형성했다는 연구 결과(Zhang et al., 2021)와는 다르게 ‘청삼’은 캘러스로부터의 신초 형성 능력이 낮은 유전적 특성을 보유하거나, 재분화 배지에 포함된 생장조절제(TDZ와 NAA)의 조합이 ‘청삼’ 유래 캘러스의 조직 재분화에 적합하지 않을 수 있음을 의미한다. 캘러스 유도 및 식물 재분화에는 시료 간 이질성이 크며, 유전적 특성과 생장조절제의 농도와 비율, 환경 조건 등에 의해서 큰 영향을 받는다(Lata et al., 2010a; Lata et al., 2010b; Galán-Ávila et al., 2020; Hesami & Jones, 2021; Monthony et al., 2021). 최근 TDZ (1 mg/L)와 NAA (0.5~2 mg/L)를 포함한 MS 배지에서 ‘청삼’ 본엽과 자엽 조직 절편으로부터 유도한 캘러스를 TDZ (0.5~10 mg/L)만 함유한 MS 배지에 배양한 결과 ~22.7% 신초가 형성되었다는 결과(Ahsan et al., 2024)가 식물 재분화에 생장조절제 농도의 중요성을 뒷받침해준다. 지금까지 다양한 연구에서 대마 조직 재분화 연구가 보고되었지만, 낮은 재분화 효율뿐만 아니라 재분화에 대한 대마 자원의 저항성, 유전자형 및 조직 특이적 반응, 그리고 문헌에서 성공적인 프로토콜의 재현성 부족 등의 문제가 제시되고 있다(Monthony et al., 2021). 예를 들어, Mandolino & Ranalli(1999)에서는 12가지 상업용 대마 품종의 4가지 조직(잎, 하배축, 자엽, 뿌리) 절편으로부터 성공적으로 캘러스를 유도하였음에도 불구하고, 오직 한개 품종에서만 낮은 빈도로 신초가 형성되었다. 또한 대마 품종과 조직의 재분화 효율을 비교한 다른 연구 결과에서도 명확한 답은 확인할 수 없었다(Ślusarkiewicz-Jarzina et al., 2005; Wielgus et al., 2008). 이는 ‘청삼’에 최적화된 재분화 방법 확립, 재현성과 효율 증진을 위한 추가 연구가 필요함을 의미한다.
Table 2.
Effect of explant type on callus induction efficiency in ‘Cheungsam’. Callus induction rates were evaluated for cotyledon, hypocotyl, and leaf explants after 28 days of culture on callus induction medium.
| Explant |
Callus formation frequency (%)1) | n | Significance2) |
| Cotyledon | 94.15 ± 1.44 | 71 | a |
| Hypocotyl | 86.67 ± 13.36 | 32 | a |
| Leaf | 96.68 ± 1.67 | 67 | a |

Fig. 2.
Callus induction from different explants of Cannabis sativa cv. ‘Cheungsam’. (A) Dry seeds. (B) Seedlings cultured on tissue culture medium for 5 days after germination. Freshly dissected (C) leaves, (D) cotyledons, and (E) hypocotyls from 5-day-old seedlings. Callus formation from (F) leaves, (G) cotyledons, and (H) hypocotyls after 28 days on callus induction medium.
‘청삼’의 조직배양 기술을 확립하기 위한 다른 방법으로 조직 절편에서 캘러스 유도를 하지 않고 직접 신초 기관 형성(direct shoot organogenesis)을 촉진시키는 직접 기관 발생 방법을 시도하였다. 대마 하배축에서 약 49.5%로 높은 신초 형성률이 보고된 연구 결과(Galán-Ávila et al., 2020)를 바탕으로 ‘청삼’의 하배축을 이용한 신초 형성 조직 재분화 효율을 조사하였다. ‘청삼’ 7일생 유묘의 하배축을 절단하여 생장조절제가 없는 배지에 치상하고 7일이 지난 이후에 1~2개의 신초가 형성되었으며(Fig. 3A, B), 14일 이후에는 자발적인 뿌리 형성이 관찰되었다(Fig. 3C). 이러한 신초와 뿌리 형성은 생장조절제인 ZEARIB (1 mg/L)과 NAA (0.02 mg/L)가 포함된 배지에서도 유사하게 관찰되었다(Fig. 4). 신초 형성률과 신초 개수는 생장조절제 유무에 크게 영향을 받지 않았지만, 자발적 뿌리 형성률은 생장조절제가 포함된 배지에서는 13.7%, 포함되지 않은 배지에서는 43.8%로 유의한 차이를 보였다(Table 3). 이는 다른 식물 종인 파프리카(Capsicum annumm L., bell pepper)와 시계꽃(Passiflora setacea D.C.)에서도 무호르몬 조건에서 하배축 유래 식물체의 재분화 및 자발적 뿌리 형성이 관찰된 결과와 유사하게(Ezura et al., 1993; Vieira et al., 2014), ‘청삼’에서도 무호르몬 배지에서 자발적 뿌리형성이 촉진되었다. 이는 식물 내부에서 생성되는 옥신이 이러한 생장을 유도할 수 있음을 시사한다. 하배축으로부터 재생된 식물체는 21일 후 안정적인 뿌리 발달과 함께 정상적인 잎 형성과 줄기 신장을 보였으며(Fig. 3D), 이후 토양 화분으로 옮겨 순화시켰다. 순화 21일(배양 시작 후 50일) 후에 재분화된 식물에서 정상적인 성장과 발달이 관찰되었으며(Fig. 3E), 약 10주 후에는 웅성 식물과 교배를 통해서 종자를 확보할 수 있었다(Fig. 3F, G). 반면, 생장조절제 배지에서 재분화된 식물체는 뿌리 형성은 유도되었으나, 토양 순화시 줄기와 뿌리가 더 이상 자라지 못하고 식물 성장이 멈추었다(Fig. 4D). 식물 생장조절제 중 시토키닌과 옥신은 신초 및 뿌리 분화를 조절하며, 이들의 균형은 세포 분열 및 분화를 조절한다(Chapman & Estelle, 2009; Li et al., 2021). 또한 과도한 시토키닌은 비정상 생장을 유도할 수 있으며, 옥신 신호가 억제되면 세포 분열이 저해된다. 이는 ‘청삼’ 하배축을 이용한 직접 기관 발생에서는 시토키닌과 옥신의 첨가가 내생 호르몬 분포에 영향을 주었을 수 있으며, 최종적으로 줄기 신장 및 뿌리 형성에 중요하게 관여했을 수 있음을 시사한다.

Fig. 3.
Developmental stages of direct in vitro plant regeneration from hypocotyl explants of ‘Cheungsam’ without plant growth regulators. (A) Hypocotyl explants dissected from 7-day-old seedlings. (B) Vigorous shoot induction at the upper part of hypocotyl explants after 7 days of culture. (C) Root emergence from the lower part of hypocotyl explants after 14 days. (D) Diverse root morphologies in hypocotyl-derived plants after 21 days (red arrow). (E) Acclimation of hypocotyl-derived plant to external conditions after 50 days. (F) Fertilized female plant regenerated from hypocotyl explants, showing sexual functionality at 69 days (in vitro inoculation; red arrow indicates seed pods). (G) Mature seeds harvested from the regenerated plant.

Fig. 4.
Developmental stages of direct in vitro plant regeneration from hypocotyl explants of ‘Cheungsam’ with plant growth regulators. (A) Newly dissected hypocotyl explants from 7-day-old seedlings. (B) Shoot development at the upper part of hypocotyl explants after 7 days of culture with plant growth regulators. (C) Spontaneous root formation at the lower part of hypocotyl explants after 14 days. (D) Hypocotyl-derived plant exposed to external humidity, showing failure to acclimate 36 days after culture initiation.
Table 3.
Comparative analysis of medium composition on direct in vitro regeneration from hypocotyl explants of ‘Cheungsam’. Regeneration efficiency was evaluated after 14 days of culture in media with or without specific growth regulators. The table presents the mean percentage (± standard error, SE) of responding explants, the number of shoots per responding explant (± SE), and spontaneous rooting frequency (± SE), with significance and sample number (n) shown in separate columns.
|
Medium (mg/L) |
Responding explants (%) | n |
Signifi- cance1) |
Shoots per Responding explant (n) | n |
Signifi- cance cance1) |
Spontaneous rooting frequency (%) | n |
Signifi- cance cance1) |
|
Without Plant growth regulators | 61.39 ± 5.9 | 151 | a | 1.08 ± 0.02 | 91 | a | 43.80 ± 7.73 | 41 | a |
|
ZEARIB 1 + NAA 0.02 | 58.77 ± 2.31 | 174 | a | 1.19 ± 0.04 | 102 | a | 13.73 ± 4.9 | 14 | b |
‘청삼’의 아그로박테리움 매개 유전자 발현 효율
앞서 확보한 ‘청삼’ 하배축 유래 직접 기관 발생 방법을 이용하여 형질전환 기술을 확립하고자 아그로박테리움 매개 형질전환을 수행하였다. 식물 형질전환 빈도는 아그로박테리움 종류에 따라 차이가 날 수 있으므로, 표지 유전자를 포함하는 아그로박테리움 LBA4404, GV3101, AGL1 균주를 ‘청삼’ 유묘에 감염시키고 표지 유전자 발현 효율을 조사하였다. 이때 사용한 표지 유전자는 RUBY로 타이로신(Tyrosine)을 베탈레인(Betalain) 색소로 전환하는 3가지 효소[P450 oxygenase CYP76AD1, L-DOPA (L-3,4-dihydroxyphenylalanine) 4,5-dioxygenase (DODA), glucosyltransferase]들의 공동 발현을 통해 축적된 빨간색 베탈레인으로 유전자 발현 여부를 육안으로 확인할 수 있다(He et al., 2020). 본 연구에서 사용한 3종류 아그로박테리움에 의해 ‘청삼’ 유묘에서 베탈레인 축적이 관찰되었지만, ‘청삼’에 가장 효율적인 균주는 AGL1으로 54.2% 형질전환 효율이 확인되었다(Fig. 5). 이는 국외 헴프 자원인 ‘Yunma 7’과 마리화나 계열 대마 ‘Galaxy CBD’에서도 AGL1 균주가 54~56% 높은 형질전환 효율을 보인 결과와 일치한다(Li et al., 2024). 국외 2 자원에서는 아그로박테리움 일시발현 방법으로 LBA4404 균주(42~46%)도 ‘청삼’보다 높은 형질전환 효율을 보였지만, GV3101과 EHA105은 2% 이하로 매우 낮은 형질전환 효율을 보였다. 이와는 반대로 ‘Pink Kush’ 품종 잎 절편에 GV3101과 EHA105균주를 접종하고 유도한 캘러스에서는 EHA105가 40%로 GV3101에 비해 2.2배 더 높은 형질전환 효율이 보고되었다(Holmes & Punja, 2023). 결국, 대마 형질전환을 위한 아그로박테리움균주 효율은 시험에 사용하는 대마 품종, 식물 조직 절편, 그리고 형질전환 방법에 따라 달라질 수 있으므로, 시험 조건에 적합한 아그로박테리움균주를 선발하는 것이 중요함을 시사한다.

Fig. 5.
Transient expression efficiency of the RUBY reporter gene in ‘Cheungsam’ seedlings using different Agrobacterium strains. Eight-day-old seedlings were infiltrated with Agrobacterium strains LBA4404, GV3101, or AGL1 carrying the RUBY reporter construct. Bacterial suspensions were prepared in liquid MS medium, and seedlings were vacuum-infiltrated for 20 min, transferred to solid MS medium, and incubated for 3 days at 25℃ in the dark. Seedlings were then transferred to light conditions and examined for RUBY expression 3 days later.
‘청삼’ 하배축 절편에 RUBY를 포함하는 아그로박테리움 AGL1 균주를 감염시키고, 항생제(Kanamycin) 선발 배지에 치상하여 직접 기관 발생을 통한 조직 재분화 과정에서 유전자 발현 효율을 관찰하였다. 항생제 선발 배지 치상 5일 후에 일부 하배축에서 직접 신초와 뿌리가 형성되었으며, 하배축 절편 외피, 양 끝부분과 관다발 조직 부위에서 베탈레인 축적이 확인되기 시작하였다. 흥미롭게도 ‘청삼’ 하배축 유래 신초와 뿌리가 형성되는 일부분에서만 국한되어 붉은 점처럼 베탈레인 축적이 나타났다(Fig. 6A). 선발된 하배축 유래 신초 혹은 뿌리를 형성한 식물체를 토양에 순화시키기 전에 베탈레인 축적 효율을 조사한 결과, 276개 하배축 절편으로부터 신초 혹은 뿌리를 형성한 132개의 절편에서 베탈레인 축적이 관찰되었다(49.2% ± 11.7%). 이후 상토 순화에 성공한 25개 식물 개체 중에서 19개에서만 베탈레인 축적이 확인됨을 통해서(Fig. 6B), 본 연구에서 사용한 하배축 절편(276개) 유래 유전자 형질전환 효율은 6.9%로 ‘청삼’ 하배축 절편을 활용한 형질전환이 가능함을 보여준다. 최종적으로 형질전환체로 선발된 식물에서 관찰된 베탈레인 축적은 대부분 하배축에서 뿌리가 형성되는 부위나 뿌리 일부분에 점처럼 국소적으로 나타났으며, 오직 한 개체에서만 뿌리 전반적인 베탈레인 축적이 관찰되었다(Fig. 6B). 또한 개체마다 신초 혹은 뿌리 형성 초기에 베탈레인 축적이 관찰된 부위와 발현이 일관되게 유지되지는 않았다. RUBY 유전자를 리포터 시스템으로 다른 작물에서 유전자 형질전환을 조사한 기존 보고들에 의하면, 대나무 잎에서는 아그로박테리움 감염 초기에 관찰되었던 베탈레인 축적이 시간이 지날수록 사라짐이 확인되었다(Sun et al., 2023). 또한 담배, 토마토, 대두에서는 PCR 분석으로 RUBY 유전자 삽입이 확인됨에도 불구하고 베탈레인 축적은 감염 초기에 캘러스나 조직 절편에서 붉은 점처럼 관찰되다가 새싹이 형성되면서 희미해졌으며, 성숙한 잎에서는 발현이 희미하거나 꽃에서는 강하게 축적되는 등 조직과 발달 단계에 따라 발현 패턴이 균일하지 않음이 보고되었다(Kshetry et al., 2025). 이는 RUBY 유전자를 포함하는 T-DNA가 염색체에 안정적으로 삽입되지 못하였거나 일부 세포에만 T-DNA가 도입되어 국소적으로 나타나는 현상으로 설명되고 있다. 그리고 아그로박테리움 감염 시간이 지남에 따라 도입된 T-DNA가 제거되었을 수도 있다고 해석되고 있다. 이를 바탕으로 연구자들은 RUBY가 일시적으로 유전자 발현을 확인하기에 적합한 단기 리포터 시스템임을 주장하고 있다. 본 연구에서도 최종 확보한 19개 ‘청삼’ 형질전환체 잎과 뿌리에서 PCR 분석으로 RUBY의 삽입이 확인됨에도 불구하고 베탈레인 축적이 균일하지 않았으며 형질전환체 교배를 통한 세대 진전에서 RUBY 유전자가 전이되지 않음을 확인함으로 위 주장을 뒷받침한다.

Fig. 6.
Accumulation patterns of betalain in hypocotyl explants of ‘Cheungsam’. Hypocotyl explants (prepared as in Fig. 3) were infected with Agrobacterium AGL1 carrying the RUBY gene and cultured on selection medium for ~1 month. Transformation efficiency was assessed by betalain accumulation as a marker of RUBY expression in hypocotyl-derived shoots or roots. Betalain accumulation was also examined in plants prior to soil acclimatization (A) and after 3 weeks of soil growth following acclimatization (B) Arrows indicate regions of betalain accumulation.
적 요
국내 대표 저 마약형 헴프 ‘청삼’은 섬유와 종자 산업의 주요한 자원으로 사용되고 있음에도 불구하고, 법적 규제로 인하여 기초적인 특성 분석 및 형질전환 연구는 매우 제한적이다. 본 연구에서는 ‘청삼’의 약리학적 생리활성 물질로 알려진 칸플라빈 함량을 분석하고, 식물 형질전환 기술 개발에 필요한 조직배양과 형질전환 체계 확립을 통한 유전자 일시발현 효율을 조사하고자 하였다.
1.‘청삼’ 미수정 암꽃과 성숙한 잎에서는 CFL-A와 CFL-B가 주요 성분으로 검출되었으며, 미수정 암꽃에서 CFL-A와 CFL-B 함량이 각각 105.2 μg/g(건중량)과 26.2 μg/g (건중량)으로 잎보다 3.3∼4.6배 많이 존재하였다.
2.‘청삼’ 유묘의 잎, 자엽, 하배축 절편에서 86.7~96.7%의 높은 캘러스 형성률이 관찰되었으나, 신초 재분화는 불가능하였다. 그러나 하배축 조직 절편으로부터 직접 신초와 뿌리 형성에 성공하고, 토양 순화 및 생육 후에 종자 확보까지 완료함으로써 직접 기관 발생 방법으로 캘러스 유도 없이 재분화가 가능한 조직배양 기술을 확립하였다.
3.아그로박테리움 매개 일시발현의 경우, ‘청삼’에서 아그로박테리움 균주 AGL1이 가장 높은 형질전환 효율(54.2%)을 보였다. 직접 기관 발생 방법을 활용한 아그로박테리움 매개 형질전환을 ‘청삼’에 시도한 결과, 형질전환 식물체에서 RUBY 리포터 유전자 발현으로 인한 붉은색 베탈레인 축적이 관찰되었다. 특히 베탈레인이 일부 조직에 국소적으로 발현되거나 균일하지 않음을 통해서 ‘청삼’에서도 RUBY 시스템은 단기 일시발현 확인에 적합함을 알 수 있었다. 이는 ‘청삼’ 품종에서도 아그로박테리움을 이용한 유전자 발현이 가능함을 확인한 결과로, 향후 안정적 형질전환 기술 확립을 위한 기초 자료로 활용될 수 있다.
4.종합적으로, 본 연구에서 확립된 직접 기관 발생 기반 형질전환 기술은 ‘청삼’을 포함한 다양한 대마 자원에서 일시적 유전자 발현을 통한 유전자 기능 분석과 대사공학적 품질 개선(저THC·고CBD 품종, 기능성 이차대사물질 함량 증진, 스트레스 내성 강화, 종자 생산량 증진, 조직배양·형질전환 효율 개선 등) 연구의 기반으로 활용될 수 있다. 또한, 향후 산업용 헴프 품종의 기능성 강화, 의약·화장품·바이오소재 개발 등 고부가가치 산업 응용에도 기여할 수 있을 것으로 기대된다.




