서 론
재료 및 방법
시험 재료 및 탈지 조건
수분함량, 조단백질, 회분, 조지방 및 탄수화물 함량
아미노산 분석
단백질 품질 분석
통계 분석
결과 및 고찰
작물 및 품종별 영양성분
작목 및 품종별 오메가-3 지방산 함량
작물 및 품종별 아미노산 조성
단백질 품질 평가
적 요
서 론
한국의 고령화율은 2017년 14.0%, 2022년 17.5%에서 2025년 65세 인구가 전체 인구의 20.3%를 차지하는 초고령 사회에 진입했다(Statistics Korea, 2023). 이는 2017년 고령사회에 진입한지 7년만으로 고령화 속도는 전세계에 유례없이 빠른 것으로 알려져 있다. 이러한 고령화율은 2070년에는 46.4%에 이를 것으로 예상되며, 기대수명 증가(83.5세)와 함께 노년부양비도 지속적으로 상승하여 2065년에는 생산 가능인구 1명이 노년 1명을 부양해야 하는 수준(100.4%)에 도달할 것으로 전망된다. 이러한 변화는 고령층의 의료비 증가와 생산가능인구의 부담 가중으로 향후 막대한 사회·경제적 부담으로 이어질 것으로 예상하고 있어, 이에 대한 국가적 대응이 시급한 실정이다.
고령화 사회에서 특히 주목해야 할 건강 문제 중 하나는 근감소증(Sarcopenia)이다. 근감소증은 노화에 따라 근육량과 근력이 감소하고 근육 기능이 저하되는 질환으로, 삶의 질 저하뿐 아니라 낙상, 골절, 당뇨병, 심혈관 질환 및 인지기능 저하 등 2차 합병증을 유발하여 사망률을 높이는 주요 원인으로 지목되고 있다(Choi & Kim, 2024, Hong & Choi, 2012). 국내 조사에 따르면, 65세 이상 노인의 약 42.8%가 근감소증에 해당하며, 40~64세 중장년층에서도 약 29.5%가 관련 증상을 보이는 것으로 보고되었다(질병관리청, 국민건강영양조사 제4-5기). 이에 따라 2021년 보건복지부는 노인성 질환인 근감소증을 제8차 한국표준 질병사인분류에 진단코드(M62.5)를 부여하여 정식 질병으로 인정하였다. 그러나 현재까지 근감소증에 대한 치료제는 없어, 예방 중심의 관리가 더욱 중요한 질병으로 알려져 있다.
근감소증의 발병 원인으로는 세포노화, 염증 유발 사이토카인, 미토콘드리아 기능 부전, 호르몬 불균형. 단백질 섭취 부족, 운동 부족 등이 복합적으로 작용하는 것으로 알려져 있다(Cho & Song, 2022; Huang et al., 2025; Nasso et al., 2024). 이러한 근감소증 예방을 위해서는 단백질 보충과 운동이 매우 중요하다. 이에 따라 근감소증 예방을 위해 65세 이상 노인의 단백질 1일 권장 섭취량이 체중 1 kg 당 1.2 g으로 일반성인(체중 1 kg 당 하루 0.9 g)의 단백질 섭취권장량 보다 높으나, 실제 고령층은 저작, 소화 기능 저하 등으로 인해 단백질 권장량보다 적은 단백질을 섭취하는 것으로 보고되고 있다(Bauer et al., 2013; Jang & Ryu, 2020; Park, 2018).
따라서 근감소증 예방을 위해 소화·섭취가 용이한 품질이 높은 단백질 보충 소재 개발이 요구되며, 특히 고령층은 동물성 단백질보다 곡류를 통한 단백질 섭취 비중이 높아, 식물성 자원을 활용한 근감소 예방 소재 개발이 더욱더 중요하다.
지금까지 식량작물에 대한 단백질의 특성을 평가한 논문들은 일부 보고되어 있는데, 대부분 콩을 대상으로 단백질을 추출하여 이화학적 특성을 비교(Kim et al., 2022)하였다. 단백질 추출 수율과 in vitro 단백질 소화율이 양의 상관관계를 가지며(r=0.633, p<0.05), 단백질 분자량 패턴을 분석하여, 품종별로 차이가 있음을 확인하는 수준이었다. 또한, 국내산 콩 품종별로 Rhizopus oligosporus 발효물의 단백질 품질을 평가하여 곰팡이균의 발효에 의해 단백질 소화율이 증가한다는 결과를 보고한 바 있다(Park et al., 2022). 하지만 단백질 품질평가 중 일부 항목만을 평가하여, 전체적인 단백질 품질평가 연구는 부족하며, 콩 외에 다른 작물들의 단백질에 대한 품질 평가가 종합적으로 제시된 연구는 부족하다. 향후 고령층의 식습관과 생리적 특성을 고려하여 섭취하기 쉽고, 소화율이 향상되면서 근육량을 유지시킬 수 있는 단백질 성분을 혼합하거나, 근육 단백질의 합성능력을 향상시킬 수 있는 가공처리 등을 통한 단백질 강화식품 개발이 지속적으로 요구될 것이다. 따라서 본 논문은 단백질 보충소재의 재료가 될 수 있는 식량작물과 국내 재배 품종들을 대상으로 근감소증 예방과 밀접한 연관이 있는 영양성 및 단백질 품질 특성을 평가하고자 하였다.
재료 및 방법
시험 재료 및 탈지 조건
본 연구에서는 주요 식량작물 땅콩(Arachis hypogaea L.), 참깨(Sesamum indicum L.), 들깨(Perilla frutescens L.), 팥(Vigna angularis L.), 콩(Glycine max L.), 녹두(Vigna radiata L.), 동부(Vigna unguiculata L.), 조(Setaria italica L.), 기장(Panicum miliaceum L.), 수수(Sorghum bicolor L.), 귀리(Avena sativa), 아마란스(Amaranthus L.)를 대상으로 하였으며, 2023년도에 재배된 12작목의 주요 재배품종인 29품종을 시험재료로 사용하였다(Table 1). 시험재료 중 동부인 ‘옥당’ 품종은 영광군농업기술센터에서, ‘홍원’ 품종은 전남도농업기술원에서 분양받았으며, 나머지 모든 시험재료는 국립식량과학원 육종부서에서 증식용으로 재배된 시험재료를 사용하였다. 지질함량이 많은 땅콩, 참깨, 들깨, 콩은 분쇄시료에 10배수의 헥산을 가하여 24시간 정치 탈지시킨 후 크린벤치 내 2~3일간 헥산을 날린 후 분석에 사용하였다. 모든 시험재료는 분쇄기(HMF-3100S, Hanil Co., Kangwon, Korea)로 분쇄 후 30mesh 체로 내려 사용하였으며, 분쇄된 시료는 -20℃에 보관하면서 분석에 사용하였다.
Table 1.
Crops and cultivars used as materials.
| Crop | N0. | Cultivar | ||||||
|
Peanut cance* | 2 | Hae-Ol | Gowon1 | |||||
| Sesame* | 2 | Goenbaek | SuperHani | |||||
| Perilla* | 2 | Deulsaem | Suyeon | |||||
| Red bean | 2 | Arari | Hongda | |||||
| Soybean* | 7 | Daedan | Seonpung | Daewonkong | Cheongja5ho | Seum | Soriheuk | Soman |
| Mung bean | 2 | Sanpo | Miryang-3 | |||||
| Cowpea | 2 | Okdang | Hongone | |||||
| Millet | 2 | Samdachal | Chohwangme | |||||
| Proso millet | 2 | Hallachal | Yeonheechal | |||||
| Sorghum | 3 | Donganme | Goeunchal | Sodamchal | ||||
| Oat | 2 | Daeyang | Choyang | |||||
| Amaranth | 1 | BeckSeon | ||||||
수분함량, 조단백질, 회분, 조지방 및 탄수화물 함량
수분함량은 dry oven 온도 105℃ 설정하여 설정 온도가 되면 tray에 수분 캔의 두고 뚜껑을 반쯤 열어둔 후, 105℃ dry oven에서 2시간 가열하였다. 2시간 후, 수분 캔 뚜껑을 닫고 데시게이터에 30분 방냉하였다. 방냉 후, 빈 수분 캔 무게를 측정하였다. 분쇄 시료 1 g을 칭량한 후, 다시 105℃ dry oven에서 3시간 가열하였다. 3시간 후, 수분 캔 뚜껑을 닫고 데시게이터에 30분 방냉하였다. 방냉 후, 수분 캔 무게를 측정하였다.
조단백질 함량은 Micro-Kjeldahl법을 참고하여 측정하였다(NICS, 2009). 분쇄 시료 0.5 g을 단백질 분해관에 넣고 황산 10 mL과 촉매제를 넣어 분해기(Tecator™ Digestor auto, Foss, Denmark)를 이용해 420℃에서 1시간 동안 분해하였다. 상온에서 충분히 냉각시킨 후 단백질 분석기(Vapodest® 50s, C. Gerhardt GmbH & Co. KG, Germany)를 이용하여 조단백질 함량을 측정하였다.
조지방 함량은 Soxtherm automatic system (Soxtherm® sox416, C. Gerhardt GmbH & Co. KG, Germany)을 이용하여 정량하였다(AOAC, 2005). 분쇄 시료 2 g을 extraction thimble에 담아 탈지면으로 막고 비등석과 n-hexane 140 mL을 첨가하여 187℃에서 30 분간 가열하고, 1시간 동안 추출하였다. 지방 추출 후 수기를 105℃에서 1시간 동안 건조 후 방냉하여 무게를 측정한 후 함량을 구하였다.
회분함량은 회화로 온도를 600℃로 맞추고 미리 예열한 후, 회화 용기를 도가니 집게를 사용하여 회화로에 넣고, 2시간 가열하였다. 2시간 후, 데시게이터에 1시간 방냉하였다. 방냉 후, 빈 회화 용기 무게를 측정하였다. 분쇄 시료 1 g을 칭량하였다. 600℃ 회화로에 다시 넣고, 5시간 가열하였다. 5시간 후, 데시게이터에 1시간 방냉하였다. 방냉 후, 회화 용기 무게를 측정하였다.
탄수화물 함량은 조단백, 조지방, 수분, 조회분 함량을 모두 더한 값으로 산출하였다.
아미노산 분석
구성아미노산 분석은 시료 0.3 g을 뚜껑이 있는 pyrex 시험관에 넣고 6 N HCl 10 mL를 가한 후 N2 gas를 1분간 불어 넣어 시험관 내부의 가스를 치환한 다음, 드라이 오븐에 넣어 110℃에서 22시간 동안 산 가수분해하였다. 냉각한 시료 의 가수 분해물을 0.02 N HCl 10 mL에 녹이고, 10배 희석하여 0.22 μm membrane filter (Merck Millipore, Darmstadt, Germany)로 여과하여 아미노산 분석을 위한 시료 전처리를 완료하였다. 분석기기는 아미노산 자동분석기(HITACH L-8800 Amino acid auto analyzer, Hitachi, Tokyo, Japan)를 이용하였고, 이동상은 PH1, PH2, PH3, PH4, PH-RG, R-3, C-1, ninhydrin solution, buffer solution (Fujifilm Wako Pure Chemical,Wako, Japan), 컬럼은 ion exchange Column, Hitachi, Tokyo, Japan)를 사용하였다. 컬럼과 reaction chamber 온도 조건은 각각 50℃와 135℃이었고, 표준물질(Amino acid calibration mixture, Ajinomoto-Takara Co., Tokyo, Japan)로 각 아미노산 함량을 산출하였다(Im et al., 2016).
아미노산 자동분석기(HITACH L-8800 Amino acid auto analyzer, Hitachi, Tokyo, Japan)에서 정량 분석이 어려운 트립토판은 Çevikkalp et al., 2016 방법을 변형하여 UPLC (Ultra Press Liquid Chromatography)를 사용하여 분석하였다. 트립토판 추출조건은 분쇄 시료 0.5 g을 뚜껑이 있는 pyrex 시험관에 넣고 5N sodium hydroxide solution 20 mL를 가한 후 N2 gas를 1분간 불어 넣어 시험관 내부의 가스를 치환한 다음, heating block에 넣어 110℃에서 16시간 동안 가수분해하였다. 냉각한 시료의 가수 분해물을 50 mL conical tube에 옮겨 10000 rpm에서 10분 원심분리 실시하였다. 상층액을 50 mL conical tube에 여과지로 여과한 후 산성수(pH 6.3)으로 50 mL로 정용 후 voltexting 하였다. PDVF 0.22 μm membrane filter (Merck Millipore, Darmstadt, Germany)로 여과하여 트립토판 분석을 위한 시료 전처리를 완료하였다. 분석기기는 Waters ACQUITY HPLC System equipped with 2998 photodiode array detector and autosampler을 사용하였으며, column은 Lichrospher 60 RP-Select B (250 mm × 4 mm, 5 μm, Agilent, Santa Clara, CA, USA)를 사용하였으며, 유속은 1.0 mL/min, 10 ㎕를 injection volume으로 설정하였다. 이동상으로는 900 mL의 암모늄 아세테이트 완충액(ammonium acetate buffer, pH 6.3)과 100 mL의 ACN을 혼합한 용액 (A)을 사용하여 최초 100 (A) : 0 (B) (v/v)로 시작하여 10분 동안 isocratic으로 조건을 설정하였다. Detector는 280 nm로 설정하여 분석하였다.
단백질 품질 분석
시험재료의 단백질 소화 관련한 품질분석은 protein digestibility assay kit (K-PDCAAS, Megazyme, Chicago, IL, USA)를 이용하여 분석하였다. 분쇄한 시료 500 mg와 0.06 N HCl 19 mL를 50 mL 원심 분리 튜브에 넣고 shaking incubator (DS-310F, Dasol science Ltd., Hwaseong, Korea) 37℃에서 300 rpm으로 30분간 shaking한 다음, pepsin solution 1 mL를 가하여 완전히 섞어준 후 다시 37℃에서 300 rpm으로 60분간 shaking 하였다. Pepsin 반응 후 1.0 M tris buffer 2 mL를 가하여 pH 7.4로 맞춘 후 충분히 섞어주었다. 여기에 trypsin/chymotrypsin 효소혼합액 200 μL를 가하여 완전하게 섞어준 후 37℃에서 300 rpm으로 4시간 동안 shaking 하였고, 효소반응 후 65℃의 항온수조에 10분간 처리 후 상온에서 20분간 식혀 주었다. 식힌 반응액 4 mL에 40% TCA용액 1 mL를 가하여 완전히 섞어 준 후 4℃에서 16시간 방치하였다. 1.75 mL 의 TCA 처리 반응액을 15,000×g에서 10분간 원심분리한 후 상등액 100 μL를 취하여 sodium acetate buffer (50 mM, pH 5.5) 900 μL와 혼합하여 최종 반응의 시료로 하였다. 시료 100 μL를 96-well microplate에 넣고 2% ninhydrin 용액 50 μL를 가한 후 호일로 plate를 덮은 후 70℃, 35분간 100 rpm으로 반응시킨 후 10분간 실온에서 방냉 하였다. 마지막 단계로 50% 에탄올을 0.15 mL 가한 후 분광광도계(EPOCH2, Bio Tek Instruments Inc., Winooski, VT, USA)로 570 nm에서 흡광도를 측정하였다. Megazyme사에서 제시한 Mega-Calc (Megazyme 2019)에 시료, L-glycine standards, blank 및 control sample의 흡광도 값, 각 시료의 수분, 단백질, 아미노산 조성을 대입하여 in vitro digestibility, 아미노산가(amino acid score), 제1제한아미노산(first limiting amino acid), 단백질 소화율 보정 아미노산가(PDCAAS, protein digestibility corrected amino acid score)를 산출하였다(Plank, 2017).
통계 분석
시험재료와 분석항목은 모두 3반복으로 수행하였고, 실험 결과는 평균과 표준오차로 표시하였다. 다만 단백질 품질 평가인 in vitro digestibility, 아미노산가, 제1제한아미노산, 단백질 소화율 보정 아미노산가는 실험결과의 평균값을 계산식에 대입하여 산출하였다. 통계분석은 ANOVA 프로그램(Version 18.0, SPSS Inc., Chicago, IL, USA)을 이용하였고, 평균간 비교를 위해 분산분석(ANOVA)을 수행하였다. 유의성이 있을 경우 5% 유의수준에서 Duncan의 다중검정을 실시하였다.
결과 및 고찰
작물 및 품종별 영양성분
노화에 따른 근감소 예방을 위해서는 우선 균형 잡힌 영양 공급이 중요하다. Table 2는 주요 작물 및 품종의 영양성분을 비교한 결과로, 조단백질, 지질, 회분 및 탄수화물 함량에 있어 작물 간 뚜렷한 차이를 나타내었다. 조단백질 함량은 땅콩, 참깨, 들깨, 콩이 높았으며, 특히 땅콩인 ‘고원1호’(60.1%), ‘해올’(58.8%) 품종이 가장 높았으며, 참깨인 ‘건백’(49.4%), ‘슈퍼하니’(47.1%), 들깨인 ‘들샘’(40.2%), ‘수연’(37.4%) 품종이 각각 높았다. 콩의 조단백질 함량은 48.4∼52.3% 범위였으며, ‘소만’ 품종이 가장 낮고, ‘대단’ 품종이 가장 높았다. ‘대단’ 품종은 2024년 농촌진흥청이 개발한 고단백 콩 품종으로 알려져 있어 본 연구결과와 단백질 특성이 일치하였다.
Table 2.
Nutritional composition of crops and cultivars.
지질의 경우, 단순히 에너지원으로서의 역할을 넘어 근육 대사에 관여하는 중요한 조절인자로 작용하는 것으로 보고되어 있다(Held et al., 2020). 땅콩, 참깨, 들깨, 콩은 지질함량이 높은 작물이나, 탈지 처리 한 본 시험재료에서는 땅콩, 참깨, 들깨, 콩의 지질함량이 1~2% 수준으로 나타났다. 곡물 중에서는 귀리의 ‘대양’ 품종이 10.2%, ‘조양’ 품종이 9.6%으로 다른 곡물에 비해 월등히 높은 함량을 나타내었으며, 아마란스 ‘백선’(5.7%) 품종도 다소 지질함량이 높았다. 이는 기존 보고된 함량값과 유사한 결과였다(Lee et al., 2016).
회분(ash) 함량은 작물의 무기질 함량을 반영하여 영양학적 가치평가에 활용되는데, 참깨가 가장 높았고, 들깨, 콩도 다소 높았다. 특히 참깨인 ‘슈퍼하니’(11.2%), ‘건백’(10.2%)과 들깨의 ‘들샘’(6.7%), 콩의 ‘대단’(6.3%) 품종에서 높은 함량을 보였다. 기존 문헌에도 참깨는 비타민(B1, B2, E), 셀레늄 등이 풍부하게 함유되어 있는 것으로 보고되어 있으며, 들깨는 칼슘과 철분이 풍부하여 뼈 건강과 혈액 순환에 도움을 주는 것으로 알려져 있다(Park et al., 1990; Park & Kang., 2004). 칼슘(Ca), 마그네슘(Mg), 아연(Zn) 등 무기질이 근수축과 단백질 합성 효소 활성에 관여하고, Mg와 Zn은 단백질 전사 및 번역 단계의 보조인자로 작용하여 근육세포 내 단백질 합성 효율을 높이는 것으로 보고되어 있어(Berchtold., 2000; Castiglioni et al., 2024; Costa et al., 2023; Hernández-Camacho et al., 2020; Nasso et al., 2024) 회분함량도 단백질 보충소재로 활용하기 위해 중요한 성분이 될 수 있을 것이다.
근육 내 에너지 대사에 필수적인 역할을 하는 탄수화물 함량은 기존에 보고된 바와 같이 조, 기장, 수수, 아마란스, 귀리 등과 같은 곡물이 높았으며, 조의 ‘삼다찰’(83.9%) 품종이 가장 높았으며, 수수인 ‘고은찰’(83.7%) 품종도 높았다. 두류 중에서는 팥인 ‘홍다’(73.0%), ‘아라리’(72.7%) 품종이 높았고, 녹두인 ‘옥당’(72.2%) 품종도 높은 함량을 가졌다. 탄수화물을 단백질과 함께 섭취될 경우 인슐린 분비를 유도하여 아미노산의 근육세포 내 흡수를 촉진하여 단백질 단독 섭취 시보다 근단백질 합성률을 향상시키며, 근단백질 분해 억제에도 효과적인 것으로 알려져 있다. 다수의 임상연구에서도 탄수화물과 단백질을 함께 섭취시 운동 후 근단백 합성이 증대됨을 보고하고 있다(Børsheim et al., 2004; Howarth et al., 2009). 따라서 단백질과 탄수화물이 균형적으로 포함된 곡류-두류 복합식은 근감소 예방에 유리한 식이조합으로 고려될 필요가 있으며, 본 자료가 이를 위한 기초자료로 활용 될 수 있을 것이다.
작목 및 품종별 오메가-3 지방산 함량
Table 3은 주요 작물(품종)의 지방산 조성을 분석한 결과로 작물 간에 지방산 조성과 포화·불포화지방산 함량 차이 등 뚜렷한 차이를 보였다. 불포화지방산 함량은 아마란스, 귀리, 조, 참깨, 들깨 순으로 함량이 높았다. 아마란스의 ‘백선’ 품종의 불포화지방산은 88.2%로 가장 높았고, 귀리의 ‘대양’ 품종은 84.5%, 조의 ‘삼다찰’ 품종은 83.4%, 참깨의 ‘건백’ 품종이 81.8%로 높은 비율을 보였다. 지방산 조성 중에서도 땅콩인 ‘해올’(42.9%)과 참깨인 ‘슈퍼하니’(40.0%) 품종에서 높은 올레산(cis-9-oleic acid)을 함유하였고, 이는 기존의 품종 특성과 유사한 경향을 나타내었다.
Table 3.
Fatty acid profiles of crops and cultivars.
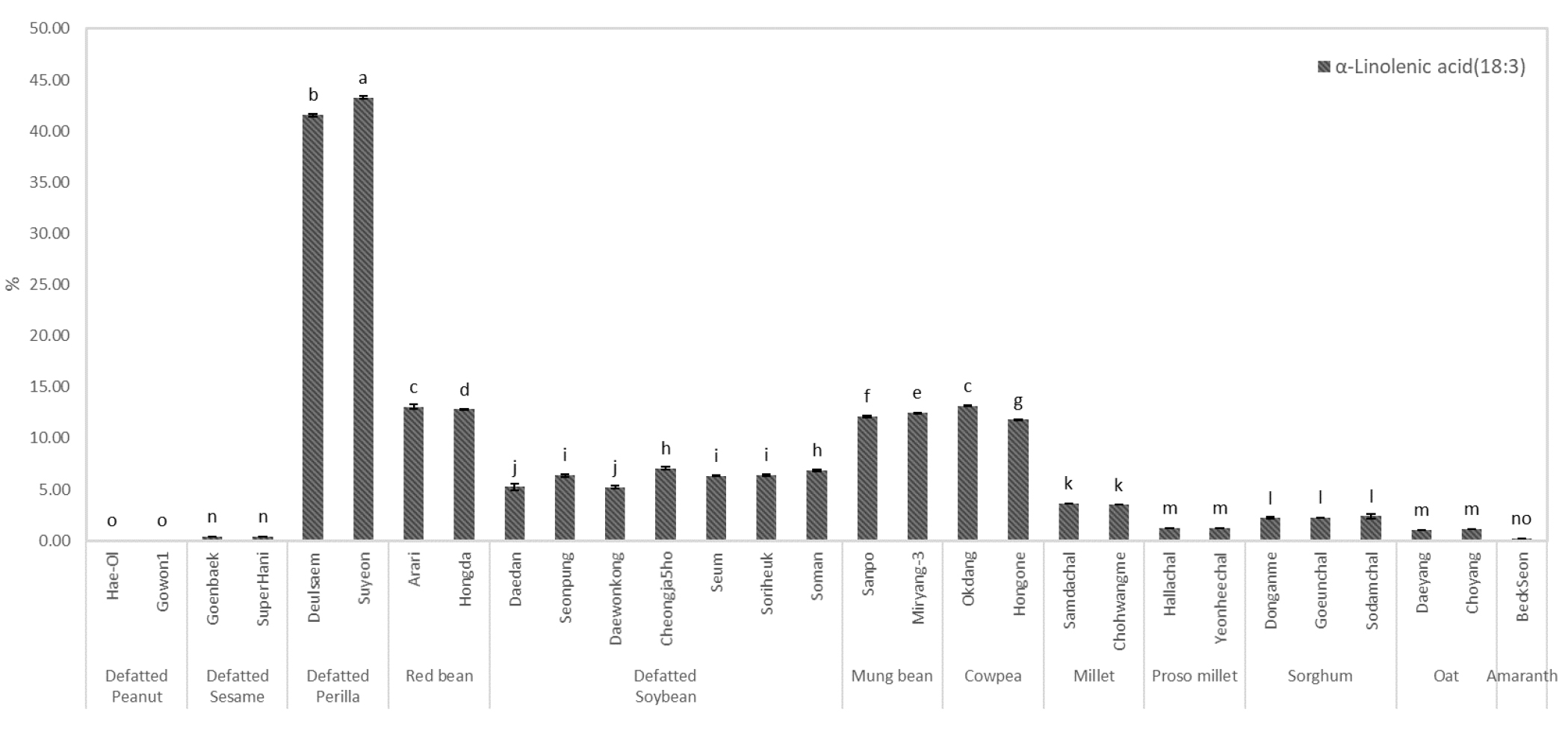
지방산 중 오메가-3 지방산(omega-3 fatty acid, ω-3 fatty acid)은 우리 몸에서 합성되지 않아 식품으로 섭취해야 하는 필수 지방산으로 α-리놀렌산(18:3, n-3, ALA), 에이코사펜타엔산(20:5, n-3, EPA), 도코사헥사엔산(22:6, n-3, DHA) 3가지 종류의 지방산으로 알려져 있다. 뇌 기능, 심혈관 건강, 염증 완화 등에 중요한 역할을 하는 것으로 보고되어 있으며(Dighriri & Alsubaie., 2022; Khan et al., 2021), 주로 등 푸른 생선(EPA, DHA)이나 식물성 기름(ALA)을 통해 섭취할 수 있다. 특히 오메가-3 지방산은 근육단백질 합성 경로(mTORC1 pathway)를 활성화하고 사이토카인(IL-6, TNF-α)의 생성을 억제하여 염증 반응을 감소시켜, 근세포 손상을 완화하고, 근질량 유지에 도움을 주는 것으로 보고되어 있다(Bird et al., 2020; Eggimann et al., 2025; Huang, 2023; Smith et al., 2011). 이러한 오메가-3 지방산 중 α-리놀렌산이 들깨, 동부, 팥, 녹두에서 다른 작물에 비해 높았으며, 특히 들깨는 ‘수연’(43.3%), ‘들샘’(41.6%)의 함량이 다른 작물에 비해 월등히 높았다(Fig. 1). 본 연구에서는 탈지한 들깨를 사용하여 기존에 보고된 들기름(60%)이나, 생들깨(약 55%)보다는 α-리놀렌산이 상대적으로 약간 낮은 함량을 보였으나, 다른 작물에 비해서는 월등히 높은 함량이었다. 들깨 이외에는 동부인 ‘옥당’(13.2%), 팥의 ‘아라리’(13.1%), ‘홍다’(12.8%), 녹두인 ‘밀양3호’(12.5%), ‘산포’(12.2%) 품종 순으로 함량이 높았다. 곡물 중에서는 조의 ‘삼다찰’(3.6%) ‘조황메’(3.5%) 품종이 다소 높은 수준으로 함유되어 있었다.
따라서 탈지 들깨는 높은 불포화지방산 함량과 α-리놀렌산 지방산 비율이 높아 근감소 예방을 위한 소재로서 활용성이 높을 것으로 판단된다.
작물 및 품종별 아미노산 조성
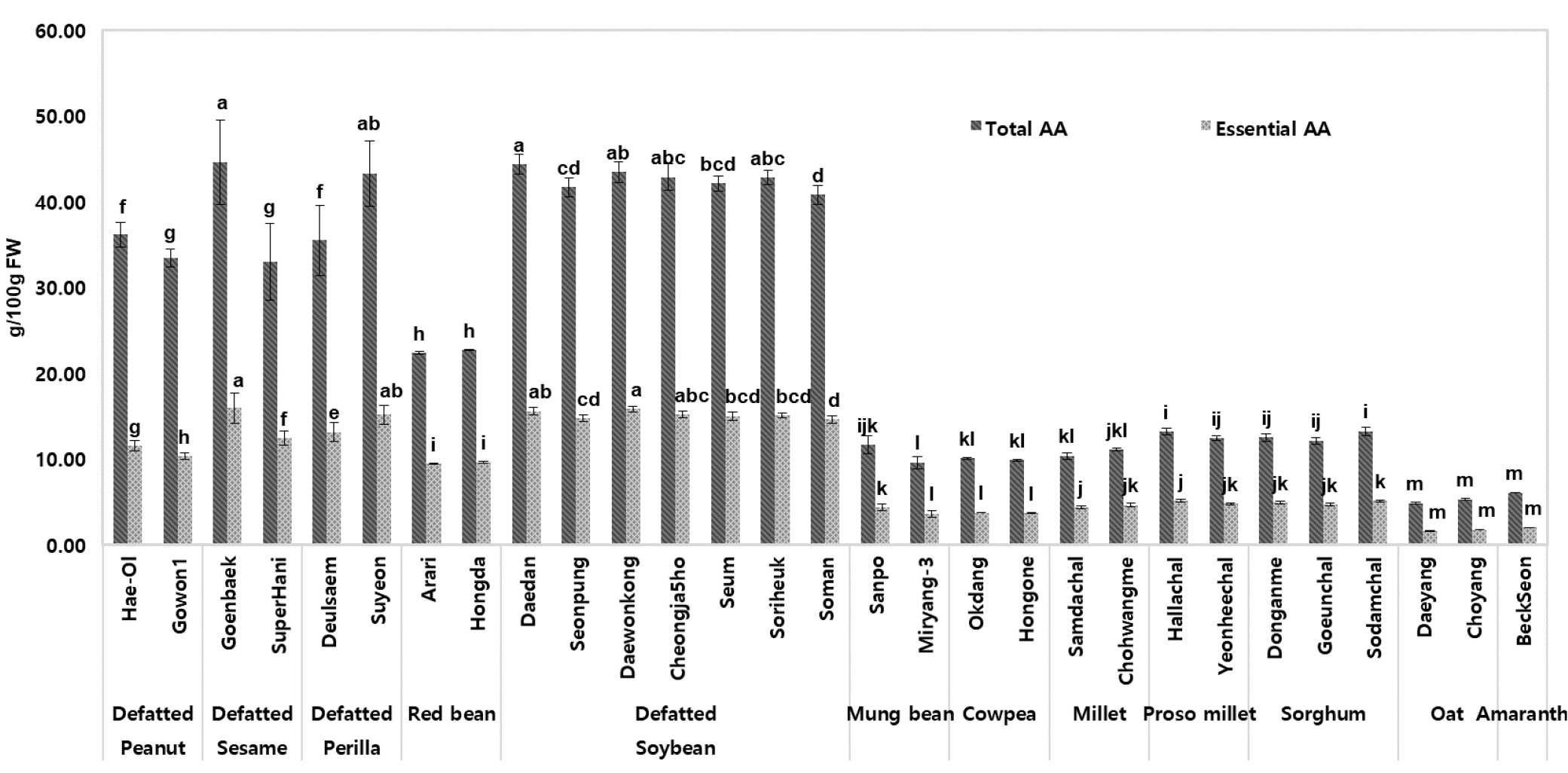
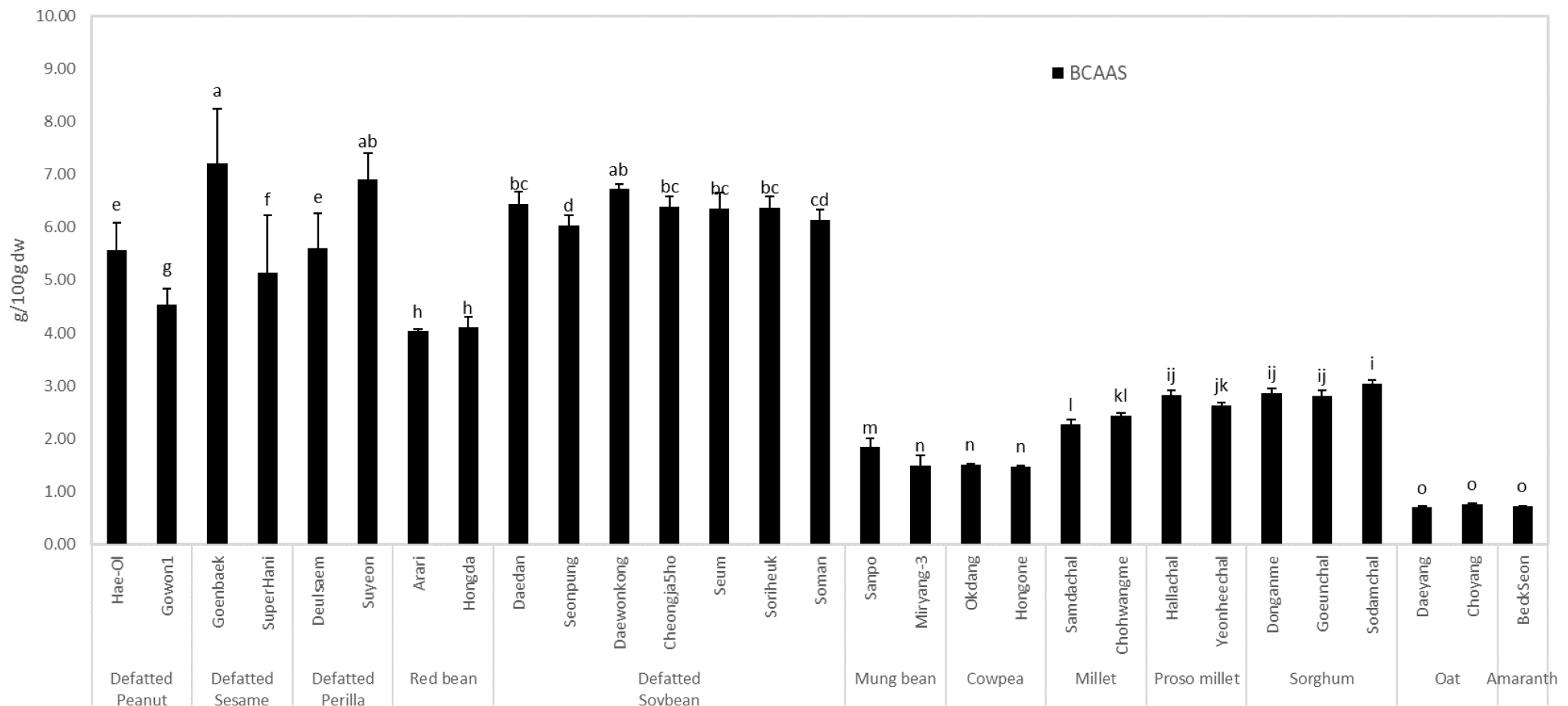
작목(품종)별 총아미노산 함량과 필수아미노산 함량을 비교한 결과(Fig. 2) 유의한 차이를 나타내었다. 총 아미노산 함량(g/100 g dw)은 콩, 참깨, 들깨, 땅콩이 높았으며, 콩은 40.8~44.3 범위였으며, ‘대단’ 품종이 가장 높았고, ‘소만’ 품종이 낮았다. 참깨는 ‘건백’(44.5), 들깨에서는 ‘수연’ (43.2), 땅콩은 ‘해올’(36.1) 품종이 높았다. 필수아미노산 함량(Essential Amino Acid, EAA)도 참깨, 콩, 들깨에서 함량이 높았으며, 참깨는 ‘건백’(15.9), 들깨는 ‘수연’(15.1), ‘들샘’(13.9), 콩은 14.7~15.8의 분포였으며, ‘대원콩’이 가장 높고, ‘소만’ 품종이 낮았다. 아미노산 조성 및 함량은 근육량 유지 및 합성에 직접적으로 영향을 미치는 요소로, 특히 근육 단백질 합성에 직접적으로 관여하는 분지사슬아미노산(Branched Chain Amino Acids, BCAAs)인 류신, 이소류신, 발린 함량은 근감소 예방에 가장 중요한 아미노산으로 평가된다. BCAAs의 함량(g/100g)도 참깨, 들깨, 콩, 땅콩에서 높았으며, 참깨 품종인 ‘건백’(7.2), 들깨 품종은 ‘수연’(6.9)이 높았고, 콩은 6.0~6.7 분포로 함유되어 있었으며, ‘대원콩’이 가장 높고, ‘선풍’이 가장 낮았다. 땅콩은 ‘해올’이 5.5 수준으로 함유되어 있었다(Fig. 3). BCAAs 함량은 재배 환경, 가공 방식 등에 따라 달라질 수 있으나, 일반적으로 아미노산 함량이 높을수록 BCAAs 함량도 높은 것으로 알려져 있다(Michael, 2005). 기존 대두의 건조중량 100 g당 약 5 g 이상의 BCAA(류신 약 2 g, 이소류신/발린 각 약 1.5 g 수준)를 함유하고 있으며, 땅콩도 건조중량 100 g당 약 5 g 수준의 BCAA를 함유하는 것으로 보고되어 있다(Kim et al., 2022). 본 시험재료는 탈지 처리한 참깨, 들깨, 콩, 땅콩으로 기존 원곡보다 다소 높은 함량을 보이는 것으로 판단된다. 곡물에서는 총 아미노산 함량, 필수아미노산, BCAAs 모두 수수, 기장, 조의 함량이 다소 높았다. 총 아미노산(g/100 g)은 수수는 12.1~13.2 분포를 보였으며, ‘소담찰’ 품종이 가장 높았다. 기장은 ‘한라찰’(13.2), ‘연희찰’(12.4)이 높은 함량을 함유하고 있었다. 필수아미노산(g/100 g)도 수수의 ‘소담찰’(5.1), ‘동안메’(4.8)가 높았으며, 기장의 ‘한라찰’(5.1) 품종이 높았다. BCAAs 함량(g/100 g)도 수수가 2.8~3.0 이었으며, ‘소담찰’ 품종이 높았다. 기장에서는 ‘한라찰’(2.8), ‘연희찰’(2.6)순으로 높았고, 조의 경우 ‘조황메’(2.4), ‘삼다찰’(2.2)이 높게 함유되어 있었다. 곡물 중에서 수수, 기장, 조는 필수아미노산 조성이 양호하고 BCAAs 함량이 높아 근감소 예방용 보조 곡물 단백질원으로서 이용성을 고려해 볼 수 있을 것이다. 전체적인 아미노산 조성을 고려했을 때 탈지 들깨와 탈지 콩은 모든 아미노산 성분이 가장 높은 분포를 보였으며(p<0.05), 근단백질 합성에 필요한 아미노산 공급원으로, 활용 가치가 클 것으로 판단된다.
단백질 품질 평가
Megazyme사에서 제시한 Mega-Calc (Megazyme 2019)을 활용하여 in vitro digestibility(단백질 소화율), 아미노산가(amino acid score), 제1제한아미노산(first limiting amino acid), 단백질 소화율 보정 아미노산가(PDCAAS, protein digestibility corrected amino acid score)를 산출하여 작물 및 품종별로 단백질 품질을 평가한 결과를 나타내었다(Table 4). 단백질 소화율은 0.78~1.00 범위였고, 대부분의 작물에서 제한아미노산은 라이신(Lysine) 또는 시스테인+메티오닌(Cys+Met)으로 나타났다. 이는 식물성 단백질의 공통적 특성으로, 특히 곡류에서는 라이신이, 두류에서는 메티오닌 및 시스테인이 제한요소로 작용하는 것으로 알려져 있다. 본 연구에서 탈지 콩(‘세움’)을 제외하고 L-발린이 제한아미노산으로 나타났으며, 이는 기존에 보고된 한국 콩의 단백질에 포함된 제일 제한아미노산은 트립토판과 메티오닌으로 알려져 있는데 콩에 포함된 필수 아미노산 중 트립토판은 과거에 검출이 어려워 대부분 고려되지 않았거나, 기존 자료를 참조하여 평가한 것으로 알려져 있다(Park et al., 2022). 본 연구에서는 트립토판이 모두 검출되어 발린이 상대적으로 가장 낮은 함량을 보여 제한아미노산으로 작용한 것으로 보인다.
Table 4.
Protein quality of crops by various cultivars.
아미노산점수(Amino Acid Score, AAS)는 단백질의 품질을 나타내는 지표로, 특정 식품의 필수 아미노산 조성이 기준 단백질 대비 얼마나 고른지를 나타내는 것으로 점수가 높을수록 단백질의 완전성이 높아져 소화와 흡수가 잘 되는 완전 단백질로 간주한다. PDCAAS는 단순히 아미노산의 함량뿐만 아니라 소화율까지 함께 고려하여 단백질의 품질을 평가하는 방법으로 1993년 미국 식품의약국(FDA)과 유엔 식량 농업 기구(FAO)·세계 보건 기구(WHO)에 의해 채택되었다(Boutrif et al., 1991). 본 연구에서 AAS는 콩에서 0.76~0.91 범위였으며, ‘대원콩’ 품종이 가장 높았으며, 들깨는 ‘들샘’(0.85), ‘수연’(0.65)으로 ‘들샘’ 품종이 높았다. 다음으로 팥은 ‘아라리’(0.87), ‘홍다’(0.84) 순으로 높은 수준이었다. 따라서 콩, 들깨, 팥은 필수아미노산 조성이 상대적으로 균형 있게 구성되어 있음을 알 수 있다. PDCAAS 값도 콩이 0.71~0.85 범위였으며, ‘대원콩’ 품종이 가장 높았다. 들깨는 ‘들샘’(0.77), ‘수연’(0.64)이 다른 작물에 비해 상대적으로 우수하였으며, 팥의 PDCAAS 값도 ‘아라리’(0.71), ‘홍다’(0.69)로 높아 아미노산점수 값과 같은 경향을 보였다. 따라서 탈지 콩, 탈지 들깨는 AAS와 PDCAAS 값이 다른 작물에 비해 상대적으로 높아 체내 이용률이 높을 것으로 판단된다. 기존에 보고되어 있는 식품의 PDCAAS 값과 비교했을 때 카제인(1.00), 달걀흰자(1.00), 분리대두단백(1.00), 유청(1.00), 쇠고기(0.92) 등과 같이 비교했을 때는 다소 낮지만, 원곡의 탈지 처리가 분리 정제한 물질이 아님에도 비교적 높은 PDCAAS 값을 보여 활용성이 높을 것으로 판단된다. 특히 제한아미노산은 단백질 합성률을 결정하는 핵심 인자로 작용하므로, 라이신 및 황 함유 아미노산의 보충 시 근단백질 합성 효율을 높일 수 있고, 들깨와 대두는 α-리놀렌산과 BCAAs가 풍부하여, 제한아미노산이 일부 존재하더라도 근단백질 합성 경로(mTOR 활성화)를 통해 단백질 효율을 보완할 수 있는 잠재력이 있을 것이다. 따라서 들깨와 대두 단백질은 근감소 예방 및 노년층 단백질 보충용 소재로서의 활용 가능성이 높을 것으로 판단된다.
적 요
본 연구는 고령화에 따른 근감소증 예방을 위한 단백질 보충소재 적용을 위한 기초자료로서, 주요 식량작물 12작목 29품종의 영양성분, 지방산조성, 아미노산 조성 및 단백질 품질 특성을 비교·평가하였다.
1.조단백질 함량은 탈지 처리한 땅콩, 참깨, 들깨, 콩이 높았으며, 참깨, 들깨, 콩은 회분 함량이 많았고, 조·기장·수수 등 곡물은 탄수화물 함량이 높았다.
2.탈지 들깨는 α-리놀렌산(‘수연’ 43.3%) 함량이 높아 근육단백질 합성경로를 활성화하고, 염증반응을 감소시켜 근세포 손상 완화에 도움을 주는 것으로 알려져 있는 오메가-3 지방산의 우수한 공급원으로 확인되었다.
3.총 아미노산과 필수아미노산(EAA) 함량은 들깨, 콩, 참깨에서 높았으며, 근육단백질 합성에 직접적으로 관여하는 분지사슬아미노산(BCAAs, g/100g)은 참깨 ‘건백’(7.2) 품종과 들깨 ‘수연’(6.9), ‘대원콩’(6.7) 품종에서 높았다.
4.단백질 품질 평가 시 본 시험재료의 제한아미노산은 주로 라이신, 시스테인+메티오닌 그리고 발린이었다. 아미노산점수(AAS)와 단백질소화율보정아미노산점수(PDCA AS)값은 콩, 들깨, 팥이 높았으며, PDCAAS 값은 콩 ‘대원콩’(0.85), 들깨 ‘들샘’(0.77), 팥 ‘아라리’(0.71) 순이었다. 따라서 탈지 들깨와 탈지 콩 단백질은 근감소증 예방 및 노년층 단백질 보충용 식품소재로서의 활용 가능성이 높을 것으로 판단된다.