서 론
재료 및 방법
식물재료
재배 방식에 따른 생리 특성 그리고 기공 특성 관찰 및 평가
재배 방식에 따른 잎 조직 특성 관찰 및 평가
통계 분석
결과 및 고찰
재배 방식과 품종에 따른 식생 지수, 광합성 및 기공 특성 평가
재배 방식과 품종에 따른 잎 조직 특성 평가
적 요
서 론
고구마(pomoea batatas (L.) Lam)는 중남미 열대 지역이 원산지인 작물로, 전 세계적으로 연간 약 9천 3백만 톤 이상 생산되는 주요 식량 자원이다(O’Brien, 1972; FAO, 2023). 고구마는 척박한 환경에서도 생육이 좋아 한국과 일본 그리고 아프리카 등에서 주식, 간식, 전분, 주정, 그리고 건강 기능성 식품 소재로 이용된다(Woolfe, 1992; Scott et al., 2000; Ishida et al., 2000; Mohanraj & Sivasankar, 2014). 국내에서는 씨고구마를 3월에 파종하여 육묘한 후 5-6월에 삽식하는 방식으로 재배한다(RDA, 2018).
삽식 재배는 고구마의 품질을 일정하게 유지시키는 장점이 있다 (Clark et al., 2012). 그러나 채묘 시 절단 스트레스를 가해야 하며 삽식 초기 활착 과정에서 수분과 온도 변화와 같은 환경 스트레스에 의해 묘의 생육이 저해될 수 있다(Wijewardana et al., 2018; Kim et al., 2020). 특히 고구마의 수확량은 생육 초기에 결정되는 괴근의 수에 좌우되며, 이 시기 괴근의 발달은 광합성 산물을 공급하는 잎의 생리적 활성에 영향을 받는다(Wijewardana et al., 2018). 따라서 초기 생육 스트레스는 안정적인 수량 확보를 어렵게 만들며, 이는 결국 고구마의 생산 비용을 높이고 재배 안정성을 저해하는 주요 원인이 된다(Fuglie, 2007; RDA, 2018).
삽식의 대안으로 씨고구마를 직파할 수 있다(Sakaigaichi et al., 2021). 직파는 채묘 스트레스가 발생하지 않으며 초기 생육 시 씨고구마의 에너지원을 활용할 수 있고 스트레스 저항성 향상 효과가 있다(Shikata, 1976; Kays, 1985; Sakaigaichi et al., 2023). 이러한 이점 덕분에 직파가 삽식보다 초기 생육 환경이 안정적일 수 있다.
삽식과 직파에 따른 생육 양상 비교 연구는 미국과 일본에서 이루어졌다(George et al., 2011; Sakaigaichi et al., 2023). 해외 선행 연구에서는 씨고구마 직파 재배가 노동력 절감과 같은 이점을 가지며, 일부 품종에서는 기존 삽식 재배보다 수확량을 유의미하게 증가하였다(Adachi et al., 2012). 하지만, 국내에서 재배되는 고구마 품종을 대상으로 하는 연구는 필요하다. 따라서, 이 연구는 국내 및 일본의 주요 고구마 품종과 계통을 대상으로 재배 방식이 고구마의 초기 생장기 식생지수, 광합성 특성, 기공 특성, 그리고 잎의 조직학적 특성에 미치는 영향을 분석하였다.
재료 및 방법
식물재료
재배 방식에 따른 고구마 유전자원의 생리 및 조직 특성을 관찰하기 위하여 국내 유전자원 하얀미, 호풍미, 소담미, 신황미, 은미, 신천미, 진주 재래종, 의령 재래종, 그리고 고성 재래종 9종과 일본 유전자원 베니하루카, 시로유다카, 그리고 야마가와 무라사키 3종을 사용하였다(Fig. 1). 고구마 직파와 삽식은 경상남도농업기술원에서 난괴법을 이용하여 2024년 4월 5일과 2024년 6월 13일에 이루어졌다. 직파에는 별도의 절단 처리를 하지 않은 온전한 씨고구마를 사용하였고, 삽식에는 약 30 cm의 건전한 묘를 사용하였다. 시비와 재배는 농촌진흥청 표준재배법에 따랐다(RDA, 2018).
모든 기공 특성, 식생지수, 광합성 특성, 그리고 잎 조직 특성은 초기 생장기가 끝나는 파종 그리고 삽식 후 50일 후에 완전히 전개된 잎(8~9 cm)을 사용하여 관찰 및 측정하였다(RDA, 2017).

Fig. 1.
Leaf phenotype of 12 sweet potato varieties selected in this study. A, Hayanmi (Korea); B, Hopungmi (Korea); C, Sodammi (Korea); D, Sinhwangmi (Korea); E, Eunmi (Korea); F, Sinchunmi (Korea); G, Jinju local landrace (Korea); H, Uiryeong local landrace (Korea); I, Goseong local landrace (Korea); J, Beni Haruka (Japan); K, Shiroyudaka (Japan); L, Yamagawa Murasaki (Japan).
재배 방식에 따른 생리 특성 그리고 기공 특성 관찰 및 평가
식생지수는 RP410/UVIS (PHOTON SYSTEMS INSTRUMENTS, Czech Republic)를 사용하여 NDVI (Normalized difference vegetation index), MCARI (Modified chlorophyll absorption in reflectance index), G (Greenness index), CRI1 (Carotenoid reflectance index 1) 그리고 ARI1 (Anthocyanin reflectance index 1) 항목을 측정하였다. 광합성 특성은 FluorPen FP110 (PHOTON SYSTEMS INSTRUMENTS, Czech Republic)를 사용하여 Fv/Fm (Maximum quantum yield), ABS/RC (Absorption flux per PSII reaction center), TR0/RC (Trapped energy flux per PSII reaction center), ET0/RC (Electron transport flux per PSII reaction center) 그리고 DI0/RC (Dissipated energy flux per PSII reaction center) 항목을 측정하였다. 기공의 길이, 너비 그리고 밀도는 잎의 향축면 기공 표본을 매니큐어를 이용하여 채취한 후 위상차현미경(BX53 with DP-22, Olympus, Japan)을 이용해 관찰 및 측정하였다(Kang et al., 2023).
재배 방식에 따른 잎 조직 특성 관찰 및 평가
잎 조직은 Formalin-Aceto-Alcohol (Ricca Chemical Company, Arlington, USA) 용액으로 4주간 고정하였다. 고정 후 조직을 80% (2시간), 90% (2시간), 그리고 99% (12시간) 에탄올에 담가 탈수하였다. 탈수 조직의 투명화와 포매는 자일렌(4시간)과 65°C 파라핀(6시간)을 이용하여 처리하였다. 파라핀 블록은 마이크로톰(Minux S700 Rotary Microtome, RWD Life Science, China)을 이용하여 15 µm 두께로 박절하였다. 조직을 탈파라핀화(deparaffinization) 시키기 위하여 65°C 슬라이드 워머(XH-2016, Roundfin, China)에서 30분 가열 후 자일렌을 1시간 침투시켰다. 그 후 재수화(rehydration)는 99% (20분), 90% (5분), 70% (1분), 그리고 50% (1분) 에탄올에 순서대로 침지해 처리하였다. 조직은 0.5% safranin O solution (10분), 0.25% fast green solution (10분)을 이용하여 염색하였다(Singh et al., 2019). 염색된 조직은 위상차현미경(BX53 with DP-22, Olympus, Japan)으로 관찰하였고 잎 두께, 주엽맥의 두께와 너비, 관다발 두께와 너비, 물관 직경 그리고 책상세포의 두께를 관찰 및 측정하였다.
통계 분석
분산 분석(Analysis of Variance; ANOVA)과 주성분 분석(Principal component analysis; PCA)은 통계프로그램 Analyse-it (ver. 6.15, Analyse-it Software Ltd., United Kingdom)로 수행하였다. 부분 최소 제곱 판별 분석(Partial least squares discrimination analysis; PLS-DA)은 Python (ver. 3.10.11)의 pandas, scikit-learn, 그리고 matplotlib 라이브러리를 사용하여 수행하였다(Rohart et al., 2017). 그룹 간의 분리에 기여한 주요 특성을 확인하기 위하여 VIP (Variable Importance in Projection) 값을 계산하였으며, 0.9 이상일 경우 유의미한 주요인자로 선별하였다. 모든 평가 항목은 3반복으로 수행하였으며 5% 수준에서 유의성을 검정하였다.
결과 및 고찰
재배 방식과 품종에 따른 식생 지수, 광합성 및 기공 특성 평가
식생지수, 광합성특성 그리고 기공 특성은 식물의 활력, 스트레스 수준, 엽록체 활성 그리고 광합성량과 상관 있다(Stirbet & Govindjee, 2011; Lawson & Vialet-chabrand, 2018; Rosa et al., 2023). 식생지수, 광합성 특성 그리고 기공 특성의 차이가 재배 방식, 품종 그리고 재배 방식 및 품종의 상호작용에 따른 변이에 영향을 받았는지 평가한 결과, 식생지수인 NDVI와 CRI1는 재배 방식에 주로 영향을 받았으며 각각 전체 변이의 60.2%와 54.3%를 차지하였다. MCARI와 ARI1은 품종(25.5%와 6.9%), 재배 방식(24.7%와 50.1%), 그리고 둘의 상호작용(31.4%와 13.1%) 모두 영향을 받았다. G는 품종 및 재배 방식의 상호작용(31.4%)과 품종(25.5%)에 영향을 받았다(Table 1). 광합성 특성인 SPAD, Fv/Fm, ABS/RC, TR0/RC 그리고 DI0/RC는 재배 방식에 주로 영향을 받았으며, 각각 전체 변이의 45.3%, 50.1%, 45.0%, 42.1%, 그리고 37.9%를 차지하였다. ET0/RC는 주로 품종에 따른 영향을 받았으며, 전체 변이의 30.0%를 차지하였다 (Table 2). 기공의 길이, 너비 그리고 밀도는 주로 품종(29.9%, 31.4% 그리고 59.0%)에 영향을 받았으나 재배 방식 및 품종의 상호작용(24.3%, 15.1% 그리고 34.3%) 영향도 받았다(Table 3).
Table 1
Vegetative index according to cultivation method and variety.
| Cultivation method | Variety | NDVI | MCARI | G | CRI1 | ARI1 |
| Direct planting | Hayanmi | 0.79 | 0.13 | 1.63 | 6.39 | 2.35 |
| Hopungmi | 0.78 | 0.21 | 2.27 | 6.73 | 0.20 | |
| Sodammi | 0.76 | 0.23 | 2.46 | 7.12 | 0.04 | |
| Eunmi | 0.75 | -0.04 | 2.31 | 4.85 | -0.04 | |
| Sinhwangmi | 0.74 | -0.09 | 2.74 | 6.52 | -0.09 | |
| Sinchunmi | 0.76 | 0.06 | 2.30 | 6.72 | 6.72 | |
| Korea landrace (Jinju) | 0.77 | -0.24 | 2.07 | 6.60 | 6.60 | |
| Korea landrace (Uiryeong) | 0.78 | -0.31 | 2.37 | 7.16 | 7.16 | |
| Korea landrace (Goseong) | 0.78 | -0.25 | 2.50 | 7.84 | 7.84 | |
| Shiroyutaka | 0.75 | 0.35 | 2.05 | 6.68 | 6.68 | |
| Yamagawa murasaki | 0.77 | 0.14 | 2.29 | 7.15 | 7.15 | |
| Beni Haruka | 0.79 | -0.10 | 2.20 | 8.34 | 8.34 | |
| Transplanting | Hayanmi | 0.74 | 0.28 | 1.87 | 1.78 | 5.05 |
| Hopungmi | 0.72 | 0.27 | 1.87 | 2.20 | 4.50 | |
| Sodammi | 0.68 | 0.30 | 1.43 | 3.76 | 2.90 | |
| Eunmi | 0.68 | 0.32 | 2.52 | -0.14 | 4.75 | |
| Sinhwangmi | 0.70 | 0.16 | 2.15 | 0.16 | 4.20 | |
| Sinchunmi | 0.68 | 0.17 | 2.05 | -0.08 | 4.86 | |
| Korea landrace (Jinju) | 0.71 | 0.24 | 2.20 | 0.18 | 5.21 | |
| Korea landrace (Uiryeong) | 0.69 | 0.21 | 2.02 | 0.37 | 4.62 | |
| Korea landrace (Goseong) | 0.66 | 0.32 | 1.76 | 2.81 | 3.62 | |
| Shiroyutaka | 0.71 | 0.28 | 2.23 | 0.02 | 4.68 | |
| Yamagawa murasaki | 0.65 | 0.44 | 2.50 | 0.48 | 4.59 | |
| Beni Haruka | 0.73 | 0.32 | 2.15 | 0.93 | 5.73 | |
| Source of Variation | F-value† | |||||
| Cultivation method (C) | 142.04*** | 43.93*** | 9.19** | 119.36*** | 13.88*** | |
| Variety (V) | 2.76** | 4.47*** | 3.07** | 2.28* | 3.85*** | |
| C × V | 1.40ns | 3.37** | 3.78*** | 2.47* | 2.89** | |
| Source of Variation | R2 (%) | |||||
| Cultivation method (C) | 60.2 | 6.9 | 24.7 | 54.3 | 50.1 | |
| Variety (V) | 12.9 | 25.5 | 25.5 | 11.4 | 11.6 | |
| C × V | 6.5 | 31.4 | 31.4 | 12.4 | 13.1 | |
Table 2
Photosynthetic characteristics according to cultivation method and variety.
| Cultivation method | Variety | SPAD | Fv/Fm | ABS/RC | TR0/RC | ET0/RC | DI0/RC |
|
Direct planting | Hayanmi | 47.57 | 0.79 | 1.62 | 1.28 | 0.73 | 0.34 |
| Hopungmi | 42.53 | 0.80 | 1.67 | 1.33 | 0.78 | 0.34 | |
| Sodammi | 35.67 | 0.70 | 1.61 | 1.22 | 0.68 | 0.39 | |
| Eunmi | 49.73 | 0.82 | 1.41 | 1.16 | 0.71 | 0.25 | |
| Sinhwangmi | 44.93 | 0.81 | 1.32 | 1.07 | 0.82 | 0.25 | |
| Sinchunmi | 45.00 | 0.82 | 1.35 | 1.11 | 0.85 | 0.25 | |
| Korea landrace (Jinju) | 46.20 | 0.80 | 1.49 | 1.19 | 0.74 | 0.29 | |
| Korea landrace (Uiryeong) | 50.30 | 0.79 | 1.47 | 1.16 | 0.65 | 0.30 | |
| Korea landrace (Goseong) | 42.03 | 0.82 | 1.36 | 1.12 | 0.79 | 0.24 | |
| Shiroyutaka | 45.20 | 0.81 | 1.61 | 1.30 | 0.81 | 0.31 | |
| Yamagawa murasaki | 48.83 | 0.81 | 1.55 | 1.26 | 0.82 | 0.30 | |
| Beni Haruka | 41.93 | 0.80 | 1.74 | 1.39 | 0.82 | 0.36 | |
| Transplanting | Hayanmi | 33.60 | 0.48 | 3.47 | 1.69 | 0.34 | 1.79 |
| Hopungmi | 37.27 | 0.77 | 1.75 | 1.35 | 0.93 | 0.83 | |
| Sodammi | 31.93 | 0.70 | 2.45 | 1.62 | 0.79 | 0.40 | |
| Eunmi | 42.60 | 0.44 | 3.10 | 1.66 | 0.40 | 1.47 | |
| Sinhwangmi | 42.87 | 0.68 | 2.97 | 1.29 | 1.29 | 0.99 | |
| Sinchunmi | 36.13 | 0.65 | 3.07 | 1.30 | 1.30 | 1.33 | |
| Korea landrace (Jinju) | 37.53 | 0.65 | 2.53 | 1.58 | 0.50 | 0.94 | |
| Korea landrace (Uiryeong) | 40.63 | 0.51 | 3.38 | 1.65 | 0.43 | 1.73 | |
| Korea landrace (Goseong) | 35.17 | 0.66 | 2.60 | 1.66 | 0.55 | 0.93 | |
| Shiroyutaka | 37.00 | 0.64 | 3.34 | 2.04 | 0.92 | 1.30 | |
| Yamagawa murasaki | 36.00 | 0.60 | 2.61 | 1.58 | 0.61 | 1.03 | |
| Beni Haruka | 36.27 | 0.56 | 4.08 | 1.86 | 0.63 | 2.22 | |
| Source of Variation | F-value† | ||||||
| Cultivation method (C) | 134.48*** | 95.67*** | 54.85*** | 47.00*** | 0.43ns | 43.93*** | |
| Variety (V) | 8.18*** | 2.01* | 0.91ns | 0.64ns | 2.61* | 1.08ns | |
| C × V | 2.22* | 2.28* | 0.82ns | 0.88ns | 1.69ns | 1.03ns | |
| Source of Variation | R2 (%) | ||||||
| Cultivation method (C) | 45.3 | 50.1 | 45.0 | 42.1 | 0.5 | 37.9 | |
| Variety (V) | 30.3 | 11.6 | 8.2 | 8.7 | 30.0 | 10.4 | |
| C × V | 8.2 | 13.1 | 7.4 | 6.3 | 19.4 | 9.9 | |
Table 3
Adaxial stomatal trait according to cultivation method and variety.
| Cultivation method | Variety | Stomata length (μm) | Stomata width (μm) | Stomata density (No.) |
| Direct planting | Hayanmi | 23.06 | 14.56 | 423.67 |
| Hopungmi | 20.43 | 12.20 | 340.33 | |
| Sodammi | 22.32 | 14.82 | 269.57 | |
| Eunmi | 23.10 | 18.03 | 500.33 | |
| Sinhwangmi | 26.13 | 14.92 | 173.00 | |
| Sinchunmi | 26.70 | 15.91 | 413.00 | |
| Korea landrace (Jinju) | 30.59 | 16.98 | 437.33 | |
| Korea landrace (Uiryeong) | 29.22 | 19.30 | 288.33 | |
| Korea landrace (Goseong) | 20.06 | 12.84 | 488.00 | |
| Shiroyutaka | 33.74 | 17.47 | 282.33 | |
| Yamagawa murasaki | 27.40 | 16.24 | 196.33 | |
| Beni Haruka | 23.87 | 15.88 | 618.67 | |
| Transplanting | Hayanmi | 23.30 | 14.60 | 250.33 |
| Hopungmi | 28.03 | 16.95 | 213.00 | |
| Sodammi | 23.82 | 15.59 | 400.00 | |
| Eunmi | 31.55 | 22.42 | 398.00 | |
| Sinhwangmi | 30.33 | 17.33 | 224.00 | |
| Sinchunmi | 33.24 | 18.93 | 155.67 | |
| Korea landrace (Jinju) | 26.30 | 17.57 | 337.33 | |
| Korea landrace (Uiryeong) | 26.68 | 16.90 | 239.67 | |
| Korea landrace (Goseong) | 29.41 | 18.91 | 276.33 | |
| Shiroyutaka | 26.72 | 17.60 | 385.33 | |
| Yamagawa murasaki | 26.76 | 16.10 | 394.33 | |
| Beni Haruka | 26.35 | 18.55 | 470.33 | |
| Source of Variation | F-value† | |||
| Cultivation method (C) | 106.11*** | 135.30*** | 17.82*** | |
| Variety (V) | 33.30*** | 37.38*** | 19.90*** | |
| C × V | 35.80*** | 19.21*** | 18.74*** | |
| Source of Variation | R2 (%) | |||
| Cultivation method (C) | 6.0 | 9.5 | 0.2 | |
| Variety (V) | 29.9 | 31.4 | 59.0 | |
| C × V | 24.3 | 15.1 | 34.3 | |
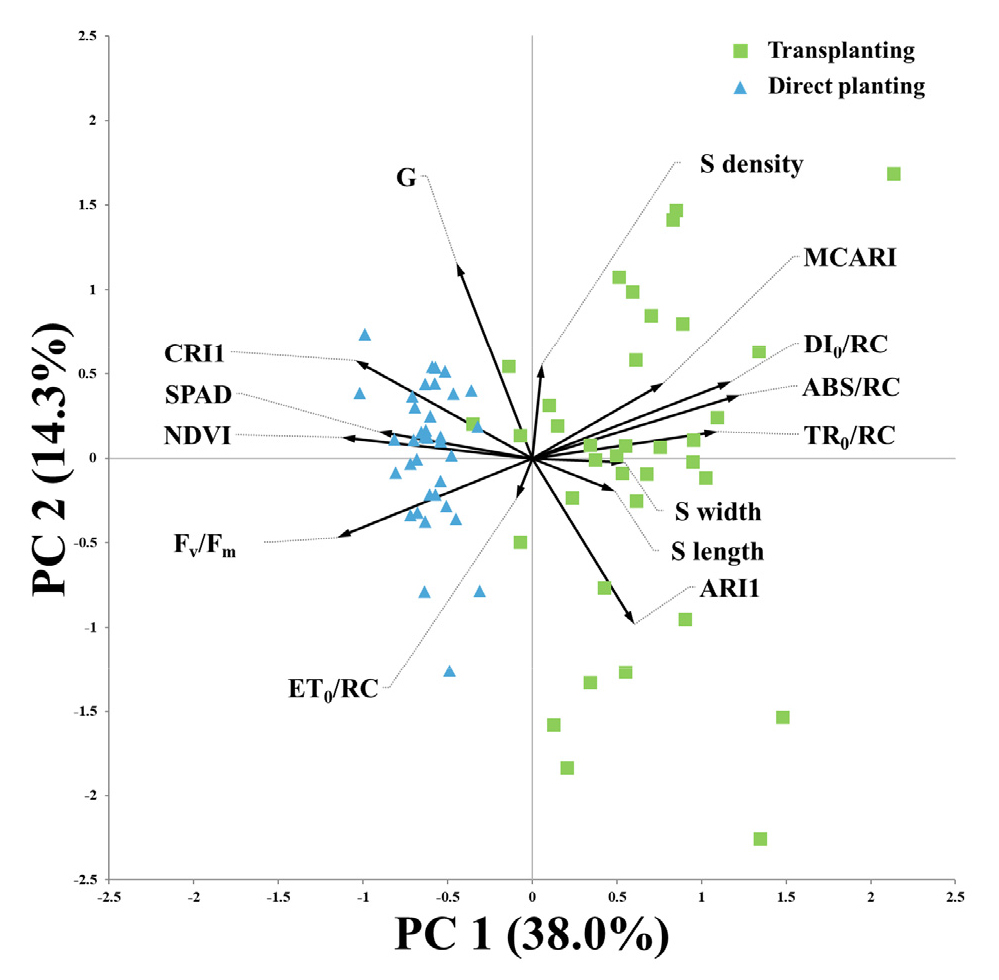
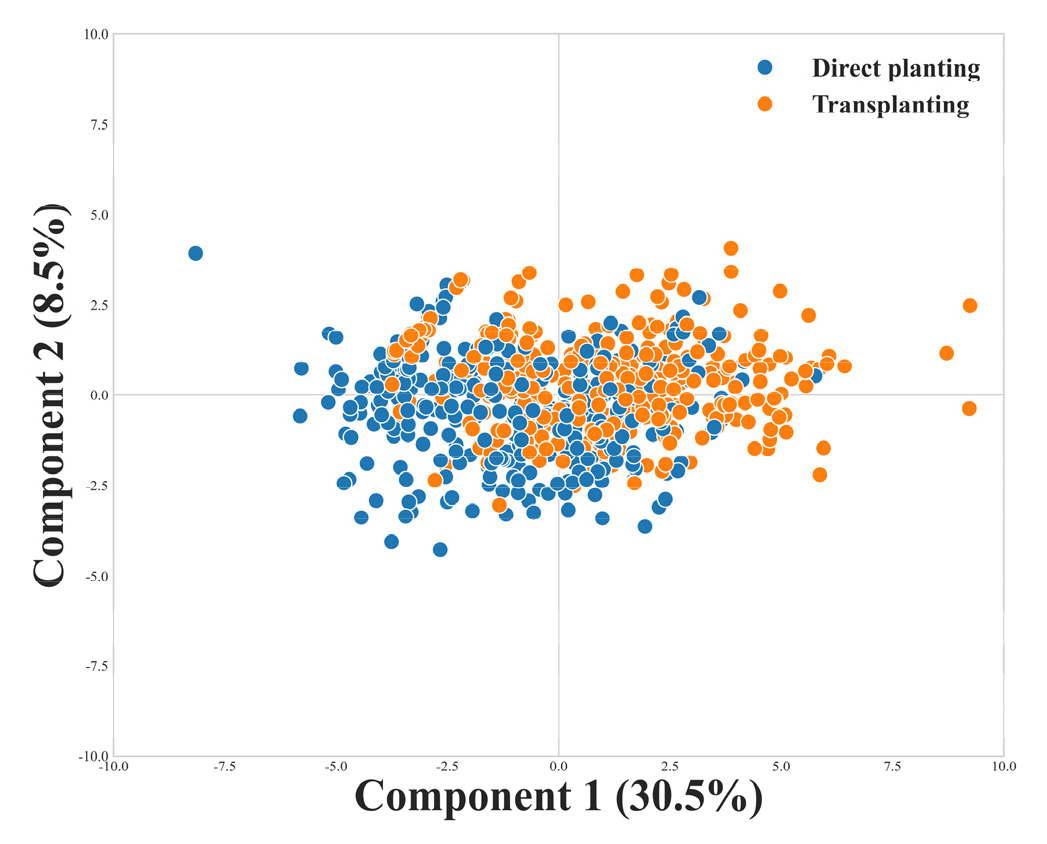
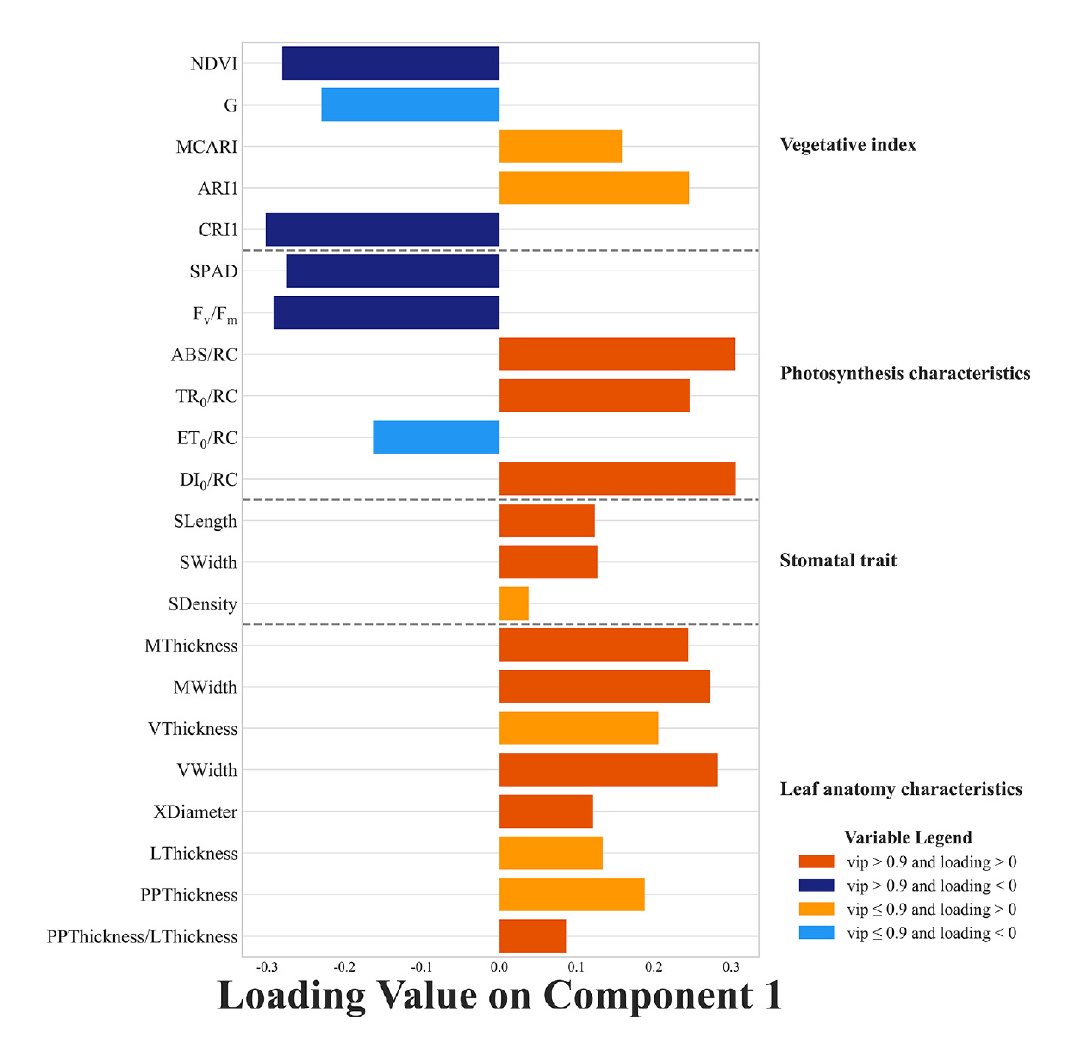
재배 방식에 따른 식생 지수, 광합성 및 기공 특성의 주성분 분석을 수행한 결과, 주성분(principal component; PC) 1과 2는 각각 38.0%와 14.3%의 설명력으로 식생 지수, 광합성 특성, 그리고 기공 특성 간 상관관계와 개체 간 분포를 확인하였다. PC 1 기준 삽식구는 양의 영역에 분포하였으며 직파구는 음의 영역에 분포하였다. 식생지수 MCARI, 광합성 지수 ABS/RC와 TR0/RC, 그리고 기공 길이와 너비는 PC 1과 양의 상관관계를 보였다. 식생지수 NDVI와 CRI1 그리고 광합성지수 SPAD와 Fv/Fm은 PC 1과 음의 상관관계를 보였다(Fig. 2). 직파구와 삽식구의 분리에 기여한 주요 변수(VIP > 0.9)를 확인하기 위하여 PLS-DA를 수행한 결과, 식생지수인 NDVI, CRI1, SPAD 그리고 광합성 특성인 Fv/Fm은 음의 로딩 값을 가졌으며 직파구에서 높았다. 반면, ABS/RC, TR0/RC 그리고 DI0/RC는 양의 로딩 값을 가졌으며 삽식구에서 높았다(Figs. 5~6).
삽식 재배에서는 직파에 비해 식물 활력(NDVI), 엽록소 함량(SPAD), 광합성 효율(Fv/Fm), 카로티노이드 지수(CRI1)가 유의미하게 낮았다 (Table 1 and Figs. 2, 6). 이는 삽식 재배에서 전반적인 건강 상태와 광합성 능력이 저조하며, 카로티노이드를 이용한 스트레스 방어 기작을 갖추지 못했음을 의미한다(Markwell et al., 1995; Niyogi, 1999; Maxwell & Johnson, 2000; Rosa et al., 2023). 또한, 삽식 재배에서 단위 반응 중심당 흡수·소산되는 에너지 양(ABS/RC와 DI0/RC)이 많았다(Table 2 and Figs. 2, 6). 이는 삽식 조건의 식물이 충분한 빛 에너지를 흡수하고 있으나 광합성에 효과적으로 사용하지 못하고 상당 부분을 열로 방출하는 비효율적인 상태에 있음을 의미한다(Maxwell & Johnson, 2000; Tsimilli-Michael, 2019). 이를 통하여 삽식 재배는 직파 재배보다 생육 및 에너지를 효율적으로 생산하기에 안정적이지 않으므로 초기 괴근 형성과 발달에 부정적인 영향을 끼친다고 설명할 수 있다(Wijewardana et al., 2018).
재배 방식과 품종에 따른 잎 조직 특성 평가
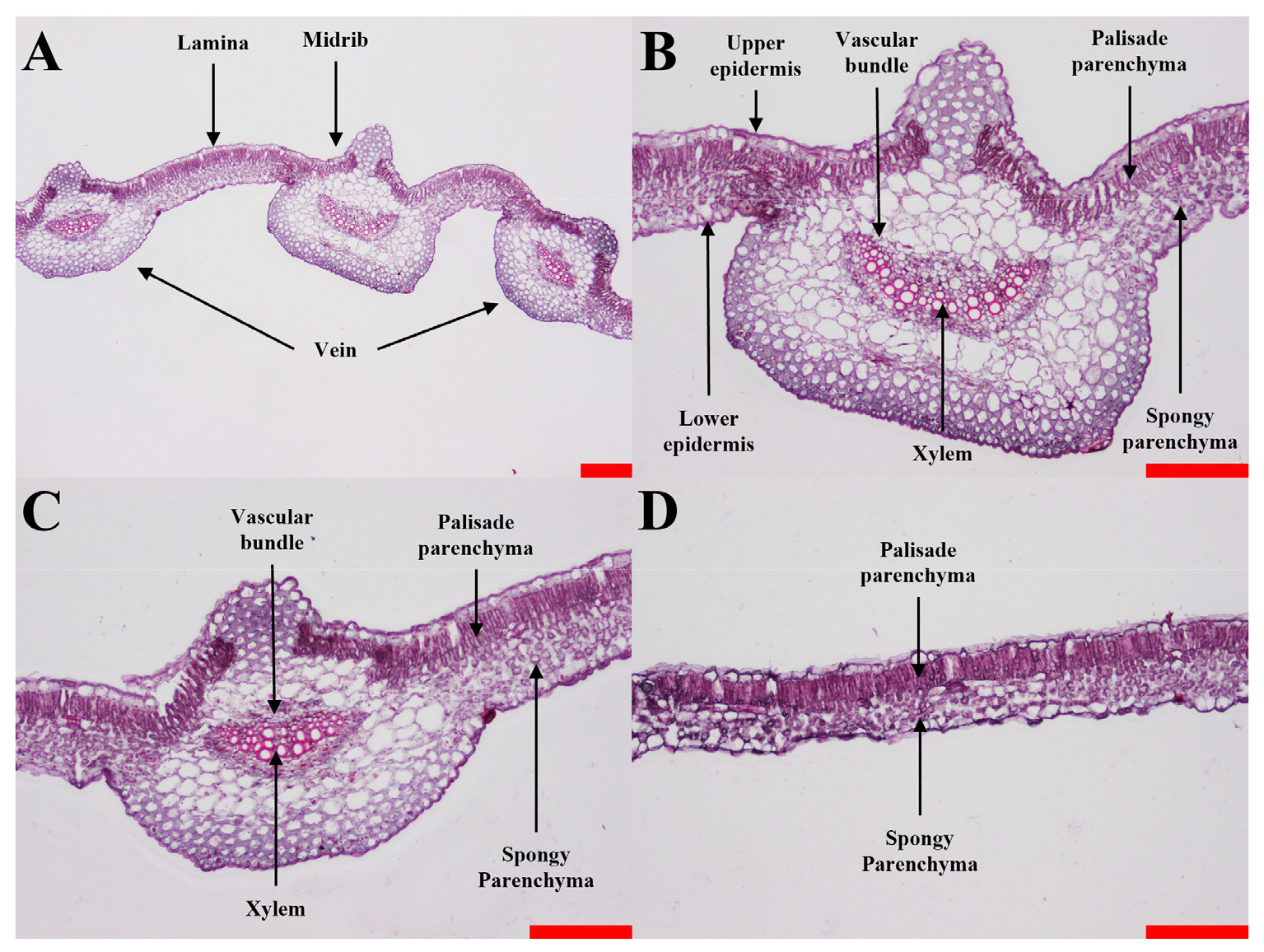
잎의 주엽맥과 관다발에서 수분 및 광합성 산물이 수송되며, 책상세포에는 당을 생산하는 엽록소가 분포한다(Urry et al., 2020). 재배 방식에 따른 잎 조직 특성의 차이가 재배 방식, 품종 그리고 재배 방식과 품종의 상호작용에 따른 변이에 영향을 받았는지 평가한 결과, 주엽맥과 관다발 두께는 품종에 주로 영향을 받았으며 각각 전체변이의 62.2%와 39.8%를 차지하였다. 주엽맥과 관다발의 너비는 품종(39.6%와 37.9%)에 주로 영향을 받았으나 재배 방식(20.1%와 28.1%)에도 영향을 받았다. 물관 직경, 잎 두께, 그리고 책상세포 두께는 주로 품종(34.0%, 21.8%, 그리고 14.7%)에 영향을 받았으나 재배 방식과 품종의 상호작용(13.1%, 13.5%, 그리고 6.9%)도 유의하였다(Table 4).
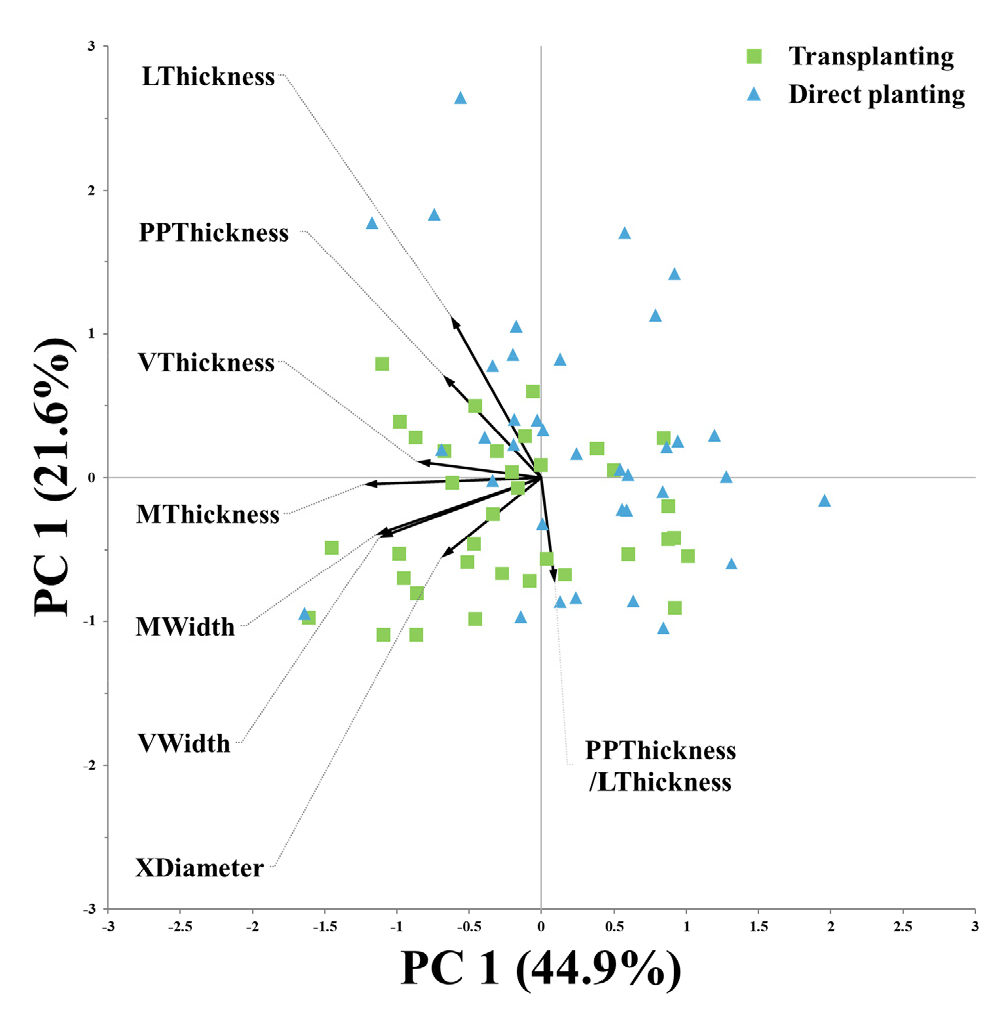
재배 방식에 따른 잎 조직 특성의 주성분 분석을 수행한 결과, PC 1과 2는 각각 44.9%와 21.6%의 설명력으로 잎 조직 특성 간 상관관계와 개체 간 분포를 확인하였다. PC 1 기준으로 직파구는 양의 영역에 분포하였으며 삽식구는 음의 영역에 분포하였다. PC 1과 음의 상관관계를 가지는 특성은 주엽맥 두께와 너비, 관다발 두께와 너비 그리고 물관 직경이었다. PC 2와 양의 상관관계를 가지는 특성은 잎의 두께와 책상세포 높이였으며 음의 상관관계를 가지는 특성은 책상세포 높이 비율이었다(Fig. 4). 직파구와 삽식구의 분리에 기여한 주요 잎 조직 특성(VIP > 0.9)을 확인하기 위하여 PLS-DA를 수행한 결과, 주엽맥의 두께와 너비, 관다발의 너비, 물관 직경, 책상세포 비율은 양의 로딩 값을 가졌으며 삽식구에서 발달하였다(Figs. 5~6).
삽식 재배한 잎은 직파 재배한 잎에 비해 수분과 양분의 수송에 관여하는 주엽맥, 관다발, 그리고 물관 조직들이 더 두껍고 넓게 발달하였다. 이는 삽식 조건에서 식물 전체로 에너지를 공급하고 수분을 수송하는 능력이 더 뛰어나다는 것을 설명한다(Sack & Frole, 2006). 또한, 광합성이 일어나는 책상조직의 두께도 삽식구에서 더 두꺼웠는데(Table 4 and Figs. 3~6), 이는 엽록소가 분포하여 빛 에너지를 얻을 수 있는 공간이 더 넓다는 것을 의미한다(Oguchi et al., 2003).
Table 4
Anatomical characteristics according to cultivation method and variety.
|
Cultivation method | Variety |
Midrib thickness (μm) |
Midrib width (μm) |
Vascular thickness (μm) |
Vascular width (μm) |
Xylem diameter (μm) |
Leaf thickness (μm) |
Palisade parenchyma thickness (μm) |
Palisade parenchyma thickness ratio (%) |
|
Direct planting | Hayanmi | 943.89 | 1164.31 | 202.28 | 569.38 | 39.58 | 130.32 | 48.95 | 37.60 |
| Hopungmi | 1267.21 | 1619.73 | 290.43 | 832.25 | 39.46 | 160.81 | 61.24 | 38.74 | |
| Sodammi | 934.01 | 1184.43 | 149.64 | 613.60 | 31.09 | 196.20 | 62.47 | 31.77 | |
| Eunmi | 980.18 | 1102.13 | 205.84 | 504.54 | 32.36 | 129.62 | 48.59 | 37.48 | |
| Sinhwangmi | 584.57 | 682.59 | 125.10 | 372.93 | 32.12 | 140.02 | 48.66 | 35.39 | |
| Sinchunmi | 675.73 | 909.40 | 157.71 | 534.85 | 35.16 | 144.79 | 54.01 | 37.23 | |
|
Korea landrace (Jinju) | 1042.10 | 1280.48 | 266.17 | 570.72 | 45.80 | 169.78 | 62.91 | 37.61 | |
|
Korea landrace (Uiryeong) | 1329.28 | 1326.91 | 277.98 | 735.90 | 47.76 | 218.20 | 71.49 | 32.82 | |
|
Korea landrace (Goseong) | 1001.27 | 1310.08 | 201.58 | 739.75 | 43.73 | 150.92 | 61.90 | 40.36 | |
| Shiroyutaka | 1385.23 | 1429.51 | 292.62 | 716.27 | 37.54 | 201.95 | 58.32 | 30.20 | |
|
Yamagawa murasaki | 1179.71 | 1112.57 | 271.74 | 614.88 | 40.07 | 196.55 | 67.13 | 33.97 | |
| Beni Haruka | 1074.60 | 1219.98 | 246.53 | 651.54 | 32.38 | 134.82 | 49.83 | 37.02 | |
| Transplanting | Hayanmi | 1142.93 | 1658.06 | 259.86 | 862.71 | 35.31 | 165.45 | 62.34 | 37.74 |
| Hopungmi | 1281.97 | 1578.72 | 207.79 | 946.02 | 40.87 | 190.72 | 68.64 | 36.11 | |
| Sodammi | 1271.10 | 1717.68 | 220.23 | 865.02 | 41.09 | 145.92 | 59.20 | 40.70 | |
| Eunmi | 607.72 | 1219.11 | 199.68 | 644.32 | 37.77 | 169.67 | 62.47 | 36.97 | |
| Sinhwangmi | 750.36 | 1010.93 | 152.30 | 599.31 | 34.54 | 158.44 | 60.83 | 38.54 | |
| Sinchunmi | 747.65 | 953.88 | 171.09 | 606.42 | 34.27 | 162.96 | 60.89 | 37.73 | |
| Korea landrace (Jinju) | 1177.53 | 1412.42 | 273.53 | 816.70 | 41.11 | 187.79 | 68.28 | 36.89 | |
|
Korea landrace (Uiryeong) | 1234.28 | 1486.42 | 277.89 | 844.99 | 41.95 | 164.75 | 60.89 | 37.41 | |
|
Korea landrace (Goseong) | 1525.81 | 2375.38 | 233.32 | 1245.44 | 50.22 | 167.70 | 57.98 | 34.71 | |
| Shiroyutaka | 1584.78 | 1846.86 | 184.56 | 1117.62 | 42.04 | 180.63 | 70.07 | 38.95 | |
|
Yamagawa murasaki | 1425.63 | 1960.12 | 217.30 | 1098.90 | 46.96 | 178.20 | 68.57 | 38.82 | |
| Beni Haruka | 1252.91 | 1846.73 | 209.33 | 829.04 | 42.22 | 120.01 | 46.99 | 39.27 | |
| Source of Variation | F-value† | ||||||||
| Cultivation method (C) | 15.26*** | 36.20*** | 0.32ns | 53.10*** | 44.77*** | 0.36ns | 12.23*** | 12.23*** | |
| Variety (V) | 11.89*** | 6.49*** | 4.06*** | 6.51** | 43.35*** | 21.31*** | 19.70*** | 19.70*** | |
| C × V | 1.49ns | 2.22* | 1.74ns | 1.48ns | 16.75*** | 13.23*** | 5.73*** | 5.73*** | |
| Source of Variation | R2 (%) | ||||||||
| Cultivation method (C) | 7.2 | 20.1 | 0.3 | 28.1 | 34.2 | 0.0 | 2.2 | 3.3 | |
| Variety (V) | 62.2 | 39.6 | 39.8 | 37.9 | 34.0 | 21.8 | 14.7 | 3.5 | |
| C × V | 7.8 | 13.6 | 17.1 | 8.6 | 13.1 | 13.5 | 6.9 | 14.3 | |
다만, 잎의 조직 특성은 품종간 편차가 유의했으며, 직파 재배 시 컸다. 이는 일부 품종의 경우 직파 재배를 해도 삽식 재배할 때 만큼 조직이 충분히 발달할 수 있음을 설명한다. 또한, 이러한 경향은 직파 시 품종에 따른 건물중 차이가 삽식할 때보다 컸고, 일부 품종의 경우 건물중이 삽식할 때보다 무거웠던 기존 연구와 일치하였다(Sakaigaichi et al., 2023).
이 연구는 재배 방식에 따른 고구마 생육 초기의 생리 및 조직 특성을 비교 분석하였다. 삽식 시 고구마 잎 조직 발달 양상이 우수하고 획득하는 빛 에너지 양이 많았으나, 직파할 때보다 열로 소산되는 에너지의 양이 많아 광합성 과정이 비효율적이었으며, 식물의 활력이 낮았고, 카로티노이드를 이용한 스트레스 방어기작을 갖추지 못했다. 이를 통해 삽식재배는 초기 생리 특성이 저해됐다고 설명할 수 있다. 따라서 삽식으로 인한 초기 생리 특성 저해를 경감하기 위한 후속 연구가 필요하다.
적 요
1.직파 재배 시 삽식 스트레스가 없는 안정적인 생육 환경으로 인해 높은 식물 활력(NDVI)과 광합성 효율(Fv/Fm)을 보였으며, 스트레스 방어와 연관된 카로티노이드 지수(CRI1)도 우수하였다.
2.삽식 재배는 단위 반응 중심당 빛 에너지 흡수량(ABS/RC)은 높았으나, 열 소실(DI₀/RC)도 많아 흡수한 에너지를 광합성에 효율적으로 사용하지 못했다.
3.삽식 재배에서 잎의 수분과 양분 수송 통로인 주맥과 관다발 조직은 더 두껍고 넓게 발달하여, 구조적으로 식물 전체에 자원을 공급하는 능력이 우수하였다.
4.삽식 스트레스로 인해 초기 생육기 생리 특성이 저해되며, 이러한 생육 저해를 경감하기 위한 후속 연구가 필요하다.