서 론
재료 및 방법
재료 및 시약
표준용액의 조제
시료 전처리
측정기기 및 기기분석 조건
결과 및 고찰
GC/MS 정성분석
직선성(Linearity)
품종별 밀리아신 함량
적 요
서 론
기장(Pacnicum miliaceum L.)은 조, 수수, 율무, 보리, 기장 등 소립종의 곡물을 통틀어 의미하는 Millet류에 속하는 잡곡이다(Kim et al., 2021). 다른 Millet류 곡물에 비해 단백질 및 무기질이 풍부하며(Choi et al., 2019), 항산화, 항비만 등 다양한 기능성 물질을 갖고 있는 것으로 알려져 있다(Kim et al., 2021). 쌀, 보리, 밀 등에 비해 생산량은 매우 적지만, 건강에 대한 관심이 증가함에 따라 다양한 곡물을 소비 하고자 하는 추세에 있어, 혼반용으로 이용이 가능한 조와 기장의 수요가 증가하고 있다(Choi et al., 2019).
특히 기장에는 유기화합물 부류에 속하는 주요 Triterpenoid인 밀리아신(Miliacin) 성분이 있으며, 이는 각질 세포의 대사와 증식을 촉진하는 것으로 알려져 있다(Boisnic et al., 2016). 선행연구에서는 세포 배양 연구에서 밀리아신이 DNA 단편화 정도를 감소시켜 비장세포에 대한 보호 효과를 나타내는 것으로 밝혔다(Panfilova et al., 2003). 또한, 밀리아신은 지질과산화의 활성화 및 지질과산화 생성물의 축적을 막는다고 알려져 있다(Panfilova et al., 2006). 밀리아신에 초점을 맞춘 최근 연구에서는 세포의 재생과 증식, 모발 성장과정을 촉진하여 여성의 탈모에 효과가 있는 것으로 나타났다(Boisnic et al., 2016). 이러한 밀리아신의 조직 수복 및 상처 치료의 특성으로 인해 피부과 연구에서 많은 관심을 불러일으키고 있다(Keophiphath et al., 2020).
이 연구에서는 기장과 조의 불검화물을 추출하여 분석하였다. 일반적으로 식물성 기름의 대부분은 트리글리세리드 (Triglyceride)로서 알칼리 처리를 해 가수분해하면 글리세롤과 지방산의 알칼리염으로 분해되는데, 이를 검화 반응이라고 한다(Lee & Lee, 2014). 이때 검화되지 않는 불검화 지질만을 추출하는 불검화물 추출 방법을 사용하여 분석하였다. 식물성 지질 Mass fraction의 98%를 차지하고 있는 Acylglycerol 때문에 측정 시에 방해 물질을 제거하지 않으면 정확한 측정이 불가능하게 되어(Kim et al., 2011) 검화 반응을 시켜 불검화물 추출 방법으로 분석하였다.
기장의 이화학적 성질에 관한 국내의 연구 동향을 살펴보면, 지질 및 지방산 조성에 관한 연구(Kim et al., 2010), 항산화 활성에 관한 연구(Park et al., 2020), 단백질 특성에 관한 연구(Ha & Lee, 2001) 등이 있는 정도이며 기장의 기능성 물질에 관한 연구는 적은 실정이다. 이 연구에서는 기장 5품종의 밀리아신 성분을 분석하였고, 함량 비교를 위한 조 2품종을 함께 분석하였으며, GC/MS 정성분석을 통해 트리테르페노이드(Triterpenoid)류 등의 성분들을 확인하였다. 이러한 연구는 기장을 여러 식품에 접목할 수 있도록 유용한 기초지식을 제공하고, 다양한 화장품, 식품을 개발하는 데 활용될 수 있을 것으로 기대된다.
재료 및 방법
재료 및 시약
본 연구에 사용된 시료는 밀양에 위치한 국립식량과학원 남부작물부 시험 포장에서 2021년도에 생산된 기장 한라찰, 올레찰, 연희찰, 이백찰, 황금기장 총 5품종과 조 삼다찰, 삼다메 2품종을 실험 재료로 이용하였다. 잡곡 도정기(LH-605SM, 이화산업사)를 이용하여 도정 후 시험용 분쇄기(Tube Mill control, IKA)로 분쇄하여 실험 재료로 사용하였다. 또한 실험 결과의 검증을 위해 표준물질로 Miliacin standard (Phytolab, Germany)을 사용하였다. 시험에 사용된 시약 중 Hexane과 Sodium sulfate anhydrous (Na2SO4)은 DAE JUNG사, Potassium hydroxide (KOH)은 Sigma-Aldrich (US)에서 구입하였으며, 모든 실험에 사용된 Deionized water는 Honeywell (US)에서 구입한 정제된 물을 사용하였다.
표준용액의 조제
표준물질 Miliacin은 Phytolab (Germany)사의 GC analytical grade를 구입하여 사용하였고, 순도는 ≥98.0%였다. 표준물질 Miliacin 10 mg을 정밀히 달아 Hexane 10 ml에 용해하여 1,000 μg/ml이 되도록 표준 원액을 조제하였고, 500 μg/ml, 300 μg/ml, 200 μg/ml, 100 μg/ml, 50 μg/ml, 25 μg/ml의 농도로 단계별 희석하여 사용하였다. 표준용액은 사용 시 조제하여 실험에 사용하였으며, 갈색 병에 담아 보관하였다.
시료 전처리
시료의 전처리 방법은 Fletouris의 방법을 참고하여, 기장 기름에 KOH 용액을 가해 직접 검화(saponification) 한 후 Hexane과 증류수를 이용하여 불검화물을 분획하여 추출하였다(Fletouris et al., 1998). 수확 후 기장과 조 종자를 도정 후 분쇄한 시료를 Soxhlet (BUCHI Korea)으로 추출한 기장 기름 100 mg에 KOH 2 ml을 가하였다. 항온수조(DAIHAN Scientific) 60℃에서 50분간 검화 시킨 후 추출물에 hexane 10 ml과 distilled water 10 ml을 가하였고, 약하게 흔들어 주어 층 분리를 시켰다(강하게 흔들 시 emulsion 발생). Hexane 층을 수집하였고, 이와 같은 과정을 3회 반복하여 총 30 ml의 hexane 층을 수집하였다. 1~2 g의 Sodium sulfate anhydrous를 넣은 여과 깔때기에 Hexane 층을 탈수 여과시켜 round-bottomed flask에 모았다. 여과된 hexane층을 회전 농축기(EYELA)를 이용하여 45℃ 수욕 상에서 완전히 농축한 후 잔류물을 2 ml hexane으로 재용해하였다. 추출물을 0.22 um PTFE syringe filter (Whatman, Clifton, NK, USA)로 여과 후 Table 1의 조건으로 GC/MS 분석하였다. 조성분석은 표준물질 및 NIST Library의 mass spectrum data와 표준물질의 retention time (RT)을 비교하여 확인하였다.
Table 1.
The analytical conditions of GC/MS for qualitative analysis.
|
Instrument
|
Parameters
|
Conditions
|
|
GC
|
Gas chromatography
|
Thermo Scientific Trace 1310
|
|
Capillary Column
|
Trace GOLD TG-5SilMS, 30 m × 0.25 mm × 0.25 μm
|
|
Carrier Gas
|
Helium at 1 ml/min
|
|
Septum purge flow
|
5 ml/min
|
|
Mode
|
Split, 20:1
|
|
Inlet temperature
|
250°C
|
|
MS transfer line
|
280°C
|
|
Oven temperature
|
Rate (°C/min)
|
Temp. (°C)
|
Hold (min)
|
Run (min)
|
|
Initial
|
150
|
1
|
1
|
|
20
|
210
|
0
|
4
|
|
4
|
310
|
1
|
30
|
|
25
|
315
|
5
|
35.2
|
|
MS
|
Instrument
|
Thermo Scientific ISQ 7000
|
|
Ionization
|
EI, 70 eV
|
|
Ion Source temperature
|
280°C
|
측정기기 및 기기분석 조건
GC/MS 장비는 Thermo Scientific사의 Gas chromatography Trace 1310과 결합된 ISQ7000 MSD 질량분석기를 사용하였으며, 칼럼은 Trace GOLD TG-5SilMS GC column, 30 m * 0.25 mm * 0.25 μm을 사용하였다. Injection volume은 1 μl이며, carrier gas는 Helium 1 ml/min으로 흘려주었고, split ratio 20:1, purge flow 5 ml/min으로 하였다. 주입구 온도는 250℃, ms transfer line 온도는 280℃로 설정하였다. 오븐의 시작 온도는 150℃에서 1분간 유지하였으며, 이후 210℃까지 20℃/min 승온하였다. 이후 310℃까지 4℃/min 승온 후 1분간 유지하였고, 크로마토그래피에서 분리된각 화합물의 정성분석을 위해 질량분석기를 사용하였으며, mass spectrum 확인을 위한 MS ionization voltage는 EI mode에서 70 eV였으며, ion source 온도는 280℃였다(Table 1).
결과 및 고찰
GC/MS 정성분석
Fig. 1은 확립된 전처리 방법 및 기기 분석 조건을 이용하여 기장 한라찰과 조 삼다메에서 추출한 성분의 GC-chromatogram의 결과이다. 기장에서는 약 14~18개의 peak, 조에서는 약 13~15개의 peak들을 관찰할 수 있었다. 스펙트럼 확인을 위해 GC/MS의 scan mode로 m/z 50~550 mass range에서 분석하였다. 검출된 성분들의 구조와 조성을 library search를 통해 확인한 결과 triterpene의 β-amyrine, lupeol, friedelan-3-one 지방산인 palmitic acid 등 외에 γ-sitosterol, heptacosane 등의 성분들이 검출되었다. Tables 2, 3, 4, 5, 6, 7, 8에 기장과 조의 품종별 검출된 밀리아신 제외 성분들의 library search 및 mass fragment 결과를 RT 순으로 나타내었다. 품종별 다양한 성분이 검출되었고, 그 중 한라찰에서는 pentacyclic triterpene인 β-amyrine과 friedelan-3-one이 검출된 것을 확인하였다. 이는 선행연구에서 기장에서 발견된 성분과 같음을 확인하였다(Bossard et al., 2013). 또한, 이백찰, 올레찰, 연희찰에서는 pentacyclic triterpene 중 lupeol, olean-12-ene이 검출되었다. Pentacyclic triterpne은 항염, 항바이러스, 항암 등이 효과가 뛰어나다고 알려져 있는 성분으로(Patocka, 2003) 추출 및 분석법의 추가적인 실험을 통해 기장에 포함된 pentacyclic triterpene 성분의 함량 분석 등의 연구가 필요할 것으로 보인다. 조 품종의 삼다메와 삼다찰에서는 기장의 품종과 비슷한 성분들이 검출되었지만 RT 26.00대의 peak는 확인되지 않았으며, 조에서는 밀리아신 함량이 검출되지 않았음을 알 수 있다.
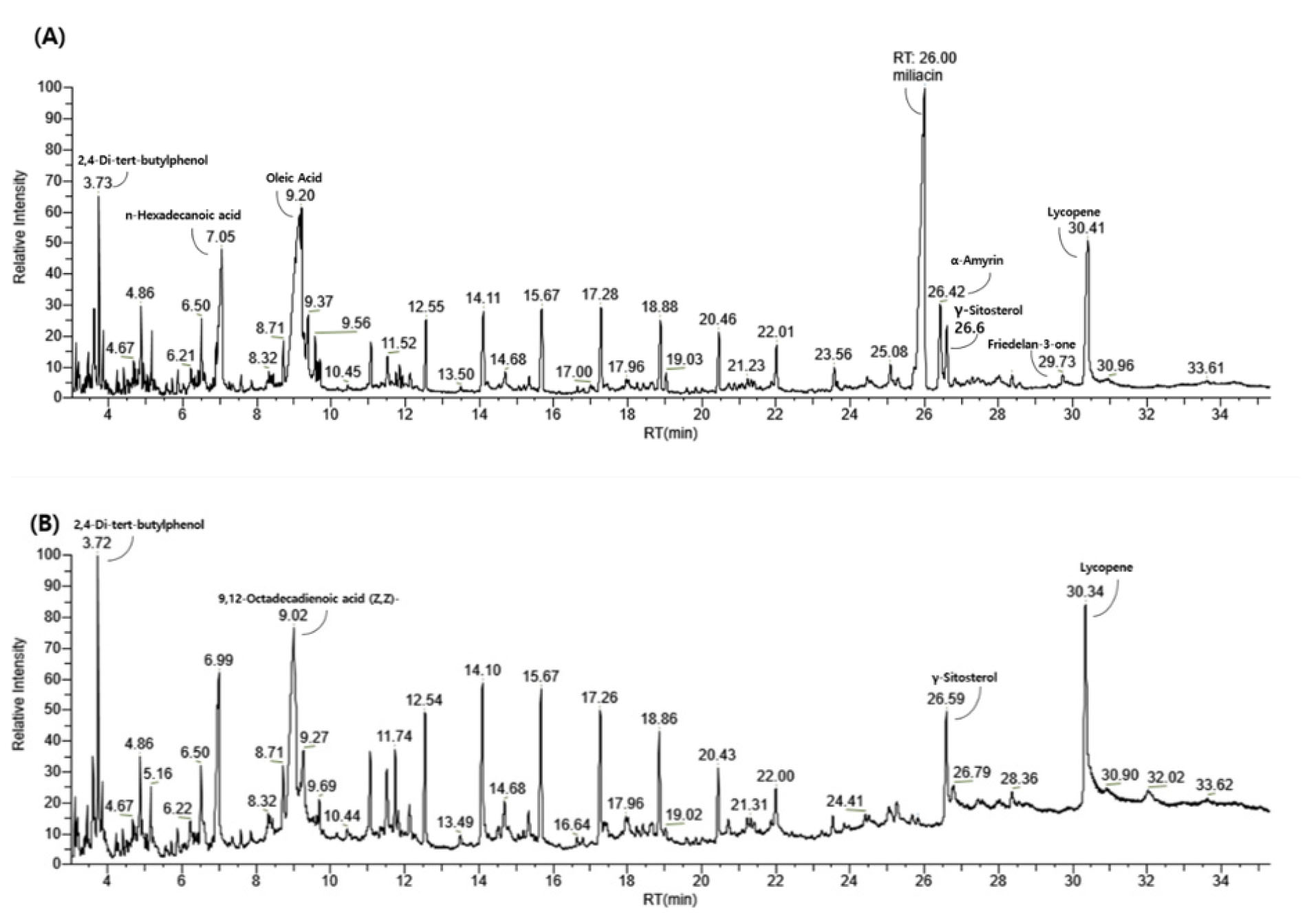
Fig. 1.
Chromatogram in scan mode of (A) Hallachall and (B) Samdame analyzed by GC/MS.
Table 2.
Chemical composition from Hallachal of proso millet by GC/MS scan mode (m/z 50~550).
|
RT
|
Constituents
|
Mass fragments
|
|
3.73
|
2,4-Di-tert-butylphenol
|
191z |
206y |
|
4.86
|
Eicosane, 2-methyl-
|
57
|
43
|
|
6.5
|
Octadecane, 2-methyl-
|
43
|
57
|
|
7.05
|
n-Hexadecanoic acid
|
73
|
60
|
|
9.2
|
6-Octadecenoic acid
|
55
|
97
|
|
11.52
|
Nonacosane
|
57
|
43
|
|
12.55
|
Tetracosane
|
57
|
43
|
|
14.11
|
Pentacosane
|
57
|
71
|
|
15.67
|
Octacosane
|
57
|
43
|
|
17.28
|
Tetratriacontane
|
57
|
71
|
|
18.88
|
Octacosane
|
43
|
57
|
|
20.46
|
Tetratriacontane
|
57
|
71
|
|
22.01
|
Tetratriacontane
|
57
|
71
|
|
26.42
|
β-Amyrin
|
218
|
203
|
|
26.6
|
γ-Sitosterol
|
414
|
107
|
|
29.73
|
Friedelan-3-one
|
69
|
109
|
|
30.41
|
Triptolide, TMS
|
73
|
75
|
Table 3.
Chemical composition from Hwanggeum of proso millet by GC/MS scan mode (m/z 50~550).
|
RT
|
Constituents
|
Mass fragments
|
|
3.72
|
2,4-Di-tert-butylphenol
|
191z |
206y |
|
4.86
|
Eicosane, 2-methyl-
|
57
|
43
|
|
6.5
|
Pentacosane
|
57
|
71
|
|
6.97
|
Hexadecanoic acid
|
73
|
60
|
|
9.24
|
Octadecanoic acid
|
43
|
73
|
|
11.52
|
Nonacosane
|
57
|
43
|
|
12.6
|
Tetracosane
|
57
|
71
|
|
14.16
|
Pentacosane
|
57
|
71
|
|
15.74
|
Tetratriacontane
|
57
|
71
|
|
17.33
|
Tetratriacontane
|
57
|
71
|
|
18.92
|
Tetratriacontane
|
57
|
71
|
|
20.49
|
Tetratriacontane
|
57
|
71
|
|
22.03
|
Tetratriacontane
|
57
|
71
|
|
26.4
|
Betulinaldehyde
|
189
|
135
|
|
26.58
|
γ-Sitosterol
|
43
|
55
|
|
29.88
|
Octadecane
|
57
|
207
|
|
30.38
|
Ginkgolide B 3TMS
|
73
|
147
|
Table 4.
Chemical composition from Ibaekchal of proso millet by GC/MS scan mode (m/z 50~550).
|
RT
|
Constituents
|
Mass fragments
|
|
3.72
|
2,4-Di-tert-butylphenol
|
191z |
206y |
|
4.86
|
Heptadecane, 2-methyl
|
43
|
57
|
|
7.12
|
n-Hexadecanoic acid
|
73
|
60
|
|
11.88
|
Butyl 9,12-octadecadienoate
|
67
|
81
|
|
14.11
|
Pentacosane
|
57
|
71
|
|
15.68
|
Tetratriacontane
|
57
|
71
|
|
17.28
|
Tetratriacontane
|
57
|
71
|
|
19.05
|
Supraene
|
69
|
81
|
|
20.45
|
Nonacosane
|
57
|
43
|
|
22
|
Nonacosane
|
57
|
43
|
|
26.42
|
Lupeol, methyl ether
|
95
|
109
|
|
26.59
|
γ-Sitosterol
|
414
|
107
|
|
28.36
|
Ethyl iso-allocholate
|
43
|
55
|
|
28.74
|
Olean-12-ene
|
57
|
207
|
|
30.36
|
Triptolide, TMS
|
73
|
75
|
Table 5.
Chemical composition from Ollechal of proso millet by GC/MS scan mode (m/z 50~550).
|
RT
|
Constituents
|
Mass fragments
|
|
3.72
|
2,4-Di-tert-butylphenol
|
191z |
206y |
|
4.86
|
Eicosane, 2-methyl-
|
57
|
43
|
|
7.07
|
n-Hexadecanoic acid
|
73
|
60
|
|
11.53
|
Octadecane,
|
43
|
57
|
|
14.08
|
Pentacosane
|
57
|
71
|
|
15.66
|
Nonacosane
|
57
|
43
|
|
17.26
|
Heptacosane
|
57
|
43
|
|
18.86
|
Nonacosane
|
57
|
43
|
|
20.44
|
Nonacosane
|
57
|
43
|
|
22.01
|
Nonacosane
|
57
|
43
|
|
26.41
|
Lupeol, methyl ether
|
95
|
189
|
|
26.6
|
γ-Sitosterol
|
414
|
107
|
|
28.58
|
Olean-12-ene
|
57
|
207
|
|
30.38
|
Triptolide, TMS
|
73
|
75
|
Table 6.
Chemical composition from Yeonheechal of proso millet by GC/MS scan mode (m/z 50~550).
|
RT
|
Constituents
|
Mass fragments
|
|
3.72
|
2,4-Di-tert-butylphenol
|
191
|
206
|
|
4.86
|
Eicosane, 2-methyl-
|
57
|
43
|
|
7.21
|
n-Hexadecanoic acid
|
73
|
60
|
|
8.41
|
9,12-Octadecadienoic acid (Z,Z)-,
|
67
|
81
|
|
9.64
|
9,12-Octadecadienoic acid (Z,Z)-
|
67
|
81
|
|
11.93
|
Butyl 9,12-octadecadienoate
|
67
|
81
|
|
14.14
|
Pentacosane
|
57
|
71
|
|
15.7
|
Tetratriacontane
|
57
|
71
|
|
17.29
|
Nonacosane
|
57
|
43
|
|
19.08
|
Supraene
|
69
|
81
|
|
20.45
|
Nonacosane
|
57
|
43
|
|
26.42
|
Lupeol, methyl ether
|
95
|
189
|
|
26.6
|
γ-Sitosterol
|
414
|
107
|
|
28.56
|
Olean-12-ene
|
57
|
207
|
|
30.37
|
Triptolide, TMS
|
73
|
75
|
Table 7.
Chemical composition from Samdachal of foxtail millet by GC/MS scan mode (m/z 50~550).
|
RT
|
Constituents
|
Mass fragments
|
|
3.72
|
2,4-Di-tert-butylphenol
|
191z |
206y |
|
4.86
|
Hexadecane, 2-methyl-
|
57
|
43
|
|
6.98
|
n-Hexadecanoic acid
|
73
|
60
|
|
8.98
|
9,12-Octadecadienoic acid (Z,Z)-
|
67
|
81
|
|
9.25
|
Oxiraneoctanoic acid
|
55
|
41
|
|
11.51
|
Nonacosane
|
57
|
43
|
|
12.53
|
Tetracosane
|
57
|
43
|
|
14.07
|
Pentacosane
|
57
|
71
|
|
15.66
|
Tetratriacontane
|
57
|
71
|
|
17.25
|
Heptacosane
|
57
|
43
|
|
18.85
|
Nonacosane
|
57
|
43
|
|
26.59
|
γ-Sitosterol
|
414
|
107
|
|
30.35
|
Triptolide, TMS
|
73
|
75
|
Table 8.
Chemical composition from Samdamae of foxtail millet by GC/MS scan mode (m/z 50~550).
|
RT
|
Constituents
|
Mass fragments
|
|
3.72
|
2,4-Di-tert-butylphenol
|
191z |
206y |
|
4.86
|
Eicosane, 2-methyl-
|
57
|
43
|
|
6.99
|
n-Hexadecanoic acid
|
73
|
60
|
|
9.02
|
9,12-Octadecadienoic acid
|
67
|
81
|
|
9.27
|
L-Ascorbic acid, 6-octadecanoate
|
57
|
43
|
|
12.54
|
Tetracosane
|
57
|
43
|
|
14.1
|
Pentacosane
|
57
|
71
|
|
15.67
|
Octacosane
|
57
|
43
|
|
17.26
|
Tetratriacontane
|
57
|
71
|
|
18.86
|
Octacosane
|
57
|
43
|
|
20.43
|
Nonacosane
|
57
|
43
|
|
26.59
|
γ-Sitosterol
|
414
|
107
|
|
26.79
|
β-Sitosterol
|
43
|
55
|
|
30.34
|
Tris(2,4-di-tert-butylphenyl) phosphate
|
57
|
647
|
직선성(Linearity)
밀리아신 표준용액을 농도가 25, 50, 100, 200, 300, 500μg/ml이 되도록 제조하여 GC/MS로 분석하였다. 성분의 농도에 따른 피크의 면적을 이용하여 검량선을 작성한 결과 Fig. 2에 나타난 것과 같이 직선식은 Y=1.765e6x+3.062e7, 상관계수(R2)가 0.999 이상으로 양호한 직선성을 나타내었다. 각 시료에서의 밀리아신 농도는 이 검량선을 이용하여 정량하였다.
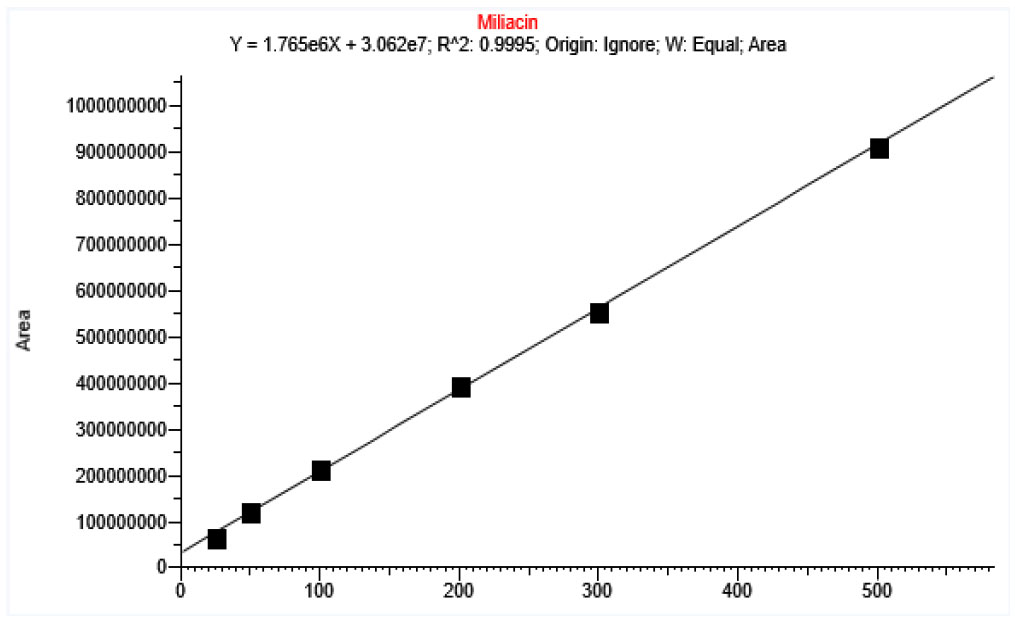
Fig. 2.
Calibration curve of miliacin standard solution.
품종별 밀리아신 함량
밀리아신 표준물질을 GC로 측정한 Chromatogram 결과 RT 26.00로 나타났으며, MS spectrum 결과 분자량 440.3이 Fig. 3과 같이 확인되었다. 추출 및 분석은 3반복을 진행하였고, 검량선을 통해 평균 정량값을 계산하였다. 그 결과, 한라찰 품종이 평균 370.38±0.04 μg/100 mg oil로 기장 품종 중 가장 높은 함량을 나타내었다. 다음으로 올레찰 평균 237.26±0.42 μg/100 mg oil, 연희찰 평균 167.62±0.22 μg/100 mg oil, 이백찰 평균 151.88±0.58 μg/100 mg oil 순으로 밀리아신함량이 높게 나타났으며, 황금기장에서 평균 78.76±0.17 μg/100 mg oil으로 가장 낮은 함량을 나타내었다. 조 품종인 삼다찰과 삼다메에서는 밀리아신 함량이 검출되지 않았다(Table 9). 즉, 밀리아신 성분은 기장의 품종에서만 검출되는 것을 확인하였다.
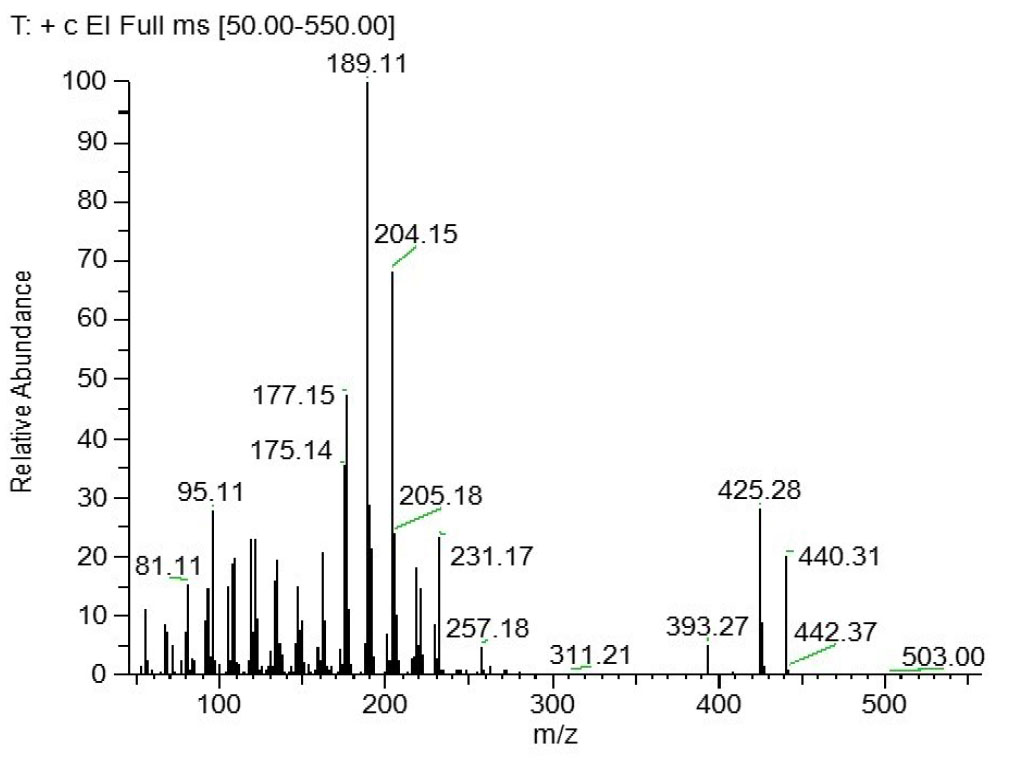
Fig. 3.
MS spectrum of miliacin analyzed by GC/MS.
Table 9.
Quantification of miliacin contents for each varieties.
|
Millet sample
|
Variety
|
Miliacin (μg/100 mg oil)
|
Average ± SD
|
|
n=3
|
|
Proso millet
|
Hallachal
|
370.37
|
370.34
|
370.42
|
370.38±0.04
|
|
Hwanggeum
|
78.78
|
78.59
|
78.92
|
78.76±0.17
|
|
Ibaekchal
|
152.28
|
151.21
|
152.14
|
151.88±0.58
|
|
Ollechal
|
236.88
|
237.71
|
237.18
|
237.26±0.42
|
|
Yeonheechal
|
167.87
|
167.55
|
167.45
|
167.62±0.22
|
|
Foxtail millet
|
Samdachal
|
ND
|
ND
|
ND
|
ND
|
|
Samdamae
|
ND
|
ND
|
ND
|
ND
|
본 연구를 통해 밀리아신 성분은 기장의 target 물질로 추측할 수 있으며, 이후에 추가적인 밀렛류의 분석 및 기장의 종실뿐만 아니라 잎, 줄기 등의 추가적인 연구가 필요할 것으로 생각된다. 또한, 기장의 탈모 예방 효과를 위하여 먹는 약이나 식품, 화장품 등으 로의 개발하는데 필요한 기초자료로 활용할 수 있을 것으로 기대된다.
적 요
기장에 있는 트리테르페노이드류인 밀리아신 성분은 각질 세포의 증식을 촉진하는 등의 특성을 가지고 있어 탈모에 효과가 있다고 알려져 있다. 이 연구에서는 기장의 기름을 추출하여 검화 반응을 거쳐 불검화물의 추출 방법을 이용하여 GC/MS로 분석하였다. 기장 기름 성분을 GC/MS의 정성분석을 통해 확인하였으며, 기장 5품종과 비교를 위한 조 2품종의 밀리아신 함량을 분석하였다.
1.기장에서는 β-amyrine, lupeol 등의 pentacyclic triterpene류의 성분들이 검출되었다.
2.밀리아신 함량은 기장의 한라찰에서 370.38±0.04 μg/100 mg oil으로 가장 높은 함량을 나타내었다.
3.특히 조의 품종인 삼다찰과 삼다메에서는 밀리아신 함량이 검출되지 않았다.
Acknowledgements
본 연구는 농촌진흥청 국립식량과학원 연구 사업(과제명: 기능성 고함유 잡곡 실용화 모델 개발, 과제번호: PJ014565012022)의 지원에 의해 이루어진 결과의 일부이며, 이에 감사드립니다.
References
Boisnic, S., M. C. Branchet, E. Gaillard, and I. Lamour. 2016. Miliacin associated with polar lipids: effect on growth factors excretion and extracellular matrix of the dermal papilla hair follicle model maintained in survival conditions. Hair Ther Transplant, 6(143) : 2167-0951.
Bossard, N., J. Jacob, C. Le Milbeau, J. Sauze, V. Terwilliger, B. Poissonnier, and E. Vergès. 2013. Distribution of miliacin (olean-18-en-3β-ol methyl ether) and related compounds in broomcorn millet (Panicum miliaceum) and other reputed sources: Implications for the use of sedimentary miliacin as a tracer of millet. Organic geochemistry. 63(1) : 48-55.
10.1016/j.orggeochem.2013.07.012Choi, J. M., D. Y. Kwak, M. E. Choe, S. B. Song, C. H. Park, and K. Y. Ko. 2019. Nutritional Compositions of Varieties of Foxtail millet and Proso millet Developed in Korea. Korean Journal of Crop Science. 64(2) : 137-143.
Fletouris, D. J., N. A. Botsoglou, I. E. Psomas, and A. I. Mantis. 1998. Rapid determination of cholesterol in milk and milk products by direct saponification and capillary gas chromatography. Journal of Dairy Science. 81(11) : 2833-2840.
10.3168/jds.S0022-0302(98)75842-49839224Ha, Y. D. and S. P. Lee. 2001. Characteristics of proteins in Italian millet, sorghum and common millet. Korean J Postharvest Sci Technol. 8(2) : 187-192.
Keophiphath, M., C. Courbière, L. Manzato, I. Lamour, and E. Gaillard. 2020. Miliacin encapsulated by polar lipids stimulates cell proliferation in hair bulb and improves telogen effluvium in women. Journal of cosmetic dermatology. 19(2) : 485-493.
10.1111/jocd.1299831135099Kim, H. J., K. S. Woo, J. Y. Lee, J. H. Choo, B. W. Lee, Y. Y. Lee, and M. S. Kang. 2021. Functional Compounds and Physiological Activities of Proso Millet Cultivars. Journal of the Korean Society of Food Science and Nutrition. 50(7) : 692-698.
10.3746/jkfn.2021.50.7.692Kim, J. M., J. M. Park, T. H. Yoon, D. G. Leem, C. Y. Yoon, J. Y. Jeong, and J. H. Ahn. 2011. Development of analysis method for cholesterol in infant formula by direct saponification. Food Science of Animal Resources. 31(6) : 944-951.
10.5851/kosfa.2011.31.6.944Kim, S. M., Q. Y. Zhang, X. Z. Yu, S. T. Yoon, S. J. Ji, and J. B. Kim. 2010. Fatty acids composition of foxtail millet (Setaria italica BEAUVOIS) seeds collected in South Korea. Korean Journal of Medicinal Crop Science. 18(6) : 405-408.
Lee, S. H. and K. Y. Lee. 2014. Effect of Drying Time and Additives regarding the Physical Properties of Vegetable Fatty Acid Soap. Journal of the Korea Academia-Industrial cooperation Society. 15(6) : 4032-4038.
10.5762/KAIS.2014.15.6.4032Panfilova, T. V., A. A. Shtil, E. R. Polosukhina, A. Y. Baryshnikov, and B. A. Frolov. 2003. Effect of the triterpenoid miliacin on the sensitivity of lymphocytes in the thymus and spleen to dexamethasone-induced apoptosis. Bulletin of experimental biology and medicine, 136(4) : 336-339.
10.1023/B:BEBM.0000010945.81238.b614714076Panfilova, T. V., A. A. Shtil, and B. A. Frolov. 2006. Triterpenoid miliacin inhibits stress-induced lipid peroxidation. Bulletin of experimental biology and medicine. 141(6) : 685-687.
10.1007/s10517-006-0252-717364049Park, J. S., J. S. Lee, and J. H. Lee. 2020. Antioxidative and antimutagenic effects of Panicum miliaceum L. Korean Journal of Food Preservation. 27(2) : 261-269.
10.11002/kjfp.2020.27.2.261Patocka, J. 2003. Biologically active pentacyclic triterpenes and their current medicine signification. Journal of Applied Biomedicine. 1(1) : 7-12.
10.32725/jab.2003.002






