벼(Oryza sativa L.)는 우리나라의 주곡 작물로 지난 5,000 여 년간 재배되어왔으나 최근 1인당 연간 쌀 소비량의 급 격한 감소와 쌀 시장 개방으로 인하여 국내 쌀 산업은 어려 움을 겪고 있다. 이에 대응하기 위하여 소비자의 기호에 부 응하는 다양한 특성의 신품종이 개발, 보급되고 있는데, 건 강 기능성이 강화된 품종들과 더불어 독특한 향기가 나는 향미벼가 이에 포함되고 있다.
향미벼는 향기성분과 재배지역 및 쌀 모양을 고려하여 Basmati type과 Jasmin type으로 분류가 된다(Singh et al., 2000). Basmati type의 주요 향기성분은 2-acetyl-1-pyrroline과 2-phenylethanol이며, 재배지역은 인도, 파키스탄, 방글라데 시 등이며, 쌀 모양은 Jasmin type 보다 쌀알이 가늘고 길 다고 알려져 있다. 반면 Jasmin type의 주요 향기성분은 2-acetyl-1-pyrroline과 indole이며, 재배지역은 태국 등으로 알려져 있다. 향미벼는 팝콘 향 또는 독특한 향기를 발산하 는 벼로 인도, 방글라데시 등 동남아시아에서 주로 재배되 어왔으며 다양한 식품소재로도 활용되어 왔다(Buttery et al., 1986). 한편 국내에서의 향미벼에 대한 선호도는 동남 아시아 국가보다는 낮으나, 이용 확대를 위해 1993년 ‘향미 벼1호’의 개발(Choi et al., 1995)을 비롯하여 다양한 향기 특성 및 유전 연구가 진행되고 있다(Kim et al., 2009, Lee et al., 1991, Lee et al., 2003). 향미벼의 주요 방향성 물질 에 대한 연구는 Buttery et al. (1986)의 보고 이후 체계적으 로 진행되어 왔으며, 특히 최근 분석기기의 발전에 힘입어 현재 약 200여 종의 성분이 보고되고 있다(Bryant and McClung, 2011). 향미벼의 주요한 방향 성분으로는 팝콘향 을 내는 2-acetyl-1-pyrroline(2AP)이 알려져 있는데, 2AP 는 betaine aldehyde dehydrogenase (BADH2) 유전자의 이 상으로 생성되는 것으로 보고되고 있다(Grimm et al., 2001, Jezussek et al., 2002, Kovach et al., 2009).
국내 소비자들의 소득 수준의 향상은 단순히 식량원으로 서의 쌀에서 건강 기능성이 부여된 기능성 쌀의 수요를 꾸 준히 상승시켜왔고, 이에 부응하여 anthocyanin과 phenolics의 함량이 높은 유색미를 비롯하여 vitamin E와 oryzanol 함량 이 높은 거대배아미 등 다양한 품종이 개발되고 있으며 아 울러 새로이 개발된 품종의 생리활성에 대한 연구 역시 활 발하게 이루어지고 있다(Kim et al., 2010, Sung et al., 2013).
발아 현미 역시 많은 연구가 진행된 벼의 기능성 분야이 다. 벼는 영을 제거하여 현미를 만들고 이를 다시 도정하 여 생산된 백미의 형태로 주로 유통되고 또 소비된다. 도 정 과정 중 제거되는 미강에는 비타민 B1, B2, tocols, squalene, phytosterols, oryzanol 등 많은 생리활성물질이 포함되어 있는 만큼, 현미는 백미에 비해 영양가가 높다. 그러나 현 미는 쌀보다 식감이 거칠 뿐 아니라 영양 성분의 소화 흡 수율이 낮아 소비자의 기호가 낮다(Moon et al., 2010, Sung et al., 2013). 이러한 현미의 단점을 개선하기 위해 현미를 발아시킨 것이 발아현미이다. 현미는 발아 과정에서 γ -aminobutyric acid(GABA)와 arabinoxylan 등 기능성물질 의 함량이 높아지고, 소화를 억제시키는 것으로 알려진 phytic acid 등이 감소되어 소화율이 높아지고 동시에 조직 이 연화되어 식미감이 개선되는 것으로 보고되고 있다(Kim 2014, Kim et al., 2001, Kim et al., 2012, Kwak et al., 2013, Lee et al., 2011, Oh et al., 2010, Sung et al., 2013).
본 연구는 발아 향미의 실용성을 검토를 위하여 발아 과 정 중 향기 성분과 기능성 지질성분 함량의 변화를 구명하 고자 수행되었다.
재료 및 방법
실험재료
본 실험의 재료로는 2016년도에 특허 출원된 향미벼 ‘천 지향1세(Cheonjihyang-1 se)’를 사용하였다. ‘천지향1세’는 향기 특성을 갖는 향미벼로서, 주남벼 및 추청벼//유메츠쿠 시/ 재래 향미 교배후대 계통의 교배후대 향미 계통을 모본 으로 하고, 추청벼//유메츠쿠시/ 재래 향미 계통을 부본으로 하여 인공교배하여 육성되었으며 15%-20%의 아밀로즈 함 량과 70 - 75의 도요식미 값 특성을 갖고 있는 품종이다. 2014년도에 수확된 종자를 2015년도에 재배하였는데, 48 시간 최아시켜 육묘상자에 파종하여 2주간 비닐온실에서, 2주는 실외에서 육묘된 유묘를 이앙하였으며 이후는 농촌 진흥청의 표준 재배법에 준하여 재배하였다. 2015년도 가 을에 수확된 종자는 수분 함량 15%로 건조한 후 약 6개월 간 4°C의 저온 저장고에 보관하며 발아현미의 제조에 이용 하였다
발아 현미 제조
향미벼를 이용하여 발아현미를 제조하였을 때의 향기성 분 및 생리활성물질의 함량 변화를 평가하기 위하여 현미 를 세척 후, 6시간 동안 실온에서 침지하고, 이를 순환식 showering이 되는 발아조에 넣은 후 38°C의 incubator에 넣었다. 12시간 후 순환되는 물을 교체하고 다시 12시간을 더 발아시켰다. 발아 전 시료 및 발아가 완료된 시료는 분 석 전까지 –20°C에 보관되었으며 향기 및 생리활성물질 분 석 직전 상온에서 해동한 후, 분쇄기(IKA, A11 basic, USA)를 이용하여 30초간 분쇄하고 40 mesh의 체를 통과 하여 얻어진 가루를 분석에 이용하였다.
향기성분 분석
향기성분의 분석을 위하여 시료 분말 2.0 g을 25 ml headspace (HS) vial에 넣고 내부표준물질로 100 μl의 2-acetylpyrrole (100 ppm)을 넣은 후 magnetic cap으로 밀봉하였다. 향기 성분을 흡착시키기 위하여 solid phase microextraction (SPME) 방법을 사용하였는데, 흡탈착용 fiber로는 divinylbenzene/ carboxen/PDMS (57348-U, Supelco, USA)를 이용하였다. 시료와 내부표준물질을 함유한 headspace vial을 분석 전 20분간 preheating을 한 후 동일한 온도에서 20분간 흡착을 진행하고 이를 gas chromatography mass spectrometer (GCMS; QP-2010 Ultra, Shimadzu, Japan)의 injector(250°C)에서 10분간 탈착하였다. 향기 성분의 분리를 위하여 Rtx-5MS 컬럼(30 m × 0.25 mm ID)을 이용하였으며 oven 온도는 초 기 40°C에서 5분간 유지 후 160°C에 도달할 때까지 분당 3°C의 속도로 증가시켰으며, 이후 270°C까지 다시 분당 20°C의 속도로 온도 증가시킨 후 5분간 유지하였다. 컬럼의 유속은 1 ml·min -1 이었으며 질량분석기의 ion source 온도 는 200°C, interface 온도는 270°C를 유지하였다. 향기 성분 의 동정은 mass spectrum에 기초한 Wiley (ver. 9) 및 NIST (ver. 11) library 검색을 우선적으로 수행하였으며, 추가적으 로 n-alkane을 이용하여 얻어진 retention index의 +/- 20 내 의 검색 결과를 확인하며 수행되었다. GCMS에 의하여 검출 되는 모든 종류의 휘발성 물질 중에는 실제 인간의 감각기관 으로는 느껴지지 않는 다수의 성분이 포함되어 있는 바, Volatile Compounds in Food Library (Nijssen et al., 2016) 에서 향기특성이 언급된 성분들만을 본 연구에 제시하였다.
Tocols, squalene 및 phytosterols 분석
벼 종실중 지용성 생리활성물질인 tocol류(α -, β -, γ -, δ -tocopherol 및 α -, β -, γ -, δ -tocotrienol)와 squalene 및 phytosterol류(campesterol, stigmasterol, sitosterol)의 정량 분석은 Jung et al. (2008)의 방법에 준하여 실행되었다. 즉, 분말시료 0.5 g을 0.1 g의 ascorbic acid가 포함된 시험관에 넣고 5 ml EtOH을 넣은 후, 80°C shaking water bath에서 10분간 추출하고, 즉시 44% KOH 150 μl를 넣고 다시 80°C shaking water bath에서 18분간 비누화 반응을 진행하였다. 반응의 종료 즉시 얼음에 넣어 냉각 시킨 후 증류수 5 ml와 hexane 5 ml을 넣어 교반하고 이를 원심분리(5°C, 1,000 rpm, 1분)하여 상징액을 모으는 과정을 3회 반복하여 수행하고, 이를 다시 증류수 5 ml로 3회 세척한 후 Na2SO4에 통과시 키면서 수분을 제거한 후, 질소농축기를 이용하여 hexane 을 제거한 후 isooctane 1 ml에 재용해하여 gas chromatographymass spectrometry(GC-MS, QP-2010 Ultra, Shimadzu, Japan) 로 분석하였다. GC 컬럼은 BR-5 (25 m × 0.25 mm)를 사 용하였으며 1.20 ml·min -1 의 유속과 1:5의 split ratio를 적 용하였다. 컬럼 오븐의 온도는 초기 240도에서 1분간 유지 하다 290°C까지 분당 3°C씩 증가시킨 후 15분간 유지하였 다. GC-MS의 ion source와 interface 온도는 각각 200°C와 280°C를 유지하였으며, 동정과 성분정량을 위해 사용된 selected ion mode 에서의 각 성분별 m/z는 다음과 같았다; squalene: 69, δ -tocopherol: 402, β - 및 γ -tocopherol: 416, δ -tocotrienol: 346, α -tocopherol: 430, β - 및 γ -tocotrienol: 410, campesterol: 400, α-tocotrienol: 424, stigmasterol: 412, β -sitosterol: 414. 각 성분은 authentic standard (Supelco)의 retention time 과 농도대비 peak 면적의 calibration curve를 사용하여 수 행하였다.
지방산 조성 분석
지방산 분석은 Cho et al. (2006)에 준하여 수행하였는데, 시료 가루 0.2 g을 1.5ml amber vial에 넣은 후 680 μl의 methylation mixture 용액(MeOH: benzene: 2,2-dimethoxypropane: H2SO4 = 39: 20: 5: 2) 680 μl와 혼합하고 vortexing 하여 균일하게 섞은 후, 400 μl의 heptane을 넣고 완전밀봉 한 후 2시간동안 80°C의 수욕상에서 가열하였다. 가열 완 료된 vial은 상온에서 방냉하고 원심분리 (12,000 rpm)를 하여 상층의 heptane 층을 150 μl 유리 insert가 넣어진 vial 에 담은 후 GC gas chromatography (MODEL: Shimadzu Japan) 로 분석하였다. GC의 분석 조건으로 column은 CP-SIL 88 CB FAME (100m × 0.25 mm)을 사용하였으며, injector와 FID 검출기의 온도는 210°C이었으며 oven temperature는 초기 100°C에서 5분간 유지한 후 180°C 까지 4°C/min 속도 로 증가하고 이를 5분간 유지한 후, 다시 210°C까지 5°C/min 로 증가하였다. 외부표준물질로 37 종의 Fatty Acid Methyl Ester(FAME) 가 혼합된 표준물질(Supelco, USA)을 사용 하여 retention time을 비교하였으며, 각 지방산의 조성 비 율은 전체 지방산의 peak면적 합계에 대한 각 성분 peak area의 백분율(%)을 계산하여 표기하였다.
통계 분석
모든 성분의 분석은 3회의 독립적인 분석 반복을 수행하 였으며, 얻어진 결과는 SPSS (ver. 22)를 이용하여 평균, 표 준편차 등 통계량을 구하고 t-test를 수행하였으며 이 때 유 의수준은 5%를 유지하였다. 향기 성분의 다변량분석은 MetaboAnalyst (version 3.0, http://www.metabolanalyst.ca, Xia et al., 2015)를 이용하여 수행하였는데, 이 때 각 성분 의 peak area 값은 처리, 혹은 반복간 편차의 보정을 위하 여 내부 표준물질인 2-acetylpyrrole을 기준으로 normalization 을 수행한 후, 면적이 크고 작은 여러 성분들 간의 변화의 상대적 비교를 위하여 이를 다시 Z-score로 보정하여 분석 에 이용하였다.
결과 및 고찰
발아에 따른 향기 성분의 변화
향미벼의 발아 전, 후 동정된 휘발성분(volatiles) 중에서, 인간의 감각기관에서 느껴지지 않는 단순 휘발성 성분들을 제외하고 특정 향기 특성을 가진 것으로 묘사가 가능한(VCF ver. 16.2, 2016) 성분들을 선별한 결과, 발아 전 52개, 발아 후 51개 등 총 56개 성분이 확인되었다(Fig. 1, Table 1). 이 들 성분을 화학적 특성에 따라 분류할 때 hydrocarbon류 16개(29%), alcohol류 13개(23%), aldehyde류 12개(21%), ketone류 8개(14%), ester류 4개(7%), bases류, furan류 및 sulfur compound류 각각 1개씩 이었으며, 이러한 향기성분 의 구성 비율은 발아 전과 발아 후의 차이는 없는 것으로 나타났다.
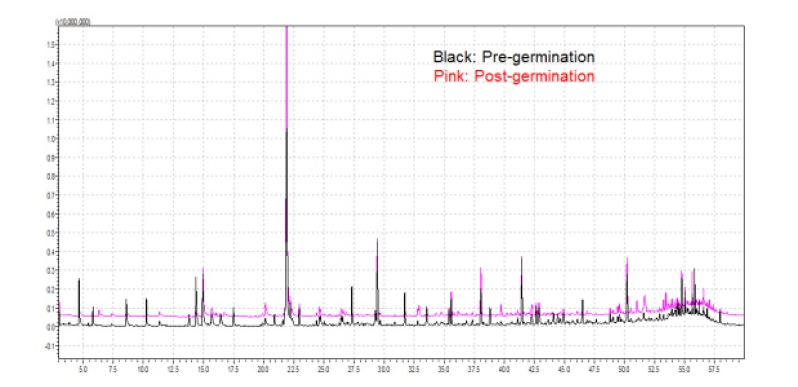
Fig. 1.
Chromatograms of scented rice at pre- and post-germination stages. Rice grains at the pre- and post-germination were placed in a headspace vial, and the volatile compounds were analysed by using a gas chromatography-mass spectrometry (GC-MS) combined with solid phase microextraction (SPME) system.
Table 1
Changes in odor-active compounds during germination in scented rice.
| No. | Group | Flavor compound | Pre-germination | Post-germination | Change | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| Peak Area | STD1) | Composition (%)2) | Peak Area | STD1) | Composition (%)2) | Difference3) | Ratio4) | |||
| 1 | 1-Butanol, 2-methyl- | 69,142 | 15,144 | 0 | 84,001 | 44,829 | 0.1 | 14,859 | 121% | |
| 2 | 1-Butanol, 3-methyl- | 63,020 | 7,774 | 0 | ND5) | - | - | -63,020 | 0% | |
| 3 | 1-Decanol | 517,940 | 86,242 | 0.3 | 832,454 | 28,835 | 0.7 | 314,514 | 161% | |
| 4 | 1-Decanol, 2-methyl- | 1,957,911 | 228,543 | 1.3 | 1,744,089 | 252,128 | 1.5 | -213,822 | 89% | |
| 5 | 1-Heptanol | 3,358,756 | 171,083 | 2.2 | 385,120 | 76,350 | 0.3 | -2,973,636 | 11% | |
| 6 | 1-Hexanol | 9,167,290 | 1,897,081 | 6.0 | 1,431,025 | 278,871 | 1.2 | -7,736,265 | 16% | |
| 7 | Alcohol | 1-Hexanol, 2-ethyl- | 1,689,123 | 475,488 | 1.1 | 2,920,194 | 541,912 | 2.5 | 1,231,071 | 173% |
| 8 | 1-Nonanol | 5,716,467 | 530,519 | 3.7 | 237,321 | 47,108 | 0.2 | -5,479,147 | 4% | |
| 9 | 1-Octanol | 9,669,464 | 1,044,510 | 6.3 | 2,705,326 | 387,457 | 2.3 | -6,964,139 | 28% | |
| 10 | 1-Octanol, 2-butyl- | 753,179 | 107,279 | 0.5 | 1,009,992 | 109,947 | 0.9 | 256,813 | 134% | |
| 11 | 1-Octen-3-ol | 1,403,123 | 155,815 | 0.9 | 996,775 | 200,087 | 0.9 | -406,348 | 71% | |
| 12 | 2-Octen-1-ol, (E)- | 1,843,662 | 170,502 | 1.2 | 1,455,115 | 196,319 | 1.2 | -388,547 | 79% | |
| 13 | Menthol | 323,090 | 34,524 | 0.2 | 249,855 | 46,612 | 0.2 | -73,234 | 77% | |
| 14 | 2-Decenal, (E)- | 4,450,053 | 656,680 | 2.9 | 1,576,800 | 83,391 | 1.4 | -2,873,253 | 35% | |
| 15 | 2-Heptenal | 1,311,488 | 52,772 | 0.9 | 1,133,423 | 103,620 | 1.0 | -178,065 | 86% | |
| 16 | 2-Nonenal, (E)- | 2,107,399 | 154,810 | 1.4 | 1,867,551 | 137,194 | 1.6 | -239,848 | 89% | |
| 17 | Benzaldehyde | 1,948,343 | 142,257 | 1.3 | 6,304,800 | 249,897 | 5.4 | 4,356,457 | 324% | |
| 18 | Benzeneacetaldehyde | 980,164 | 170,664 | 0.6 | 700,656 | 66,587 | 0.6 | -279,507 | 71% | |
| 19 | Alde- | Decanal | 5,763,721 | 936,857 | 3.8 | 6,437,514 | 485,419 | 5.5 | 673,793 | 112% |
| 20 | hyde | Heptanal | 794,688 | 33,013 | 0.5 | 968,111 | 60,517 | 0.8 | 173,423 | 122% |
| 21 | Hexanal | 5,823,508 | 650,312 | 3.8 | 4,118,691 | 756,900 | 3.5 | -1,704,817 | 71% | |
| 22 | Nonanal | 17,545,917 | 2,961,413 | 11.5 | 22,570,891 | 3,184,172 | 19.4 | 5,024,973 | 129% | |
| 23 | Octanal | 4,491,752 | 37,561 | 2.9 | 4,148,884 | 624,135 | 3.6 | -342,869 | 92% | |
| 24 | Pentadecanal- | 614,542 | 206,644 | 0.4 | 2,351,497 | 390,061 | 2.0 | 1,736,955 | 383% | |
| 25 | Pentanal | 152,774 | 23,930 | 0.1 | 150,342 | 69,575 | 0.1 | -2,433 | 98% | |
| 26 | Bases | 2-Acetyl-1-pyrroline | 5,371,558 | 159,685 | 3.5 | 566,425 | 32,407 | 0.5 | -4,805,133 | 11% |
| 27 | Acetic acid, phenylmethyl ester | ND | - | - | 2,795,942 | 288,565 | 2.4 | 2,795,942 | ||
| 28 | Esters | Hexadecanoic acid, methyl ester | 993,775 | 437,153 | 0.6 | 374,618 | 89,570 | 0.3 | -619,156 | 38% |
| 29 | Hexanoic acid, methyl ester | 149,853 | 27,558 | 0.1 | ND | - | -149,853 | 0% | ||
| 30 | n-Propyl acetate | ND | - | - | 19,932 | 3,333 | 0.0 | 19,932 | ||
| 31 | Furan | Furan, 2-pentyl | 9,045,473 | 922,552 | 5.9 | 4,325,234 | 688,550 | 3.7 | -4,720,239 | 48% |
| 32 | 1-Pentadecene | 610,075 | 30,969 | 0.4 | 3,129,104 | 242,528 | 2.7 | 2,519,029 | 513% | |
| 33 | Benzene | 10,025,814 | 137,470 | 6.6 | 7,573,613 | 2,629,137 | 6.5 | -2,452,201 | 76% | |
| 34 | Benzene, 1,3,5-trimethyl- | 3,772,188 | 154,201 | 2.5 | 1,742,075 | 182,497 | 1.5 | -2,030,113 | 46% | |
| 35 | Decane | 410,129 | 38,862 | 0.3 | 152,844 | 24,069 | 0.1 | -257,286 | 37% | |
| 36 | Dodecane | 3,924,218 | 226,506 | 2.6 | 2,350,555 | 100,600 | 2 | -1,573,662 | 60% | |
| 37 | Ethene, tetramethoxy- | ND | - | - | 1,639,177 | 397,699 | 1.4 | 1,639,177 | ||
| 38 | Ethylbenzene | 2,726,600 | 303,471 | 1.8 | ND | 102,529 | 0.7 | -1,919,476 | 30% | |
| 39 | Hydrocar | Heptane, 2,2,4-trimethyl- | 164,823 | 20,141 | 0.1 | - | - | -164,823 | ||
| 40 | bone | Heptane, 3,3,5-trimethyl- | 159,428 | 38,305 | 0.1 | 1,216,455 | 189,304 | 1.0 | 1,057,027 | 763% |
| 41 | Heptane, 3-[(ethenyloxy)methyl]- | 201,515 | 32,388 | 0.1 | 103,431 | 22,324 | 0.1 | -98,085 | 51% | |
| 42 | Hexadecane | 1,747,002 | 410,950 | 1.1 | 1,508,368 | 311,172 | 1.3 | -238,634 | 86% | |
| 43 | o-Xylene | 1,803,025 | 224,042 | 1.2 | 1,064,130 | 130,956 | 0.9 | -738,895 | 59% | |
| 44 | Pentadecane | 1,730,571 | 186,832 | 1.1 | 338,860 | 45,420 | 0.3 | -1,391,711 | 20% | |
| 45 | Tetradecane | 6,670,047 | 688,382 | 4.4 | 3,111,267 | 226,010 | 2.7 | -3,558,780 | 47% | |
| 46 | Toluene | 6,115,610 | 1,786,946 | 4.0 | 2,994,286 | 617,616 | 2.6 | -3,121,323 | 49% | |
| 47 | Tridecene | ND | - | - | 877,264 | 64,260 | 0.8 | 877,264 | ||
| 48 | 2,3-Butanedione | 130,565 | 9,587 | 0.1 | 49,065 | 16,819 | 0.0 | -81,499 | 38% | |
| 49 | 2-Heptanone | 483,258 | 33,423 | 0.3 | 2,352,088 | 429,956 | 2.0 | 1,868,829 | 487% | |
| 50 | 2-Nonanone | 239,010 | 30,184 | 0.2 | ND | - | - | -239,010 | ||
| 51 | Ketone | 2-Octanone | 491,897 | 8,774 | 0.3 | 84,408 | 15,677 | 0.1 | -407,489 | 17% |
| 52 | 2-Pentadecanone, 6,10,14-trimethyl- | 1,815,482 | 170,606 | 1.2 | 1,238,274 | 18,038 | 1.1 | -577,208 | 68% | |
| 53 | 3-Hexanone | 2,649,881 | 414,904 | 1.7 | 1,910,939 | 872,842 | 1.6 | -738,941 | 72% | |
| 54 | 5,9-Undecadien-2-one, 6,10-dimethyl | 2,582,557 | 467,555 | 1.7 | 1,300,721 | 128,307 | 1.1 | -1,281,836 | 50% | |
| 55 | 5-Hepten-2-one, 6-methyl- | 3,307,484 | 434,580 | 2.2 | 3,749,357 | 431,059 | 3.2 | 441,872 | 113% | |
| 56 | Sulfur compounds | Dimethyl trisulfide | 227,172 | 10,004 | 0.1 | ND | - | - | -227,172 | 0% |
2)Composition (%) : (Peak area of each peak/total peak area of a column) × 100 (%)
3)Difference : Peak area at pre-germination stage peak area at at post-germination stage
4)Ratio : (Peak area at post-germination stage/peak area at pre-germination stage) × 100 (%)
5)ND : Not detected
GCMS chromatogram상 나타난 모든 peak들의 면적 합 계를 100%로 하여 각 성분별 peak 면적을 상대적 함량(%) 의 지표로 분석한 결과, nonanal이 발아 전에는 전체의 11.5% 를, 발아 후에는 19.4%를 차지하는 주요 구성 성분이었으 며, nonanal 이외에도 발아 전 종실에는 benzene(6.6%), 1- octanol(6.3%), 1-hexanol(6.0%)과 furan, 2-pentyl (5.9%) 이, 발아 후 종실에는 benzene(6.5%), decanal(5.5%) 및 benzaldehyde(5.4%)가 주요 성분으로 나타났다.
향미벼의 향기 성분 함량은 발아로 인하여 증가한 경우 도, 감소한 경우도 발견되었는데, 발아 전(100%)과 비교할 때, 13개의 향기성분, 특히 heptane,3,3,5,-trimethyl-과 1-pentadecene, 2-heptanone, 그리고 pentadecanal 및 benzaldehyde가 각각 763%, 513%, 487%, 383%, 및 324%의 함량 증가를 나타 내었다. 그러나 동정된 56개 향기 성분 중 대부분을 차지하 는 39개 성분은 발아로 인한 함량의 감소가 관찰되었다. 특 히 1-nonanol, 2-acetyl-1-pyrroline, 1-heptanol, 1-hexanol, 2-octanone, pentadecane, 1-octanol 등은 발아 후에는 발아 전 함량(100%) 대비 각각 4%, 11%, 11%, 16%, 17%, 20%, 28% 수준까지 뚜렷하게 감소되었다. 이러한 본 연구 결과 는 수확 후 건조 및 저장 조건에 따라 향기성분이 크게 영 향을 받고 감소한다는 Baradi and Elepano(2012)의 보고와 일치하는 경향이었다. 향미벼에서 ‘팝콘향’, 혹은 ‘누룽지향’ 을 나타내는 주요 향기성분으로 알려진 2-acetyl-1-pyrroline은 발아로 인하여 89%가 감소하고 약 1/10 수준으로 그 함량 이 저하되었음을 감안할 때, 향미벼를 이용한 발아 현미 제 조를 위해서는 세척 시간의 단축과 발아 온도 및 기간의 조 정 등 더욱 세밀한 공정의 개발과 주의가 필요함을 시사하 는 것으로 판단되었다.
한편, 일부 향기 성분의 경우 발아 전후로 존재 여부가 달라지기도 하였는데, 발아 전 관찰되었던 2-nonanone 등 5개 성분은 발아 후에는 관찰되지 않아 발아의 과정 중 소 멸된 것으로 나타났다. 그러나 이들 성분이 모두 발아 전 구성 비율이 0.2% 미만의 매우 작은 크기의 성분이었음을 고려할 때, 정성적인 존재 여부로 평가하기 보다는 낮은 함 량 수준의 해당 성분이 발아로 인하여 더욱 그 함량이 감소 한 결과 본 연구의 분석조건 하에서 검출 한계 미만으로 저 하된 때문에 기인한 것으로 판단되었다. 한편 발아로 인하 여 새롭게 생성된 4개 성분이 관찰되었는데, 이들 중 acetic acid, phenylmethyl ester와 ethene, tetramethoxy등 2개 성 분은 peak 면적의 구성 비율이 전체의 2.5%, 1.5%를 차지 하는 것으로 나타나 발아의 과정 중 새롭게 생성된 휘발성 물질임을 알 수 있었다.
향기 성분의 profile에 기초한 발아 전 후의 비교를 위하 여 partial least squares-discriminant analysis(PLS-DA) 분 석을 수행한 결과 Fig. 2와 같이 향기성분의 특성에 따라 발아 전과 발아 후는 뚜렷하게 구별이 가능하였으며, component 1의 75.1%와 component 2의 12.5% 등 합계 87.3%의 설명 력을 갖는 것으로 나타났다. Variable Importance in Projection (VIP) score 분석을 수행한 결과, 2-acetyl-1-pyrroline, 2-octanone, dimethyl trisulfide와 1-hepanol 등의 성분은 발아 전에서, benzaldehyde, tridecene, 1-pentadecene 등의 성분은 발아 후에 뚜렷하게 존재하는 것으로 나타났다(Fig. 3). 본 VIP 분석 결과 제시된 상기 성분들과 Table 1에서 발아 전후 peak 면적, 혹은 변화 비율이 높게 나타난 성분과 상이한 것은, 상이한 면적을 갖는 여러 성분들의 상대적 변화를 고 려하기 위하여 PLS-DA 분석 과정 중 Z-score를 이용하여 VIP score가 계산된 때문으로 판단되었다.
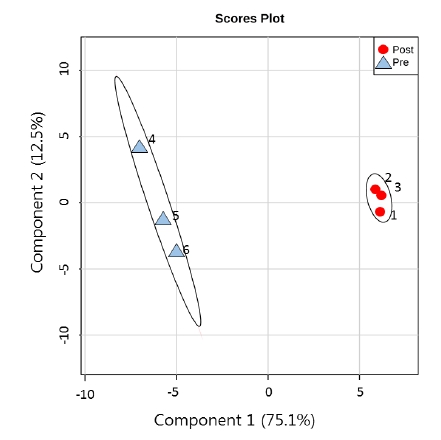
Fig. 2.
Partial least square-discriminant analysis (PLS-DA) plot of the flavoring compounds observed at preand post-germination stages in scented rice.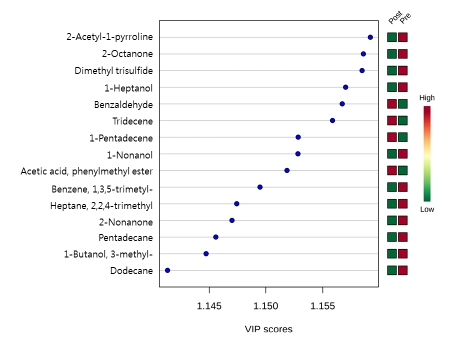
Fig. 3.
Variable importance in projection (VIP) plot of the flavoring compounds observed at the pre- and postgermination stages in scented rice/비록 본 연구의 수행으로 발아 전후 향기성분의 변화는 확인되었으나, 이는 olfactory에 기초한 연구가 수행되지 않 은 채 GCMS의 chromatogram 상에 나타나는 각 성분의 peak 면적의 변화에 기초한 것이며, 특히 SPME fiber의 흡 착도가 상이할 수 있는 다수의 휘발성 성분을 대상으로 수 행된 것임을 감안할 때 실제 소비자가 감지할 수 있는 발아 전 후 향기 성분의 절대량 변화, 그리고 그에 따른 선호도 변화에 대하여는 관능평가 전문가를 활용한 panel test 등 추가적인 연구가 필요할 것으로 판단되었다.
발아에 따른 생리활성 물질 함량의 변화
향미벼의 발아는 본 실험에서 평가된 모든 생리활성물질 들의 함량 감소를 가져왔는데(Table 2), campesterol과 sitosterol, stigmasterol 및 총 phytosterol 함량은 발아 전 29.94 μg g -1 , 138.64 μg g -1 , 39.38 μg g -1 및 207.97 μg g -1으로부터 발아 후 21.02 μg g -1 , 86.07 μg g -1 , 29.57 μg g -1 , 136.66 μg g -1 으로 낮아져 약 25% ~ 38%의 함량 감소를 나타내었다. Squalene 역시 발아 전 31.74 μg g -1로부터 발아 후에는 25.12 μg g -1로 약 21% 함량이 감소하였다. 대표적인 항산 화 물질인 α-tocopherol 및 항암성 효과가 우수한 것으로 알려진 γ -tocotrienol 등 vitamin E 성분들(tocols)의 경우도 모든 isomer들이 발아를 거치며 20.3% (β -tocopherol) ~ 35.8% (γ -tocotrienol)감소하는 것으로 나타났다. 발아로 인 한 생리활성물질의 함량 변화에 대하여 Jung et al. (2008) 은 벼 품종에 따라 정도의 차이는 있지만 stigmasterol의 경우 발아로 인하여 5 ~ 27%가 증가하나, 그 밖의 phytosterol류 및 tocols, squalene 함량은 뚜렷하고 공통적인 함량 변화는 없었다고 보고하였고, Kwak et al. (2013)은 발아 현미로부 터 추출된 현미유의 경우 발아로 인하여 phytosterol류와 squalene의 함량은 높아진 반면 tocols와 γ -oryzanol 함량은 감소한 것을 보고하였다. Shu et al. (2008)은 발아의 시작 후 48 ~ 72시간까지 campesterol, stigmasterol, sitosterol이 증가하는 경향을 보이다 이후에는 증가가 둔화되거나 오히 려 함량이 감소하는 경향을 보고하였다. 이러한 각 보고별 차이는 사용된 품종에 따라서, 그리고 발아의 온도와 경과 시간 및 발아 중의 관수 여부 등에 따른 차이로 판단되는 데, 본 실험에 사용된 향미벼 품종을 사용하여 적용된 발아 공정에 따라 발아현미를 제조할 경우 생리활성물질들의 함 량 감소 가능성이 높을 것으로 판단되며, 따라서 보다 생리 활성물질 함량을 증대할 수 있거나 최소한 유지할 수 있는 발아 조건의 탐색이 필요할 것으로 판단되었다.
Table 2
Germination-induced changes in phytosterol, squalene, and tocol contents (μg g-1) in scented rice.
발아에 따른 지방산 조성의 변화
발아 전 향미벼 종실의 주요 지방산은 linoleic acid (36.6%), oleic (34.2%) 및 palimtic (24.4%) 등이었으며, 이러한 주 요 지방산의 종류는 발아 이후에도 변함이 없었다(Table 3). 그러나 발아로 인하여 조성 비율은 차이가 나타났는데, linoleic acid와 oleic acid는 발아 후 37.9%와 36.9%로 각 각 1.3%와 2.7%가 증가한 반면 palmitic acid의 경우는 발 아 후 20.7%로 3.7%가 감소하였다. 이러한 지방산 조성 비 율의 변화는 발아로 인한 linoleic acid의 증가와 palmitic acid의 감소를 보고한 Kim et al. (2012)와는 일치하고, 발 아현미유에서 발아 전보다 유의하게 증가한 oleic acid와 소폭 감소를 나타낸 palmitic 및 oleic acid를 보고한 Kwak et al. (2013)과는 유사한 결과였으나, 일품벼와 거대배아미 인 큰눈벼의 발아 24시간 경과 시 oleic acid는 감소하나 linoleic acid와 palmitic acid는 증가하는 경향을 보고한 Choi et al. (2009)의 결과와는 상반되는 경향이었다. 이러한 발아 중 지방산 조성 비율 변화의 각 보고서별 차이는 앞서 tocols 등 생리활성에서 관찰되었듯이 실험 대상 품종과 발 아 조건 등의 차이에 따른 것으로 판단되었다.
Table 3
Germination-induced changes in fatty acid composition (%) in scented rice.
| Fatty acid | Pre-germination | Post-germination | p value1) | ||
|---|---|---|---|---|---|
| Mean | STD | Mean | STD | ||
| Myristic acid (14:0) | 0.98 | 0.03 | 0.57 | 0.03 | 0.004 |
| Palmitic acid (16:0) | 24.40 | 0.33 | 20.72 | 0.01 | 0.004 |
| Palmitoleic acid (16:1) | 0.11 | 0.01 | 0.13 | 0.00 | 0.053 |
| Stearic acid (18:0) | 1.51 | 0.02 | 1.44 | 0.00 | 0.038 |
| Oleic acid (18:1) | 34.16 | 0.11 | 36.92 | 0.45 | 0.014 |
| Linoleic acid (18:2) | 36.63 | 0.36 | 37.86 | 0.52 | 0.112 |
| Linolenic acid (18:3) | 1.17 | 0.00 | 1.2 | 0.01 | 0.035 |
| Arachidic acid (20:0) | 0.38 | 0.01 | 0.43 | 0.00 | 0.036 |
| Eicosenoic acid (20:1) | 0.34 | 0.01 | 0.41 | 0.02 | 0.061 |
| Behenic acid (22:0) | 0.31 | 0.00 | 0.33 | 0.01 | 0.210 |
적 요
새로운 식품 소재의 개발을 목적으로 향미벼 신품종을 이용하여 발아현미를 제조하고 발아 전 후 종실에 함유된 향기성분과 생리활성 물질, 그리고 지방산 조성의 변화를 관찰한 결과는 다음과 같다.
향기성분은 발아 전 52개, 발아 후 51개 등 총 56개 성분이 동정되었으며 이들은 hydrocarbon(29%)과 alcohol (23%) 및 aldehyde(21%)류로 분류되었으며, 주요 향 기성분으로는 nonanal, benzene, 1-octanol, 1-hexanol, furan, decanal 등이 동정되었다.
발아로 인하여 heptane,3,3,5-trimethyl, 1-pentadecene, 2-heptanone 등 13개 성분은 함량이 증가한 반면, 향 미벼 특유의 팝콘향을 나타내는 2-acetyl-1-pyrroline 을 비롯하여 1-nonanol, 1-heptanol, 1-hexanol 등 39 개 성분은 발아로 인하여 함량이 감소하였다.
향기 성분의 함량을 이용한 PLS-DA 분석 시 뚜렷하 게 향기 특성에 따라 발아 전과 발아 후의 구별이 가 능하였으며, 2-acetyl-1-pyrroline, 2-octanone 등은 발 아 전의, 그리고 benzaldehyde, tridecene 등은 발아 후 의 특징적인 향기성분으로 나타났다.
발아된 향미벼의 campesterol, stigmasterol, sitosterol 등 phytosterol류와 squalene, 그리고 5종의 tocols 등 생리활성물질 함량은 모두 발아 전에 비해 낮은 것으 로 나타났다.
향미벼의 주요 지방산은 linoleic, oleic 및 palmitic acid였으며 발아로 인하여 linoleic acid와 oleic acid는 각각 1.3%, 2.7%의 증가하고 palmitic acid는 3.7%의 조성 비율이 감소하는 것으로 나타났다.




